Clear Sky Science · de
Photokatalytische stereoselektive Umgestaltung von Alkynen zu 3D‑Molekülen mittels Wasserstoffatom‑Transfer‑vermittelter dynamischer Epimerisierung
Warum aus flachen Molekülen 3D‑Formen zu machen wichtig ist
Viele moderne Arzneistoffe entstehen aus flachen, blattartigen Molekülbausteinen, die sich leicht herstellen lassen, aber im Körper nicht immer ideal sind. Wirkstoffforscher haben festgestellt, dass kompakte dreidimensionale Grundgerüste oft vorteilhafter reagieren: Sie passen sich Zielstrukturen im Körper besser an, verhalten sich anders im Organismus und verursachen mitunter weniger Nebenwirkungen. Dieser Artikel beschreibt eine neue, lichtgetriebene Methode, einfache, flache molekulare „Drähte“ in einem Schritt zu komplexen 3D‑Käfigen zu formen, was die Suche nach neuen Wirkstoffen und funktionalen Materialien beschleunigen könnte.
Von geraden Linien zu winzigen Käfigen
Die meisten klassischen Verfahren zum Aufbau dieser käfigartigen Strukturen, so genannter überbrückter Ringe, gehen einen längeren Weg: Chemiker erzeugen zunächst relativ flache Ringsysteme und verbinden diese dann in einem zweiten Schritt. Diese zweistufige Strategie funktioniert, ist aber zeitaufwändig und schränkt die erreichbaren Formen ein. Die Autoren gehen stattdessen von sehr einfachen eindimensionalen Bausteinen aus: linearen Alkynen (Kohlenstoff‑Kohlenstoff‑Dreifachbindungen) und Aldehyden (kleine Kohlenstoff‑Sauerstoff‑Einheiten). Ihr Ziel ist, direkt von diesen geraden Ketten zu kompakten 3D‑Gerüsten in einer einzigen Operation zu springen, die üblichen Umwege zu vermeiden und neuen „chemischen Raum“ zu erschließen, der für die Wirkstoffgestaltung wertvoll ist.
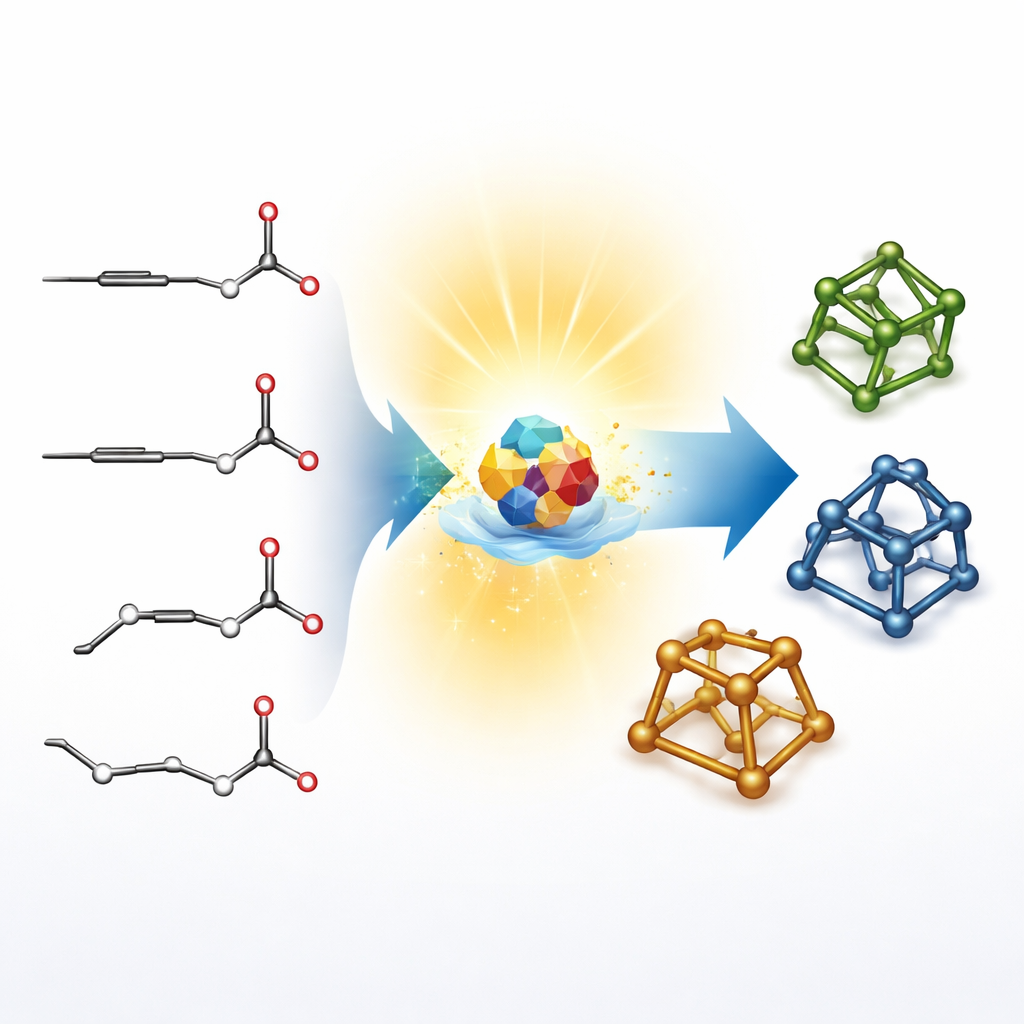
Das Licht die schwere Arbeit tun lassen
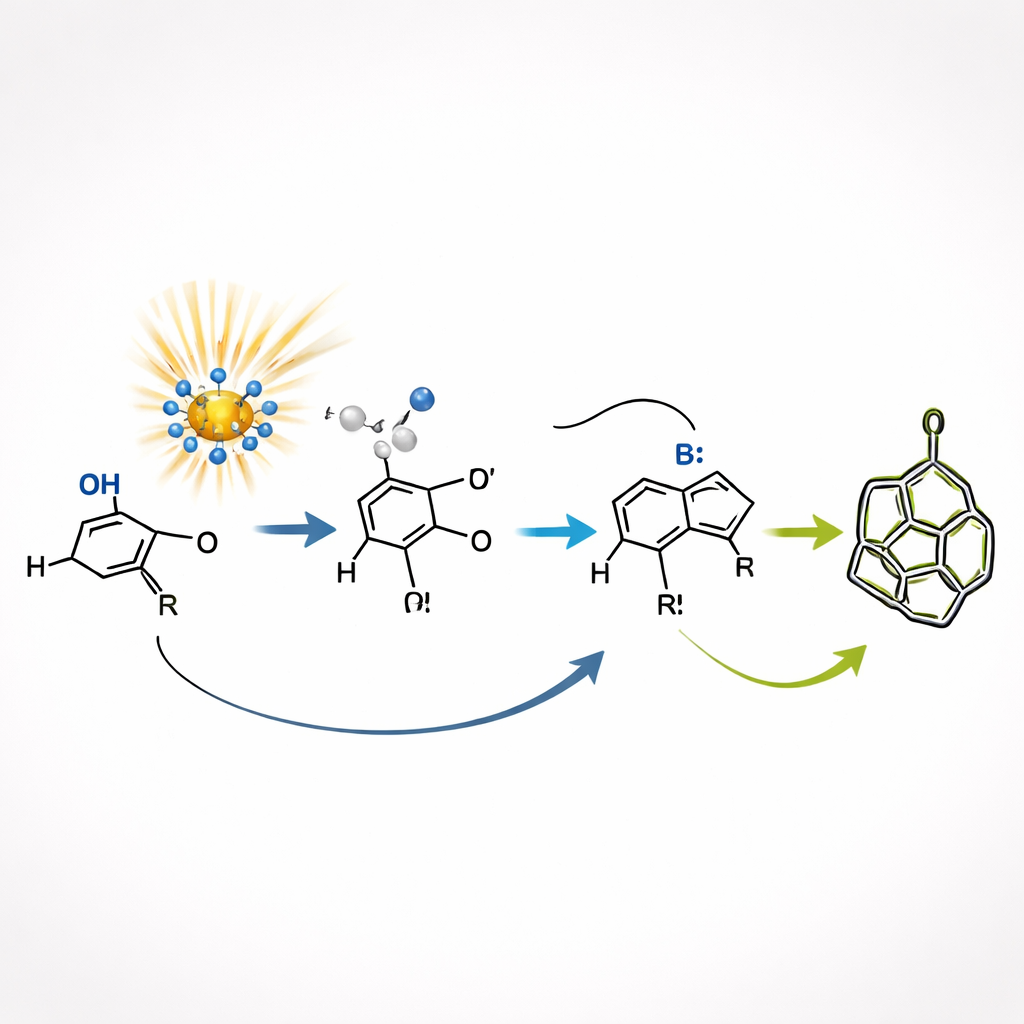
Das Team nutzt einen speziellen lichtempfindlichen Katalysator auf Basis eines Polyoxometallats namens Decatungstat. Unter violettem Licht kann dieser Katalysator ein Wasserstoffatom vom Aldehyd abstrahieren und dadurch kurzzeitig ein sehr reaktives Fragment erzeugen. Dieses Fragment addiert sich über das Alkin, klappt zurück und schließt zu einem fünfgliedrigen Ring. Für sich genommen liefert dieser erste Ringbildungsschritt ein unordentliches Gemisch von 3D‑Anordnungen an wichtigen Kohlenstoffatomen. Der clevere Kniff ist, dass dasselbe lichtgetriebene System diese Anordnungen in Echtzeit umschichten kann, indem es wiederholt Wasserstoffatome entfernt und zurückgibt, sodass das Gemisch zu den stabileren Formen hin „driftet“.
Selbstkorrigierende 3D‑Bearbeitung
Im Zentrum der Entdeckung steht eine eingebaute Selbstkorrektur, bekannt als dynamische kinetische Auflösung. Das anfängliche Ring‑Intermediat existiert in zwei eng verwandten 3D‑Formen, die sich nur in der räumlichen Orientierung der Atome unterscheiden. Durch lichtaktivierten Wasserstofftransport werden diese Formen schnell ineinander umgewandelt, während ein separater, base‑unterstützter Schließschritt nur eine von ihnen für die endgültige Käfigbildung bevorzugt. Dadurch wird das „bevorzugte“ Intermediat kontinuierlich in ein einzelnes, klar definiertes bicyclisches Produkt überführt, während die weniger begünstigte Form permanent in ihr Gegenstück umgewandelt wird. Dieses Zusammenspiel aus reversibler Formumschaltung und selektivem Einfangen liefert Produkte mit exzellenter Kontrolle über die Orientierung an mehreren Positionen, obwohl der erste Schritt selbst recht unselektiv ist.
Aufbau vielfältiger und nützlicher 3D‑Gerüste
Die Autoren zeigen, dass dieser lichtgetriebene Ansatz für eine breite Palette von Ausgangsmaterialien funktioniert und die resultierenden Käfige mit vielen verschiedenen funktionellen Gruppen versieht, die Chemiker gerne als Ankerpunkte nutzen. Sie stellen zwei Familien von Gerüsten her: Bicyclo[2.2.1]heptanone und Bicyclo[3.2.1]octanone, die beide begehrte Bausteine in der Medizinalchemie sind. Diese Strukturen finden sich in Naturstoffen, Katalysatoren und Materialien. Das Team demonstriert außerdem, dass sich ihre 3D‑Käfige in komplexere Verbindungen überführen lassen, darunter ein Schlüsselintermediat für ein elektrolumineszentes Material und eine versteifte Version eines bekannten Gehirnrezeptor‑Blockers. In einem Fall verbesserte der Austausch eines flexiblen Rings im Arzneistoff durch den neu geschaffenen 3D‑Käfig sogar moderat dessen biologische Wirksamkeit.
Eine Abkürzung zu reichhaltigeren Molekülformen
Alltäglich gesprochen zeigt diese Arbeit, wie man einfache, gerade molekulare „Stäbe“ nimmt und mit Licht und einem schlauen Katalysator in einem einzigen Schritt zu präzisen 3D‑„Skulpturen“ faltet. Der Prozess erfüllt zwei Aufgaben zugleich: Er baut das zugrunde liegende Skelett auf und stimmt die räumliche Anordnung der Atome fein ab — und das alles unter milden Bedingungen. Da Alkine häufige, preiswerte Ausgangsstoffe sind, könnte diese Strategie zu einer allgemeinen Abkürzung werden, billige Rohmaterialien in komplexe, wirkstoffähnliche Architekturen zu überführen. Während Chemiker weiter in die Welt dreidimensionaler Moleküle vorstoßen, könnten Werkzeuge wie dieses eine Schlüsselrolle beim Entwurf besser funktionierender Arzneistoffe und Materialien spielen.
Zitation: Gu, Z., Zeng, T., Yuan, Z. et al. Photocatalytic Stereoselective Editing of Alkynes to 3D Molecules via Hydrogen Atom Transfer-Mediated Dynamic Epimerization. Nat Commun 17, 2518 (2026). https://doi.org/10.1038/s41467-026-69219-0
Schlüsselwörter: Photokatalyse, Wasserstoffatom‑Transfer, 3D‑molekulare Gerüste, dynamische kinetische Auflösung, Medizinalchemie