Clear Sky Science · de
Pan-RAF-Inhibitor Exarafenib zielt auf BRAF Klasse II/III NSCLC und offenbart ARAF-KSR1-Resistenz sowie Kombinationsstrategien
Warum diese Forschung für Lungenkrebspatienten wichtig ist
Die meisten Menschen haben schon von zielgerichteten Krebsmedikamenten gehört, die auf spezifische genetische Veränderungen abzielen. Für viele Patientinnen und Patienten mit Lungenkrebs – insbesondere für diejenigen, deren Tumoren seltener auftretende Mutationen im Gen BRAF tragen – wirken die heutigen zielgerichteten Medikamente jedoch oft nicht. Diese Studie stellt ein neues experimentelles Medikament, Exarafenib, vor, das so entwickelt wurde, ein breiteres Spektrum BRAF‑getriebener Tumoren zu treffen, und erklärt, wie Krebszellen versuchen, ihm zu entkommen – wobei Kombinationstherapien aufgezeigt werden, die diese Tumoren länger unter Kontrolle halten könnten.
Eine verborgene Mehrheit übersehener Mutationen
Die Forschenden begannen mit einer grundlegenden Frage: Wie häufig sind die verschiedenen BRAF‑Mutationsarten bei fortgeschrittenen Krebserkrankungen, insbesondere beim nicht‑kleinzelligen Lungenkarzinom (NSCLC)? Mithilfe einer sehr großen Liquid‑Biopsy‑Datenbank mit über 160.000 Patientinnen und Patienten analysierten sie Fragmente tumoraler DNA, die im Blut zirkulieren. Sie fanden heraus, dass BRAF‑Mutationen bei Lungenkrebs in etwa 4–5 % der Fälle vorkommen, was weltweit dennoch viele Tausende Menschen bedeutet. Entscheidend war, dass rund zwei Drittel dieser Lungentumoren sogenannte Klasse‑II‑ und Klasse‑III‑BRAF‑Mutationen trugen – Typen, die von aktuell zugelassenen BRAF‑Medikamenten nicht wirksam adressiert werden. Patientinnen und Patienten mit einer dieser Klassen, insbesondere Klasse II, hatten tendenziell eine kürzere Überlebenszeit als diejenigen mit der bekannteren Klasse‑I‑Mutation, wahrscheinlich weil Klasse‑I‑Patienten Zugang zu etablierten zielgerichteten Therapien haben, während Klasse‑II/III‑Patienten größtenteils Standard‑Chemotherapie oder Immuntherapie erhalten.
Ein Wirkstoff der nächsten Generation, der den gesamten Weg angreift
BRAF ist Teil einer Kaskade von Proteinen (dem MAPK‑Signalweg), die Wachstumssignale von der Zelloberfläche in den Zellkern weiterleitet. Viele bestehende BRAF‑Medikamente wurden so konstruiert, dass sie nur eine mutierte Form blockieren und können sogar verwandte Proteine in normalen Zellen unbeabsichtigt stimulieren. Exarafenib wurde anders entwickelt: Es ist ein „Pan‑RAF“‑Inhibitor, der darauf ausgelegt ist, mehrere RAF‑Familienmitglieder (ARAF, BRAF und CRAF) in Einzel‑ und Paarform zu hemmen und dabei die meisten anderen zellulären Enzyme zu schonen. In biochemischen Tests über Hunderte menschlicher Kinasen blockierte Exarafenib stark alle drei RAF‑Proteine, zeigte aber wenige Off‑Target‑Effekte, was auf ein saubereres Sicherheitsprofil im Vergleich zu früheren Pan‑RAF‑Verbindungen hindeutet.
Starke Effekte in Modellen schwer behandelbarer Tumoren
Das Team testete Exarafenib in einer Reihe von Zelllinien und Mausmodellen mit verschiedenen BRAF‑ und RAS‑Mutationen, darunter realistische, patientenabgeleitete Tumoren. In Zellkulturen bremste Exarafenib das Wachstum und unterdrückte die MAPK‑Signalgebung nicht nur in klassischen BRAF V600E‑Krebszellen, sondern auch in Zellen mit Klasse‑II‑ und Klasse‑III‑Mutationen sowie in vielen RAS‑mutierten Zellen, für die derzeit gute zielgerichtete Optionen fehlen. Bei Mäusen mit Lungentumoren, die diese Veränderungen trugen, verkleinerte oder verlangsamte Exarafenib die Tumoren dosisabhängig und zeigte klare Zusammenhänge zwischen Medikamentenspiegeln, Wegunterdrückung und Tumorantwort. Frühe klinische Daten von zwei Patientinnen bzw. Patienten mit fortgeschrittenem BRAF‑mutiertem Lungenkrebs – einer mit einer seltenen BRAF‑Fusion und einer mit einer Klasse‑II‑Punktmutation – zeigten partielle Remissionen und spürbare Symptomverbesserungen und stützen die Relevanz der präklinischen Arbeiten.
Wie Krebs lernt, das Medikament zu umgehen
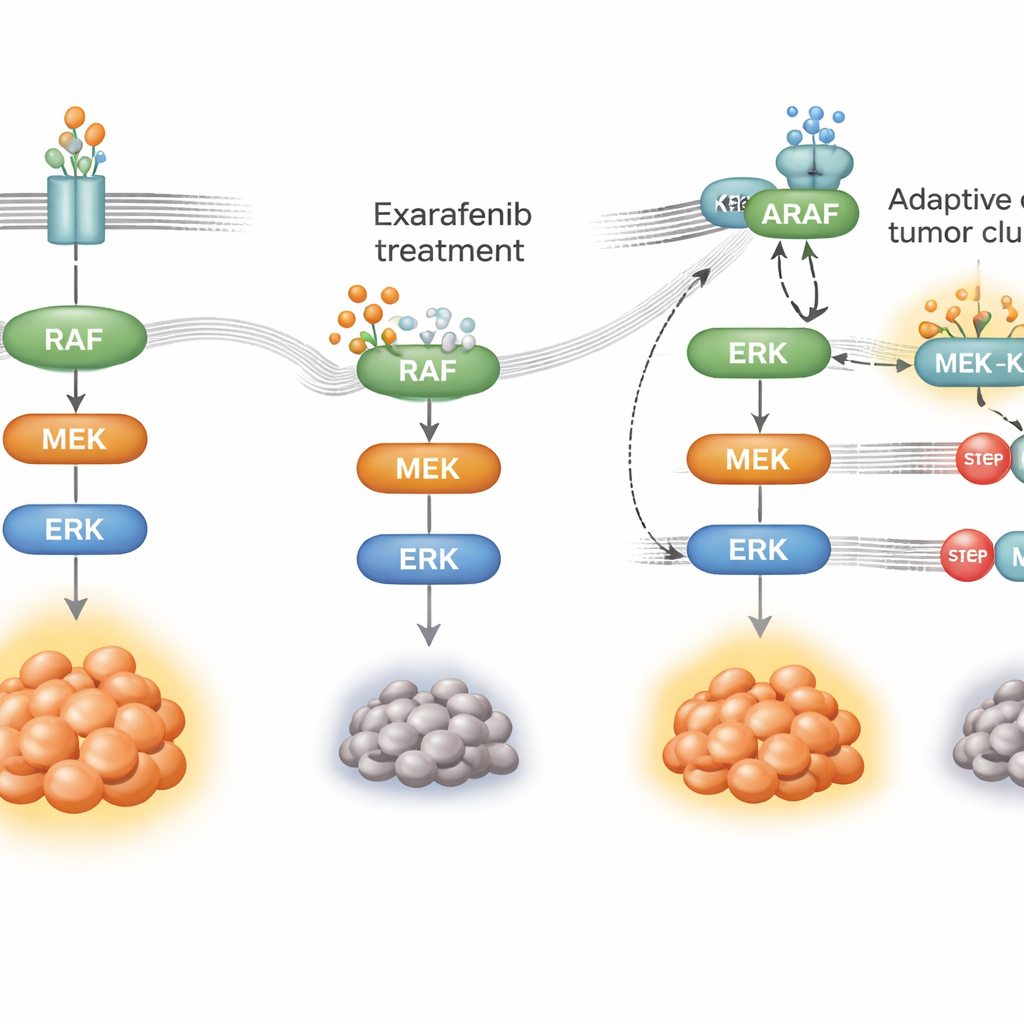
Keine zielgerichtete Therapie wirkt ewig; Krebszellen passen sich an. Um zu untersuchen, wie Tumoren gegen Exarafenib resistieren könnten, setzten die Forschenden BRAF‑mutierte Lungenkrebszellen monatelang dem Wirkstoff aus, bis resistente Populationen entstanden. Diese Zellen waren weiterhin auf denselben Wachstumsweg angewiesen, hatten aber umprogrammiert, wie sie ihn nutzen. Anstatt hauptsächlich von mutiertem BRAF abhängig zu sein, erhöhten sie die Aktivität eines vorgelagerten Schalters namens RAS und verlagerten sich hin zur Nutzung eines anderen Familienmitglieds, ARAF, zusammen mit einem Gerüstprotein namens KSR1. Unter Wirkstoffdruck bildeten ARAF und KSR1 enge Komplexe, die halfen, die MAPK‑Kaskade am Laufen zu halten, obwohl Exarafenib gebunden war. Als die Forschenden ARAF oder KSR1 selektiv stilllegten oder die RAS‑Aktivität reduzierten, wurden die resistenten Zellen wieder empfindlich gegenüber Exarafenib und die Überlebenssignale brachen zusammen.
Kombinationsstrategien, um der Resistenz voraus zu bleiben
Mit dieser mechanistischen Karte suchte das Team nach Partnerwirkstoffen, die den Signalweg an Engstellen blockieren könnten, die sowohl von der ursprünglichen als auch von der Umgehungsroute genutzt werden. Sie fanden heraus, dass die Kombination von Exarafenib mit Wirkstoffen, die MEK oder ERK hemmen – Schlüsselstationen stromabwärts in der MAPK‑Kaskade – in vielen Zell‑ und Mausmodellen starke Synergien erzeugte, einschließlich Tumoren, die von Natur aus weniger empfindlich waren oder bereits Resistenz entwickelt hatten. Diese Kombinationen hielten den Weg länger geschlossen, lösten mehr Zelltod aus und wirkten in Tieren oft ebenso gut oder besser als höhere Exarafenib‑Dosen allein, ohne offensichtliche zusätzliche Toxizität. Wirkstoffe, die direkt RAS anvisieren, verstärkten Exarafenibs Wirkung ebenfalls in Modellen, in denen RAS eindeutig die Resistenz vorantrieb, und stellen somit eine weitere klinisch vielversprechende Taktik dar.
Was das für Patientinnen und Patienten bedeutet
Für Menschen mit NSCLC, die Klasse‑II‑ oder Klasse‑III‑BRAF‑Mutationen tragen – oder komplexe BRAF‑Fusionen und RAS‑Koinmutationen haben – gibt es derzeit keine zugelassenen zielgerichteten Therapien, und die Ergebnisse liegen hinter denen von Patientinnen und Patienten mit häufigeren Veränderungen zurück. Diese Studie liefert starke wissenschaftliche Argumente dafür, dass Exarafenib helfen könnte, diese Lücke zu schließen, indem es RAF‑getriebene Signalgebung breit unterbindet. Sie erklärt auch, wie Tumoren sich über eine ARAF‑KSR1‑Umgehung anpassen können, und zeigt, dass das gleichzeitige Angreifen des Weges auf mehreren Ebenen, insbesondere durch Kombination von RAF‑ und MEK‑Inhibitoren oder durch Hinzufügen von RAS‑Inhibitoren, tiefere und haltbarere Tumorkontrolle liefern könnte. Gemeinsam zeichnen diese Erkenntnisse einen Weg zu klinischen Studien auf, die darauf abzielen, maßgeschneiderte, kombinierte zielgerichtete Therapien für eine große und bislang unterversorgte Gruppe von Lungenkrebspatientinnen und -patienten zu bringen.
Zitation: Manabe, T., Bergo, H.C., Li, Q. et al. Pan-RAF inhibitor exarafenib targets BRAF class II/III NSCLC and reveals ARAF-KSR1 resistance and combination strategies. Nat Commun 17, 2484 (2026). https://doi.org/10.1038/s41467-026-69216-3
Schlüsselwörter: BRAF-mutierter Lungenkrebs, Pan-RAF-Inhibitor, MAPK-Signalisierung, Medikamentenresistenz, kombinierte zielgerichtete Therapien