Clear Sky Science · de
Vererbbare Veränderungen der Chromatinkontakte, verbunden mit transgenerationaler Anfälligkeit für diätinduziertes Insulindysregulation und Fettleibigkeit
Wenn die Ernährung der Ahnen auf moderne Taillen trifft
Warum nehmen manche Menschen leichter zu und entwickeln eher Probleme mit dem Blutzucker als andere, obwohl ihr eigener Lebensstil gesund erscheint? Diese Studie untersucht eine beunruhigende Möglichkeit: dass die Exposition gegenüber bestimmten Industriechemikalien während der Schwangerschaft Nachkommen still und leise „vorausprogrammieren“ kann, sodass diese Generationen später auf fettreiche Nahrung ungünstig reagieren. In Mäusen zeigen die Forschenden einen Mechanismus, über den dieses Risiko ohne Änderung der DNA-Sequenz weitergegeben werden kann, nämlich durch die Umgestaltung der Art und Weise, wie das Genom innerhalb der Zelle gefaltet ist.
Ein Chemikalie mit langem Schatten
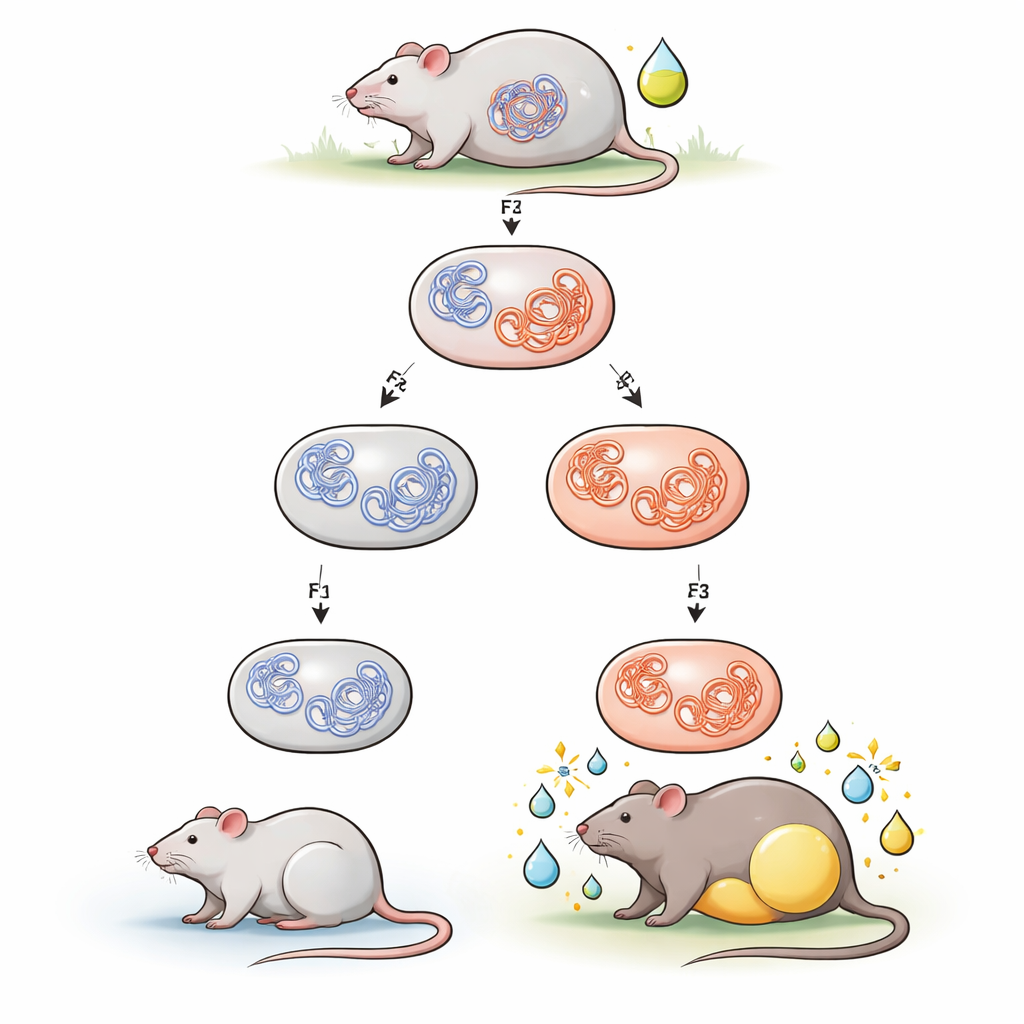
Das Team konzentrierte sich auf Tributyltin, eine einst verbreitete Antifouling- und Industriechemikalie, die als Obesogen gilt, weil sie die Fettspeicherung fördert. Schwangeren Mäusen wurden während der Trächtigkeit geringe Mengen Tributyltin im Trinkwasser verabreicht. Ihre Nachkommen (erste Generation) waren im Mutterleib exponiert, die Enkel (zweite Generation) waren als sich entwickelnde Keimzellen in diesen Nachkommen exponiert, und die Urenkel (dritte Generation) waren nie direkt ausgesetzt. Als junge erwachsene Nachkommen von Standardfutter auf fettreichere Kost umgestellt wurden, nahmen männliche Tiere mit Tributyltin-belasteten Vorfahren mehr Körperfett und Gewicht zu als ungeexponierte Kontrollen. Weibchen zeigten dagegen kaum oder keine Veränderung. Diese geschlechtsspezifische Neigung der Männchen zur diätinduzierten Fettleibigkeit stimmt mit früheren Arbeiten derselben Gruppe überein.
Genomfaltung als verstecktes Gedächtnis
Um zu verstehen, wie dieses Merkmal ohne DNA-Mutationen vererbt werden kann, untersuchten die Forschenden primordiale Keimzellen aus Embryonen der ersten drei Generationen. Dabei handelt es sich um die unreifen Zellen, aus denen später Spermien und Eizellen entstehen. Mit einer Technik, die abbildet, welche DNA-Abschnitte im dreidimensionalen Raum miteinander in Kontakt stehen, suchten sie nach langlebigen Veränderungen in der Chromosomenfaltung. Insgesamt war das Kontaktmuster recht stabil. In männlichen Keimzellen stach jedoch eine kleine Region auf Chromosom 19 hervor: Ein Cluster neuer, verstärkter Kontakte tauchte auf und blieb von den direkt exponierten Embryonen über zwei nicht direkt exponierte Generationen bestehen. Diese Region enthält das Ide-Gen, das das Insulin-abbauende Enzym kodiert, ein zentrales Protein, das normalerweise hilft, Insulin aus dem Blutkreislauf zu entfernen.
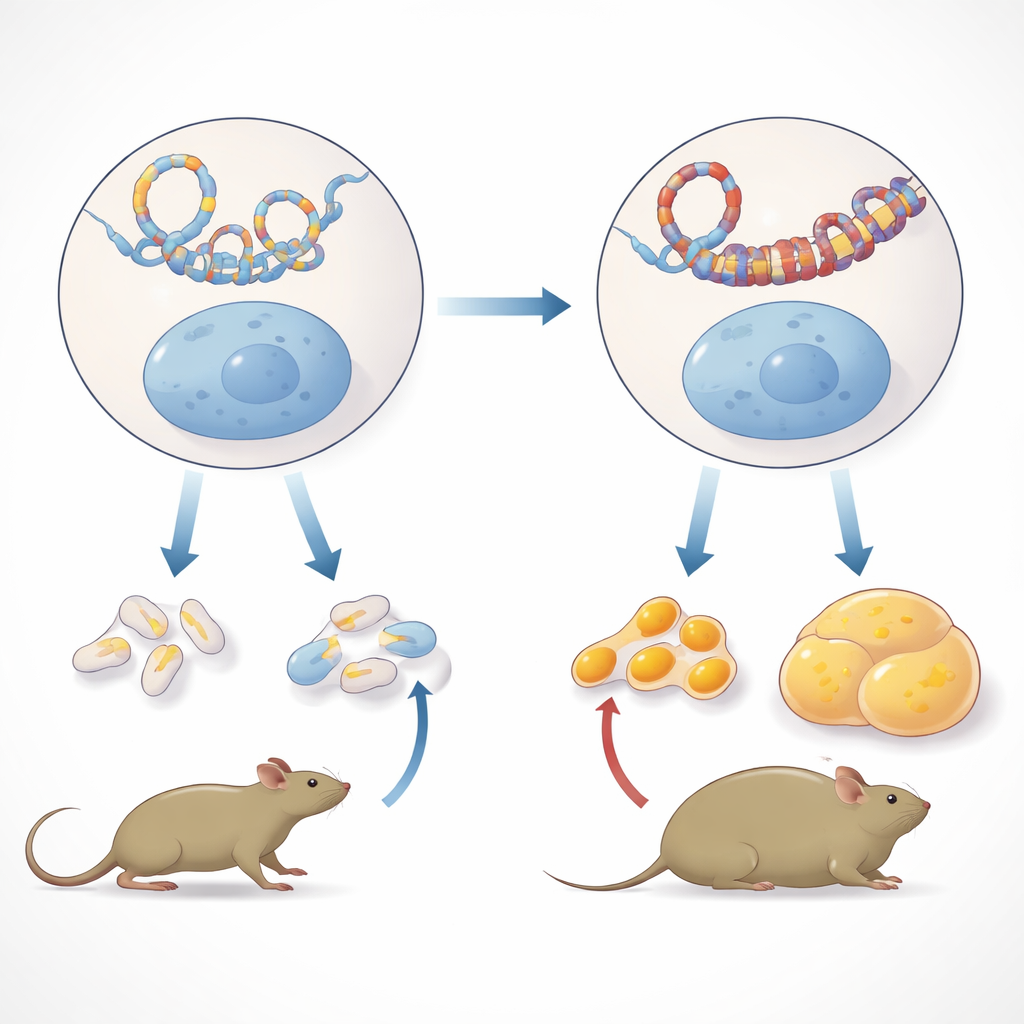
Ein einzelnes Gen im Zentrum der Stoffwechselverschiebung
Das Team fragte dann, ob diese veränderten DNA-Kontakte Folgen in gewöhnlichen Körpergeweben haben. In den Lebern erwachsener Urenkel der exponierten Mäuse beobachteten sie eine stärkere Bindung eines genomorganisierenden Proteins namens CTCF an mehreren Stellen innerhalb der Ide-Region, was mit der Bildung einer neuen Chromatinschleife vereinbar ist. Gleichzeitig sank die Ide-Aktivität in männlichen Lebern, während benachbarte Gene wie Hhex und Kif11 aktiver wurden. Dieses Muster trat nicht in Lebern von Weibchen oder in anderen männlichen Geweben wie Muskel, Fettpolstern, Gehirn oder Milz auf, was seine gewebespezifische und geschlechtsspezifische Natur unterstreicht. Wichtig ist, dass die Autorinnen und Autoren eine einfache strukturelle Duplikation dieses Chromosomenabschnitts als Erklärung ausschlossen: Die Kopienzahl der Ide-Region unterschied sich nicht zwischen exponierten und Kontrolllinien.
Von verändertem Insulinabbau zur Fettleibigkeit
Weil das Insulin-abbauende Enzym beim Entfernen von Insulin aus dem Kreislauf hilft, sollte eine reduzierte Ide-Aktivität zu mehr Insulin im Blut führen. Genau das beobachteten die Forschenden. Schon vor der fettreichen Diät hatten männliche Nachkommen tributyltin-exponierter Mütter erhöhte Insulinwerte und höhere Werte in einem Standardindex für Insulinresistenz bei normalem Nüchternglukosewert. Nach Wochen auf der reicheren Diät entwickelten sie sowohl hohen Blutzucker als auch erhöhtes Insulin, zusammen mit größeren Fettdepots und erhöhtem Leptin, einem Hormon, das mit Körperfett verbunden ist. Die Werte des C-Peptids, das die Insulinproduktion widerspiegelt, stiegen bei exponierten und Kontrolltieren ähnlich an. Der entscheidende Unterschied war das Verhältnis von C-Peptid zu Insulin, das auf eine beeinträchtigte Insulinabbaurate statt auf vermehrte Sekretion hindeutete — konsistent mit dem beobachteten Rückgang von hepatischem Ide.
Was das für Vererbung und Gesundheit bedeutet
In der Summe skizzieren die Befunde eine Kette von Ereignissen: die Ahnenexposition gegenüber einer obesogenen Chemikalie verändert subtil die Art und Weise, wie eine bestimmte Genomregion in männlichen Keimzellen gefaltet ist; diese neue 3D-Struktur wird in den Lebern männlicher Nachkommen wiederhergestellt und drosselt ein einzelnes Insulin-abbauendes Gen; dadurch haben diese Tiere chronisch höhere Insulinspiegel und sind anfälliger, bei einer fettreichen Ernährung Fett anzulagern und Blutzuckerprobleme zu entwickeln. Für eine nicht-fachliche Leserschaft lautet die Kernaussage, dass Umwelteinflüsse der Vorfahren eine physische „Erinnerung" in der Verpackung der DNA hinterlassen können — nicht durch Änderung des genetischen Codes, sondern durch Änderung seiner Form. Diese Erinnerung kann still und leise beeinflussen, wie spätere Generationen auf moderne Ernährungsweisen reagieren, und unterstreicht die Bedeutung, schädliche Expositionen lange vor dem Auftreten von Gesundheitsproblemen zu begrenzen.
Zitation: Chang, R.C., Egusquiza, R.J., Amato, A.A. et al. Heritable changes in chromatin contacts associated with transgenerational susceptibility to diet-induced insulin dysregulation and obesity. Nat Commun 17, 2662 (2026). https://doi.org/10.1038/s41467-026-69214-5
Schlüsselwörter: transgenerationale Epigenetik, Obesogene, Insulinresistenz, Chromatinstruktur, Umweltbelastung