Clear Sky Science · de
Ingenieurarbeit an einem Cytochrom‑P450‑Enzym als Peroxygenase für selektive Hydroxylierung von Steroiden
Medikamente aus schwer zu modifizierenden Molekülen herstellen
Steroidhormone — von entzündungshemmenden Tabletten bis zu Hormontherapien — gehören zu den weltweit am häufigsten eingesetzten Medikamenten. Doch diese Moleküle gezielt zu verfeinern, indem man genau an einer Stelle ein Sauerstoffatom einführt, ist mit herkömmlicher Chemie notorisch schwierig. Diese Studie zeigt, wie Forscher ein natürliches Enzym so umgestaltet haben, dass es Steroidmoleküle präzise mit einfachem Wasserstoffperoxid „polieren“ kann, was potenziell grünere und günstigere Wege zu wichtigen Arzneistoffen eröffnet.
Warum Steroide so schwer anzupassen sind
Steroide bestehen aus einem kompakten Stapel von Kohlenstoffringen mit vielen nahezu identischen C–H‑Bindungen. Konventionelle chemische Methoden tun sich schwer, genau eine dieser Bindungen anzusprechen, ohne andere zu erwischen; oft werden dafür aggressive Reagenzien, hohe Temperaturen und mehrere Schutz‑/Entschutz‑Schritte benötigt, die Abfall erzeugen. Kleine Änderungen — etwa das Einführen einer Hydroxylgruppe (–OH) an einer bestimmten Position — können die Wirkungsweise eines Steroids im Körper drastisch verändern. Enzyme der Cytochrom‑P450‑Familie sind in der Natur Spezialisten für diese präzise Aktivierung von C–H‑Bindungen. In ihrer natürlichen Form benötigen sie jedoch meist teure Hilfsmoleküle und Sauerstoff‑Handhabungsmaschinen, was ihren direkten Einsatz in der Produktion einschränkt.
Ein vielversprechendes Enzym als Ausgangspunkt finden
Mithilfe von Genome‑Mining identifizierten die Forschenden ein selbsterhaltendes P450‑Enzym namens P450stri aus einem Bodenbakterium. Im Gegensatz zu dem klassischen Arbeitspferd P450BM3, das bevorzugt kurze Fettsäuren verarbeitet, akzeptiert P450stri von Natur aus sperrige Steroidmoleküle wie Testosteron. Unter seinen nativen Bedingungen, angetrieben durch den zellulären Cofaktor NADH, fügt P450stri Hydroxylgruppen an drei Positionen des Testosterons ein und ergibt ein Gemisch von Produkten. Diese eingebaute Fähigkeit zur Steroiderkennung machte P450stri zu einem attraktiven „Startgerüst“ für die Entwicklung eines selektiveren, industrietauglichen Katalysators.
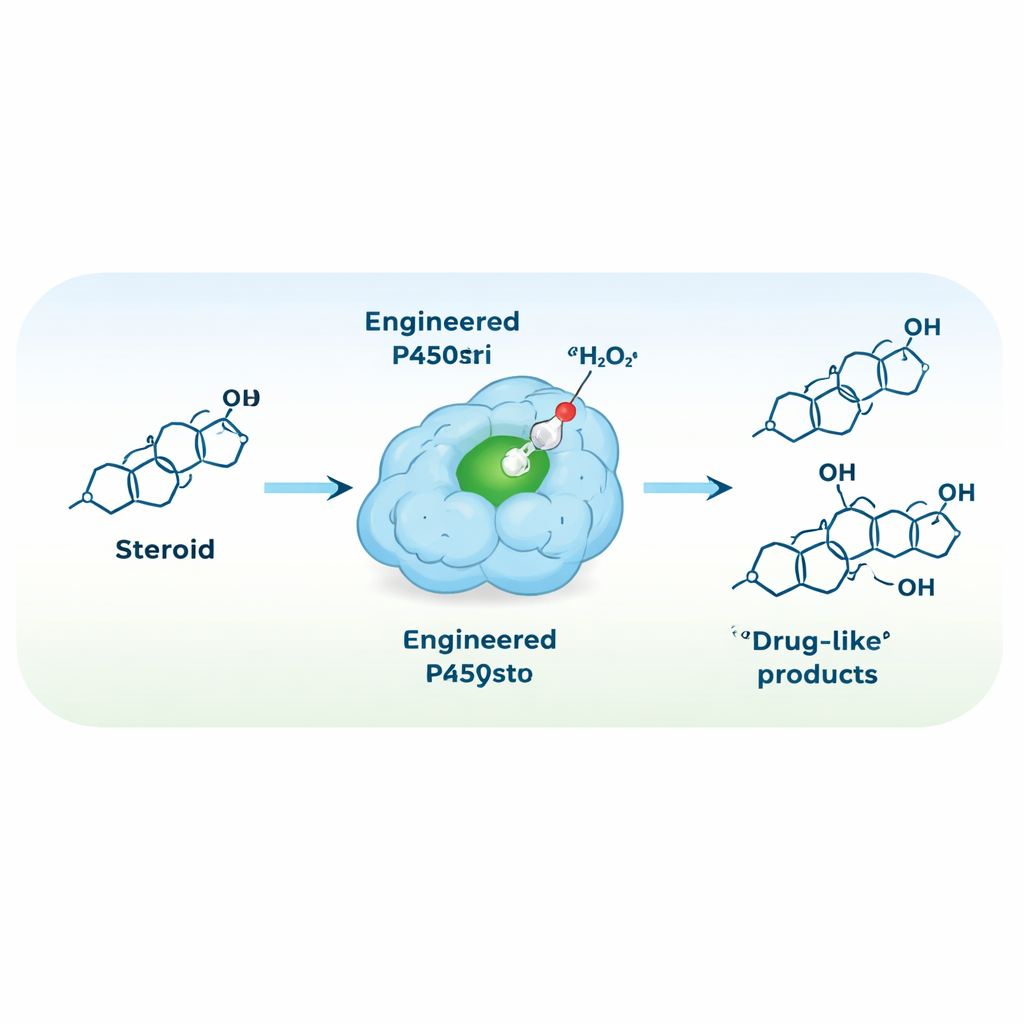
Das Enzym umbauen, damit es mit Wasserstoffperoxid läuft
Um die Reaktionsbedingungen zu vereinfachen, hatten die Autoren das Ziel, P450stri in eine Peroxygenase umzuwandeln — ein Enzym, das Wasserstoffperoxid direkt als Oxidationsmittel nutzt und so den Bedarf an teuren Cofaktoren und Zusatzproteinen eliminiert. Eine einzige strategische Mutation, bei der ein sperriges Phenylalanin direkt über dem Hämzentrum durch ein kleineres Alanin ersetzt wurde, erzeugte eine Variante namens M1. Diese Änderung schuf Platz um das reaktive Eisenzentrum und machte das Enzym überraschenderweise sowohl toleranter gegenüber hohen H2O2‑Konzentrationen als auch deutlich selektiver. Im neuen, peroxidgetriebenen Modus wandelte M1 Testosteron größtenteils in ein einzelnes Produkt um, hydroxyliert an der 15β‑Position, mit etwa 94 % Selektivität — gegenüber 35 % beim ursprünglichen Enzym.
Ein „Rundkolben“-Modell für klügeres Enzymdesign
Um die Leistung weiter zu steigern, führten die Autor:innen ein Konzept ein, das sie das „Rundkolben“-Modell nennen. Sie betrachten das aktive Zentrum, in dem die Chemie stattfindet, als die bauchige Grundform des Kolbens und die engen Zugangstunnel als Hals und Verschluss. Der Bauch bestimmt, welche Position am Steroid modifiziert wird, während der Hals kontrolliert, wie leicht das Steroid und das Wasserstoffperoxid das reaktive Zentrum erreichen. Geleitet von Computersimulationen und Tunnel‑Mapping‑Software passten sie systematisch eine kleine Gruppe von Aminosäuren an, die diese Tunnel auskleiden, und veränderten deren Größe und Hydrophobizität. Diese zweidimensionale Strategie ergab eine herausragende Variante, M4, die die hohe 15β‑Selektivität beibehielt, während sie die Reaktionsgeschwindigkeit deutlich erhöhte und H2O2‑Konzentrationen von bis zu mehreren hundert Millimolar tolerierte.
Vom Labortisch zu skalierbaren Steroid‑Upgrades
Das entwickelte Enzym M4 wurde anschließend in größerem Maßstab mit Testosteron und einem verwandten Steroid getestet, das in leistungssteigernden Kontexten verwendet wird. In einfachen wässrigen Mischungen bei Raumtemperatur, nur angetrieben durch Wasserstoffperoxid, wandelte M4 über 90 % des Ausgangsmaterials um und lieferte isolierte 15β‑hydroxylierte Produkte in Ausbeuten von rund 75–80 %. Diese Bedingungen sind deutlich milder und sauberer als typische chemische Verfahren. Schließlich zeigten die Forschenden, dass sich die Schlüsselmutsationen in mehrere verwandte P450‑Enzyme desselben evolutionären „Zweigs“ übertragen lassen, wodurch sich diese ebenfalls zuverlässig in ähnlich selektive und effiziente Peroxygenasen verwandeln ließen — ein Beleg für die Allgemeingültigkeit ihrer Gestaltungsprinzipien.
Was das für zukünftige Medikamente bedeutet
Für Nicht‑Spezialisten läuft es darauf hinaus: Die Forscher haben einem natürlichen Enzym beigebracht, wie eine hochpräzise, peroxidbetriebene „Mikrofabrik“ zu arbeiten, die Steroidmedikamente modifiziert. Durch die Kombination eines einfachen Konzeptmodells mit gezielten Mutationen schufen sie ein Enzym, das eine OH‑Gruppe genau am richtigen Ort unter schonenden und skalierbaren Bedingungen einführt und diese Strategie anschließend auf verwandte Proteine übertrug. Dieser Ansatz könnte die Herstellung bestehender Steroide vereinfachen, Zugänge zu neuen Arzneistoffkandidaten eröffnen und als Blaupause für das Engineering anderer Enzyme dienen, die hartnäckige C–H‑Bindungen in komplexen Molekülen sauber aktivieren.
Zitation: Tang, T., Wang, R. & Chen, Y. Engineering a cytochrome P450 enzyme as a peroxygenase for selective hydroxylation of steroids. Nat Commun 17, 1996 (2026). https://doi.org/10.1038/s41467-026-69211-8
Schlüsselwörter: Steroid‑Biokatalyse, Cytochrom‑P450‑Engineering, Peroxygenase, Wasserstoffperoxid‑Katalyse, selektive Hydroxylierung