Clear Sky Science · de
Strukturelle Einzelzellbiologie mit intrazellulärer Elektronenkristallographie
Die Form des Lebens sehen, eine Zelle nach der anderen
Proteine sind die winzigen Maschinen, die jede Zelle am Leben halten, doch um wirklich zu verstehen, wie sie funktionieren, müssen Forschende ihre dreidimensionalen Formen in feinen Details sehen. Traditionell bedeutete das, große Mengen des Proteins zu reinigen und außerhalb der Zelle große, fragile Kristalle zu züchten – oft ein langsamer und fehleranfälliger Prozess. Diese Studie stellt einen neuen Weg vor, Proteinstrukturen direkt aus einem einzelnen Kristall innerhalb einer einzigen Zelle abzulesen, wobei Elektronen statt Röntgenstrahlen verwendet werden. Sie weist in eine Zukunft, in der hochauflösende Strukturbiologie in normalen Laboren möglich wird und sogar auf der Ebene einzelner Zellen.
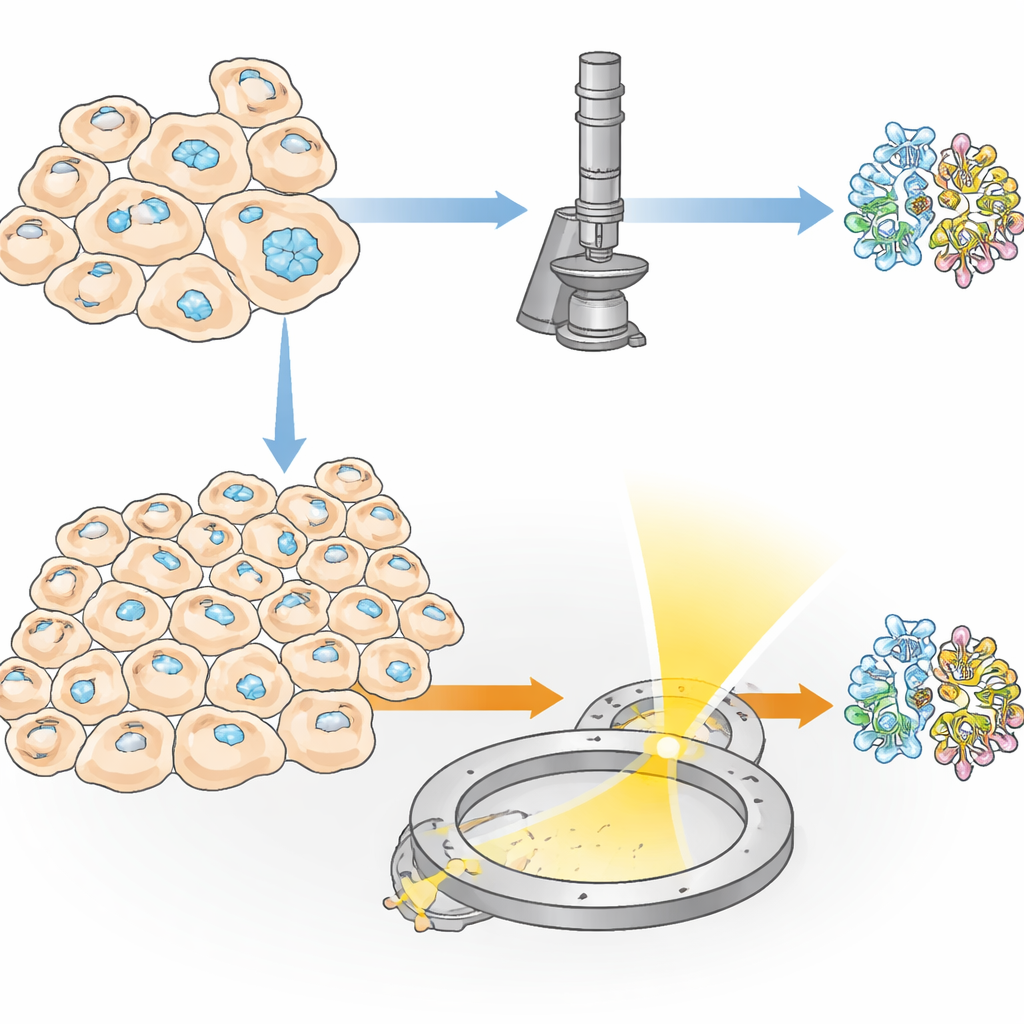
Kristalle versteckt in lebenden Zellen
Einige Proteine sammeln sich natürlicherweise zu winzigen Kristallen innerhalb lebender Zellen und erfüllen Funktionen wie Speicherung, Schutz oder das Reagieren auf Stress. Forschende können Zellen auch dazu bringen, solche Kristalle zu produzieren, indem sie sie dazu bringen, große Mengen eines ausgewählten Proteins herzustellen. Diese „in‑cell“-Kristallisation hat zwei große Vorteile: Das Protein verlässt niemals seine naturnahe Umgebung, und empfindliche Merkmale – etwa Zuckerketten oder kleine gebundene Moleküle – können erhalten bleiben, was in konventionellen Reagenzglas‑Kristallisationen oft scheitert. Ein großes Hindernis blieb jedoch: In vielen Experimenten bilden nur sehr wenige Zellen überhaupt Kristalle, sodass traditionelle Röntgenmethoden zehntausende Kristalle und damit enorm viele Zellen benötigen.
Ein neuer Weg: Elektronen statt Röntgenstrahlen
Die Autorinnen und Autoren stellen eine Methode vor, die sie IncelluloED nennen und die in‑cell‑Kristallisation mit dreidimensionaler Elektronenbeugung verbindet. Elektronen wechselwirken deutlich stärker mit Materie als Röntgenstrahlen, sodass nützliche Daten aus Kristallen gewonnen werden können, die sowohl kleiner als auch seltener sind. Das Team wählte ein Pilzprotein namens HEX‑1, das normalerweise hexagonale Kristalle bildet, die bei Stress winzige Poren zwischen Pilzzellen verschließen. Indem sie dieses Protein in Insektenzellen produzierten, erzeugten sie regelmäßige mikroskopische Kristalle, die als Testfall für die neue Pipeline dienten.
Aus einem Kristall eine detaillierte Karte gewinnen
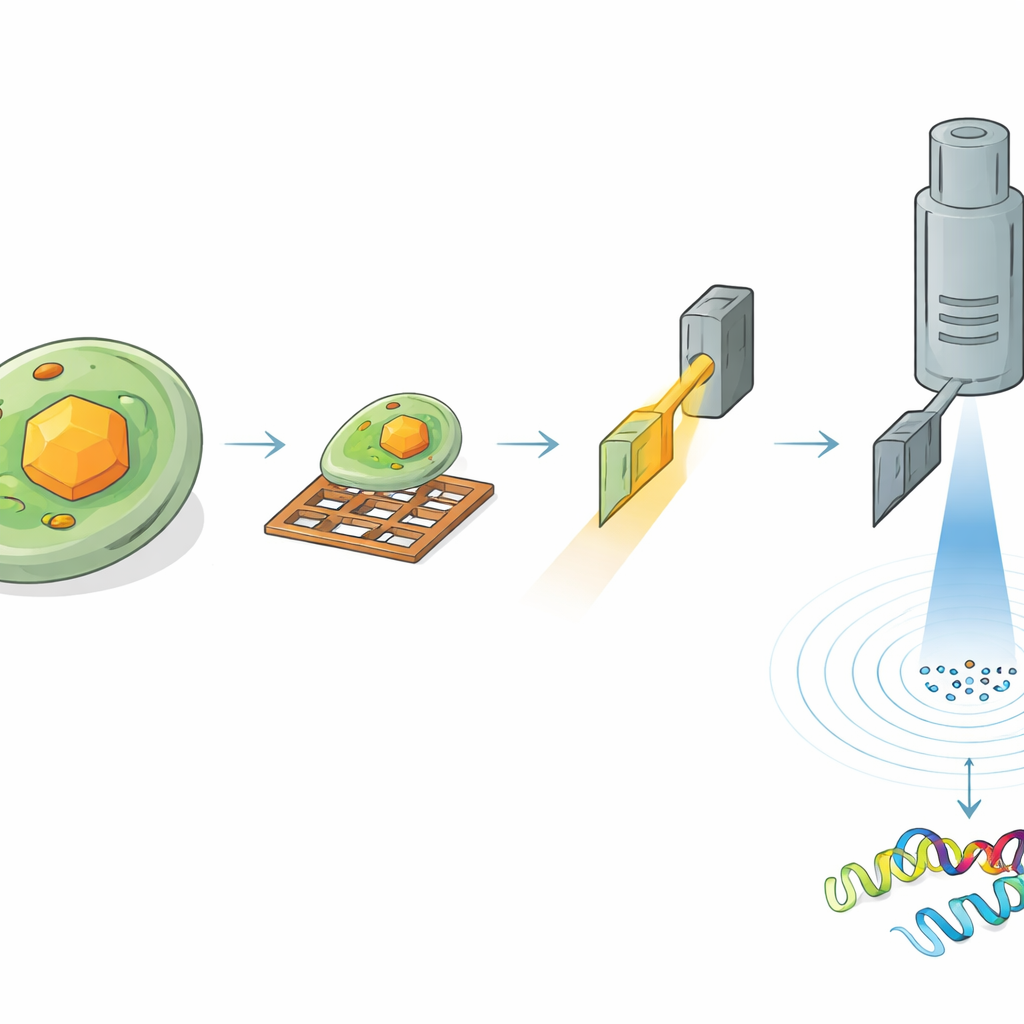
Um die Struktur von HEX‑1 innerhalb einer Zelle zu lesen, mussten die Forschenden die richtige Stelle im Probenmaterial finden und sorgfältig ausdünnen. Zuerst froren sie die kristallführenden Zellen auf winzigen Metallgittern ein und beschichteten die Oberfläche mit einer dünnen Platinschicht. Mithilfe kryogener Lichtmikroskopie scannten sie große Bereiche des Gitters, um Zellen mit Kristallen zu lokalisieren, und bestimmten die dreidimensionalen Positionen der Kristalle unter der Oberfläche. Anschließend brachten sie dieselbe Probe in ein spezialisiertes Instrument, das ein rasterelektronenmikroskop mit einem fokussierten Ionenstrahl kombiniert. Anhand der vorherigen Lichtbilder frästen sie das umgebende Material weg, um eine ultradünne Scheibe oder Lamelle durch einen ausgewählten Kristall zu schneiden, nur wenige hundert Nanometer dick – ideal, damit Elektronen hindurchtreten können.
Elektronen zeigen atomare Details aus mikroskopischen Volumina
Die vorbereiteten Lamellen wurden dann in ein hochauflösendes Elektronenmikroskop bei kryogenen Temperaturen überführt. Während die Kristallscheibe langsam im Mikroskop gedreht wurde, passierte ein fein kontrollierter Elektronenstrahl diese und erzeugte eine Reihe von Beugungsmustern – zarte Punktanordnungen, die die Positionen der Atome kodieren. Aus einem Kristallvolumen von etwa 1,6 Kubikmikrometern rekonstruierte das Team die vollständige 3D‑Struktur von HEX‑1 mit 1,9 Ångström Auflösung, scharf genug, um die meisten Seitenketten des Proteins zu modellieren. Selbst kleinere Volumina von etwa 0,8 Kubikmikrometern lieferten eine nahezu identische Struktur bei nur leicht geringerer Auflösung. Wichtig ist, dass die resultierenden Modelle eng mit denen übereinstimmten, die mithilfe konventioneller serieller Röntgenmethoden gewonnen wurden, die mehr als 60.000 Kristalle und ein Gesamt‑Kristallvolumen erforderten, das etwa sieben Millionen Mal größer war.
Wie das die Strukturbiologie verändert
Seiten‑an‑Seiten‑Vergleiche zeigten, dass die aus einem einzelnen in‑cell Elektronenbeugungs‑Kristall bestimmte Struktur im Wesentlichen dieselbe ist wie die aus der Mittelung von zehntausenden Röntgenkristallen. Unterschiede waren gering und beschränkten sich überwiegend auf flexible Schleifen, in denen natürliche Bewegungen zu erwarten sind. Die Forschenden zeigten außerdem, dass die verwendeten Elektronendosen niedrig genug waren, um schwere Strahlenschäden zu vermeiden, und dass jeder verarbeitete Kristall hochwertige Daten lieferte. Obwohl die Herstellung der dünnen Lamellen weiterhin Können und Zeit erfordert, sind die benötigten Instrumente – kryogene Lichtmikroskope, fokussierte Ionenstrahl‑Systeme und kryo‑Elektronenmikroskope – mittlerweile in vielen Forschungseinrichtungen weit verbreitet.
Von vielen Zellen zum Einzelzell‑Strukturlabor
Diese Arbeit zeigt, dass es nun möglich ist, eine atomare Proteinstruktur aus nur einem Kristall in einer einzigen Zelle zu bestimmen, ohne das Protein jemals zu reinigen. IncelluloED könnte besonders leistungsfähig sein, wenn nur wenige Zellen Kristalle bilden oder wenn Proteine schwer zu isolieren sind, ohne wichtige Partner oder chemische Gruppen zu verlieren. Wenn der Workflow stärker automatisiert und auf andere Proteine ausgeweitet wird, könnte er Forschenden erlauben, zu untersuchen, wie Strukturen von Zelle zu Zelle variieren, krankheitsbedingte Veränderungen in ihrem nativen Kontext zu studieren und sogar die Wirkstoffsuche direkt in lebenden Zellen zu unterstützen. Effektiv rückt die Studie die Vision eines „Einzelzell‑Strukturlabors“ deutlich näher an die Realität.
Zitation: Bílá, Š., Pinkas, D., Khakurel, K. et al. Single-cell structural biology with intracellular electron crystallography. Nat Commun 17, 2109 (2026). https://doi.org/10.1038/s41467-026-69205-6
Schlüsselwörter: Elektronenbeugung, in cellulo Kristallographie, Einzelzell‑Strukturbiologie, Proteinstruktur, cryo‑EM