Clear Sky Science · de
14-3-3ζ interagiert mit der DNA-Bindedomäne von FOXO3a und löst DNA kompetitiv durch Doppel-Motiv-Verankerung ab
Wie Krebszellen ihren eigenen Selbstzerstörungsschalter ausschalten
Unsere Zellen verfügen über eingebaute Sicherheitsmechanismen, die den Zelltod auslösen können, wenn Zellen zu beschädigt oder gefährlich werden. Eines dieser Systeme wird von einem Protein namens FOXO3a gesteuert, das Gene aktiviert, die schadhafte Zellen zur Selbsttötung bringen. Viele Krebsarten finden jedoch Wege, FOXO3a stummzuschalten und weiter zu wachsen. Diese Studie geht den molekularen Details nach, wie ein anderes Protein, 14-3-3ζ, Krebszellen dabei hilft, FOXO3a von der DNA zu lösen und diesen Selbstzerstörungsschalter zu deaktivieren.
Das Wächterprotein, das sich gegen Krebs behauptet
FOXO3a wirkt wie ein Sicherheitsinspektor der Zelle. Es bindet an spezifische Stellen auf der DNA und aktiviert Gene, die das Wachstum bremsen oder den programmierten Zelltod (Apoptose) auslösen, wenn etwas schiefläuft. In gesunden Zellen hilft dies, Tumoren zu verhindern. In vielen Krebsarten jedoch ist ein wachstumsfördernder Signalweg, der von mutierten Ras-Proteinen gesteuert wird, dauerhaft aktiviert. Dieser Weg schaltet eine Kinas e namens AKT ein, die FOXO3a an mehreren Stellen mit Phosphatgruppen versieht. Diese Markierungen schaffen Andockstellen für 14-3-3ζ, ein dimeres „Adapter“-Protein, das phosphorylierte Motive auf vielen Zielproteinen erkennt. Wenn 14-3-3ζ an FOXO3a bindet, versagen nach und nach die inneren Bremsen der Zelle.
Warum bloße Bindungsstärke den Effekt nicht erklären konnte
Frühere Untersuchungen an einem verwandten Protein, FOXO4, legten nahe, dass 14-3-3-Proteine FOXO-Faktoren einfach deshalb von der DNA lösen, weil sie stärker binden. FOXO3a bevorzugt jedoch seine natürlichen DNA-Ziele stärker, als das frühere Modell annahm. In dieser Studie erzeugten die Forschenden eine Version von FOXO3a, die die DNA-Bindedomäne und zwei wichtige Phosphorylierungsstellen enthält. Sie maßen, wie fest dieses Protein entweder an DNA oder an 14-3-3ζ bindet, und fanden nur moderate Unterschiede: 14-3-3ζ war nur etwa doppelt so starker Partner wie die DNA. Doch in Gemisch-Experimenten, die verfolgen, wie Moleküle durch eine Chromatographiesäule wandern, konnte 14-3-3ζ nahezu vollständige Freisetzung der DNA von FOXO3a bewirken, als wäre es etwa 100-mal wettbewerbsfähiger als erwartet. Diese Diskrepanz deutete auf einen zusätzlichen Mechanismus hin.
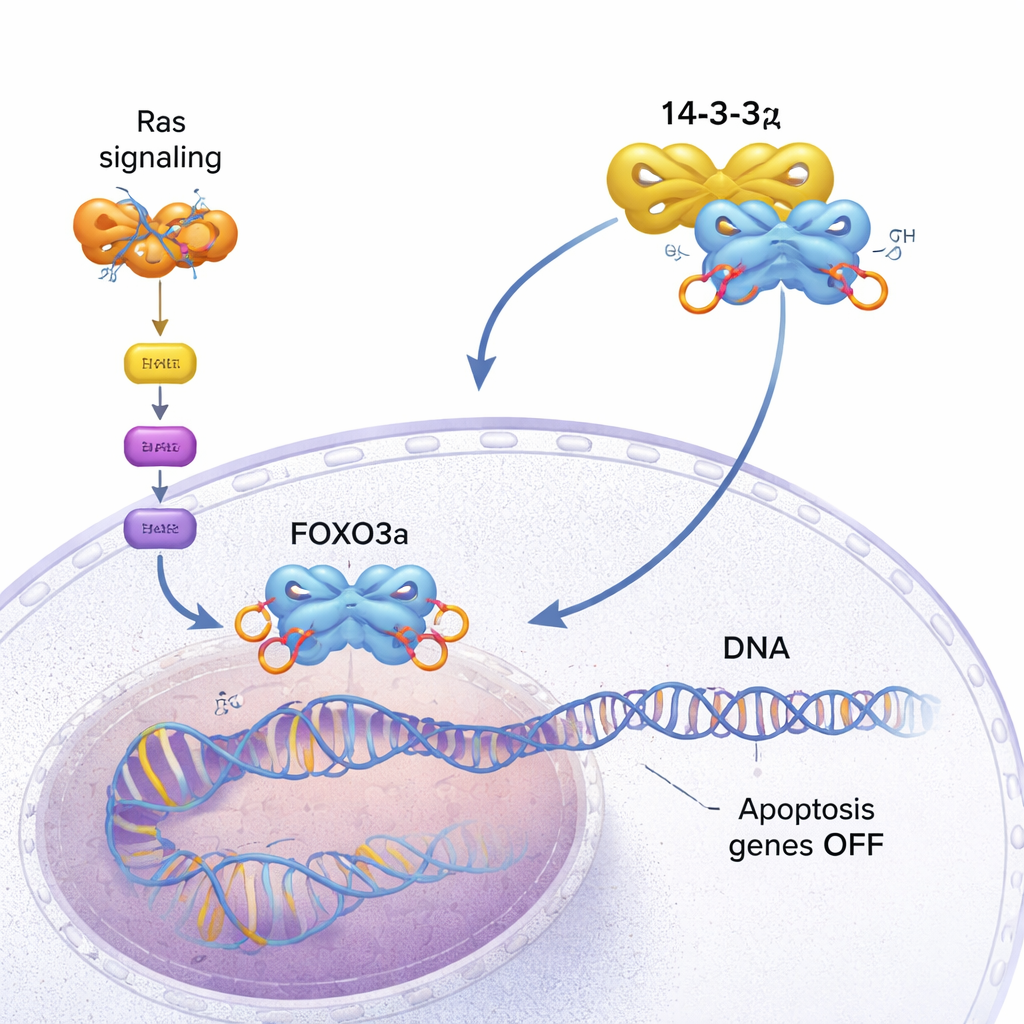
Ein Dreipunktgriff, der die DNA verdrängt
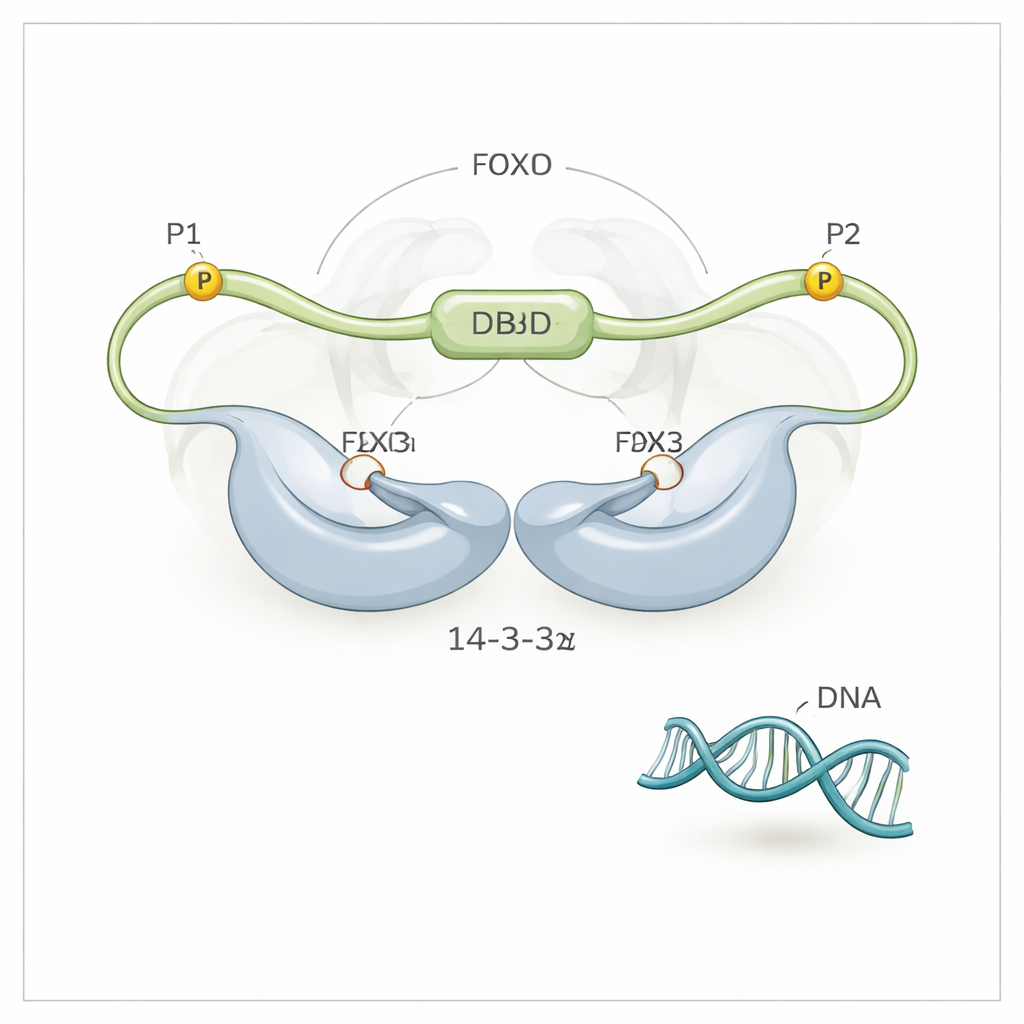
Mithilfe hochauflösender NMR-Spektroskopie entdeckte das Team, dass 14-3-3ζ mehr tut, als FOXO3a nur an seinen zwei phosphorylierten Motiven (genannt P1 und P2) zu packen. Es macht auch direkte, wenn auch schwächere Kontakte mit der DNA-Bindedomäne (DBD) von FOXO3a selbst — genau jener Oberfläche, die normalerweise die DNA umschließt. Das 14-3-3ζ-Protein bildet ein symmetrisches Dimer mit zwei Mulden. Jede Mulde klemmt eines der phosphorylierten Motive von FOXO3a ein und verankert FOXO3a so an zwei Punkten an 14-3-3ζ. Weil eines dieser Motive (P2) sehr nahe entlang der Kette an der DNA-Bindedomäne liegt, hält diese „Doppel-Motiv-Verankerung“ 14-3-3ζ effektiv direkt neben der DBD und erhöht stark die Wahrscheinlichkeit, dass die DBD die Oberfläche von 14-3-3ζ anstelle der DNA berührt und bindet. Die Forschenden konnten sogar beobachten, dass die DBD zwischen den beiden Seiten des 14-3-3ζ-Dimers hin- und herschwenkt und die meiste Zeit vor der DNA abgeschirmt verbringt.
Welche Phosphatmarken am wichtigsten sind
Um die Rollen der beiden phosphorylierten Stellen auseinanderzuhalten, erzeugte das Team FOXO3a-Varianten, bei denen jeweils nur eine Stelle gleichzeitig phosphoryliert werden konnte. War nur die P2-Stelle in der Nähe der DBD aktiv, konnte 14-3-3ζ die DNA teilweise, aber nicht vollständig verdrängen. War nur die weiter entfernte P1-Stelle aktiv, konnte 14-3-3ζ an FOXO3a binden, beeinflusste dessen DNA-Haltung jedoch kaum. Die vollständige Freisetzung der DNA erforderte beide Stellen im Zusammenspiel: P1 liefert einen hochaffinen initialen Andockpunkt für 14-3-3ζ, und P2 positioniert das Dimer nahe genug an der DBD, dass die lokale Konzentration von 14-3-3ζ an dieser Stelle effektiv enorm wird. Diese mehrstufige Verankerung verstärkt eine bescheidene Bindungspräferenz zu einer kraftvollen Fähigkeit, DNA zu vertreiben.
Vom molekularen Tauziehen zu neuen Medikamentenideen
Für Nicht-Spezialisten lautet die zentrale Erkenntnis, dass Krebszellen eine clevere molekulare Geometrie ausnutzen und nicht nur rohe Bindungsstärke, um ein wichtiges Tumorsuppressorprotein stummzuschalten. 14-3-3ζ nutzt zwei kleine, phosphatabhängige Andockstellen auf FOXO3a als Ankerpunkte und reicht dann über, um die DNA-fassende Oberfläche der Kern-Domäne von FOXO3a zu bedecken und so deren Aktivierung von Zelltodgenen zu verhindern. Da die gleichen FOXO- und 14-3-3-Familien in vielen Geweben weit verbreitet sind, ist diese Doppel-Verankerungsstrategie wahrscheinlich auch in anderen Krebsarten üblich. Die Störung entweder der phosphatabhängigen Anker oder des schwächeren Kontakts zur DNA-Bindefläche von FOXO3a könnte dessen Fähigkeit, Selbstzerstörungsprogramme in Tumorzellen zu aktivieren, wiederherstellen und vielversprechende neue Ansatzpunkte für die Entwicklung von Krebsmedikamenten bieten.
Zitation: Enomoto, S., Kuwayama, T., Nakatsuka, S. et al. 14-3-3ζ interacts with DNA-binding domain of FOXO3a and competitively dissociates DNA by dual-motif tethering. Nat Commun 17, 1503 (2026). https://doi.org/10.1038/s41467-026-69203-8
Schlüsselwörter: FOXO3a, 14-3-3-Proteine, Apoptose, Ras–AKT-Signalgebung, Krebsmedikamente