Clear Sky Science · de
Molekulare Mechanismen von Flotillin-Komplexen bei der Organisation von Membran‑Mikroumgebungen
Verborgene Räume auf der Zelloberfläche
Jede Zelle in Ihrem Körper ist von einer dünnen Membran umgeben, die auf den ersten Blick einfach wirkt, tatsächlich aber in zahllose winzige „Nachbarschaften“ unterteilt ist. Diese Bereiche steuern, wie Signale empfangen werden, wie Nährstoffe eindringen und wie Abfall ausgeschleust wird. Die vorliegende Studie zeigt, wie ein Paar lange rätselhafter Proteine, die Flotilline genannt werden, miniature geschützte Räume auf der Innenseite der Membran aufbaut – Strukturen, die Prozesse so unterschiedliche wie Zellsignalübertragung, Transport von Fracht und sogar Krebsausbreitung beeinflussen können. 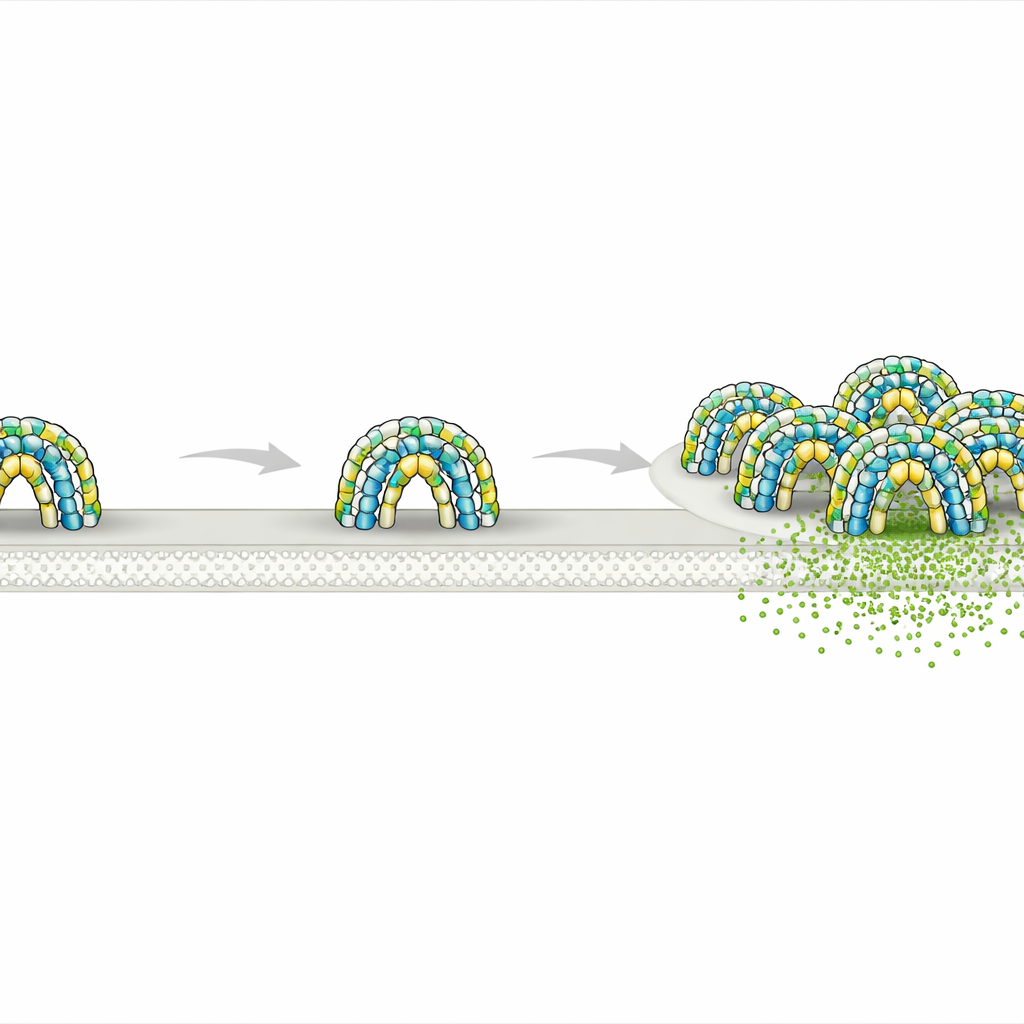
Ein genauerer Blick auf winzige Membran‑Nachbarschaften
Biologen wissen schon lange, dass Zellmembranen nicht einheitlich sind. Lipide und Proteine bilden stattdessen kleine Cluster, die wie temporäre Arbeitsstationen für spezifische Aufgaben fungieren, etwa Kommunikation oder Sortierung von Fracht. Flotillin‑1 und Flotillin‑2 markieren stets solche Bereiche, erscheinen als kleine helle Punkte auf der Zelloberfläche und beteiligen sich an der Endozytose – dem Vorgang, mit dem Zellen Material einziehen – sowie an Signalübertragung und Proteintransport. Unklar war jedoch, welche Gestalt Flotillin‑Strukturen tatsächlich annehmen und wie sie sich auf der Membran Territorien abstecken.
Kuppeln, die Kreise der Membran einfrieden
Mithilfe hochauflösender Kryo‑Elektronenmikroskopie an gereinigten menschlichen Proteinen entdeckten die Forscher, dass Flotillin‑1 und Flotillin‑2 einen bemerkenswert großen Komplex aus 44 Proteinexemplaren bilden, die abwechselnd angeordnet sind. Gemeinsam formen sie eine starre Kuppel auf der inneren Fläche der Membran. Die Basis dieser Kuppel besteht aus membranverankernden Segmenten, die reich an fettliebenden Aminosäuren und Lipidanhängen sind und teilweise in die Membran eindringen. Darüber bilden lange helikale Stiele eine dicht gepackte, fassähnliche Wand, und ein Dach aus ineinandergreifenden Proteinsegmenten verschließt die Struktur. Der Flotillinring an der Basis definiert einen kreisförmigen Membranbereich von etwa 30 Nanometern Durchmesser – er umfriedet also praktisch eine winzige Membranscheibe und den Raum direkt darüber.
Flexible Kuppeln in lebenden Zellen beobachtet
Um zu prüfen, ob diese Kuppeln in echten Zellen vorkommen, erzeugte das Team humane T‑Zellen, die mit fluoreszenzmarkiertem Flotillin‑1 und Flotillin‑2 versehen waren, und untersuchte sie kombiniert mittels Lichtmikroskopie und Kryo‑Elektronentomographie. Sie beobachteten hohle, kuppelförmige Strukturen an der Innenseite der Plasmamembran, die der in gereinigten Proben bestimmten Form sehr ähnlich waren. Viele Kuppeln erschienen leicht verzerrt oder teilweise geöffnet, und einige enthielten zusätzliche Dichten im Inneren, wahrscheinlich andere Proteine, die vorübergehend unter dem Dach eingeschlossen waren. In manchen Regionen gruppierten sich mehrere Kuppeln auf flachen oder gekrümmten Membranen, etwa an Endosomen und kleinen extrazellulären Vesikeln, was darauf hindeutet, dass Einzelkuppeln zu größeren Membranplattformen zusammenwachsen können. 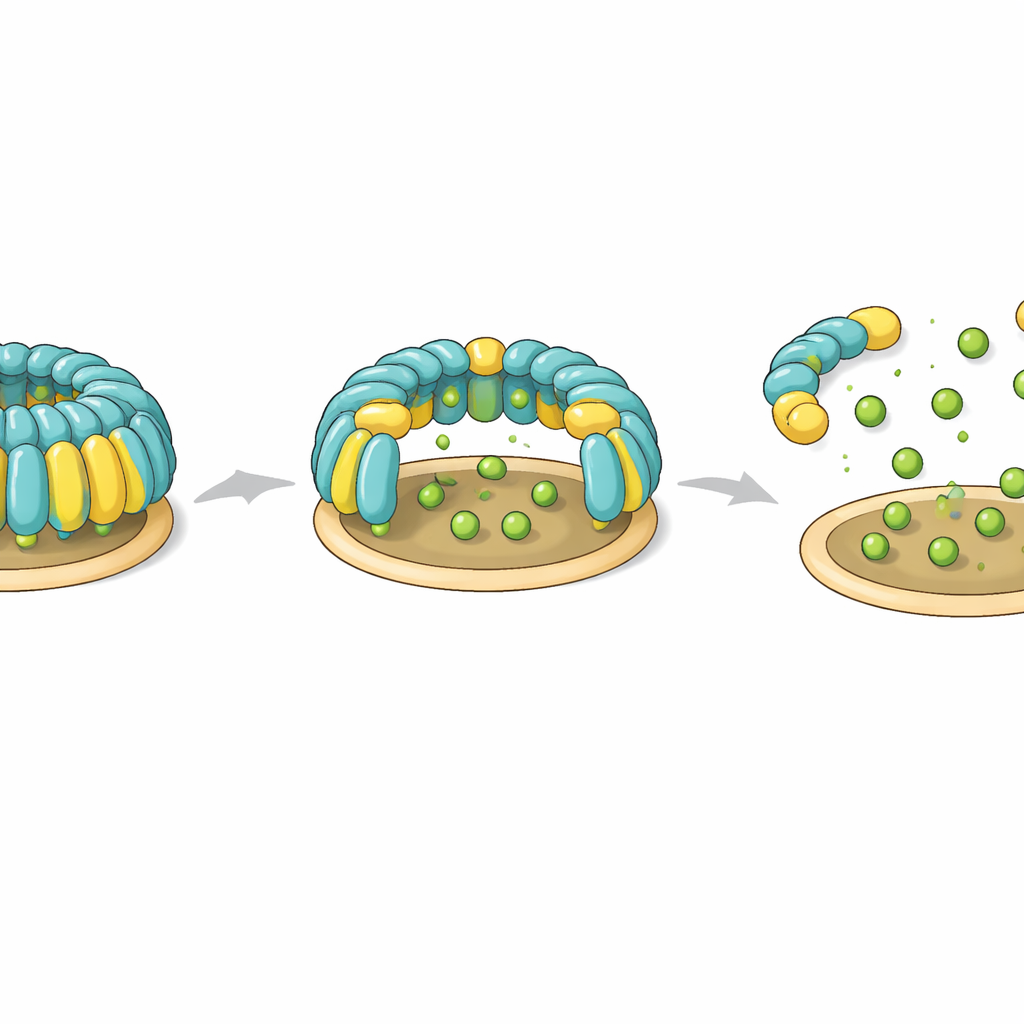
Ein molekularer Schalter zum Aufbau und Abbau von Kuppeln
Die Studie identifiziert außerdem einen möglichen Kontrollmechanismus, mit dem Zellen Flotillin‑Kuppeln aufbauen oder zerlegen könnten. Zwei spezifische Tyrosin‑Reste – je einer auf jedem Flotillin‑Protein – sitzen an scharnierähnlichen Positionen, die die membranverankernde Basis mit der helicalen Wand verbinden. Im intakten Komplex tragen diese Reste zur Bildung eines engen hydrophoben Kerns bei, der die Orientierung der Domänen verriegelt. Wenn die Forscher Mutationen einführten, die einen negativen Ladungszustand nachahmen (wie er bei Phosphorylierung dieser Tyrosine durch Enzyme entstehen würde), konnte die gesamte Kuppel nicht mehr zusammengebaut werden. Nicht geladene Mutationen ließen die Assemblierung intakt. Diese Beobachtungen deuten darauf hin, dass Phosphorylierung an diesen Scharnierpunkten als reversibler Schalter wirken könnte, der die Kuppel destabilisiert, sie öffnet oder während Prozessen wie flotillinabhängiger Endozytose auflöst.
Neuinterpretation, wie diese Domänen die Membran formen
Flotillin‑Cluster galten einst hauptsächlich als „Lipid‑Rafts“, reich an Cholesterin und verwandten Fetten. Überraschenderweise bevorzugten Flotilline in Experimenten mit großen, von Zellen abgezogenen Membranblasen die flüssigeren, nicht‑raftigen Regionen statt der starren, cholesterinreichen Bereiche. Lipidanalysen zeigten nur eine moderate Anreicherung eines bestimmten Moleküls, Sphingosin, innerhalb der Flotillin‑Komplexe, während andere mit Rafts assoziierte Lipide nicht konzentriert waren. Das deutet auf ein anderes Ordnungsprinzip hin: Statt nur Passagiere bereits existierender Lipid‑Rafts zu sein, agieren Flotillin‑Kuppeln selbst als strukturelle Behälter, die Memanstücke lateral segregieren und bestimmte Proteine und Lipide in ihrem eingezäunten Bereich einfangen.
Warum diese winzige Architektur wichtig ist
Anschaulich verhalten sich Flotillin‑Komplexe wie modulare Baldachine, die Zellen an ihrer Innenseite ausrollen können, um kleine kreisförmige Membranparzellen abzugrenzen. Jede Kuppel kann eine spezifische Mischung aus Partnerproteinen und Lipiden beherbergen und durch Clustering mit anderen größere Funktionszonen für Signalübertragung, Frachtsortierung oder Vesikelbildung schaffen. Da die Kuppeln flexibel sind und sich offenbar öffnen und schließen, und weil ihr Aufbau auf Phosphorylierung empfindlich reagiert, können Zellen diese Strukturen dynamisch an wechselnde Signale anpassen. Diese Arbeit rückt Flotilline damit von vagen „Raft‑Markern“ zu konkreten architektonischen Elementen, die die Membran in spezialisierte Mikroarbeitsbereiche formen helfen.
Zitation: Lu, MA., Qian, Y., Ma, L. et al. Molecular mechanisms of flotillin complexes in organizing membrane microdomains. Nat Commun 17, 2541 (2026). https://doi.org/10.1038/s41467-026-69197-3
Schlüsselwörter: flotillin, Membranmikroumgebungen, Cryo‑Elektronenmikroskopie, Endozytose, Lipid‑Rafts