Clear Sky Science · de
Das Überleben von Gewebe-ansässigen Makrophagen hängt von der mitochondrialen Funktion ab, die in chronischer Entzündung durch SerpinB2 reguliert wird
Warum die Immunzellen im Fett wichtig sind
Die meisten Menschen halten Körperfett für passiven Speicher, doch tatsächlich ist es ein lebendiges Gewebe voller Immunzellen, das Entzündungen und Blutzucker reguliert. Diese Studie zeigt, wie eine bestimmte Gruppe langlebiger Immunzellen im tiefen Bauchfett als Wächter gegen Typ‑2‑Diabetes wirkt – und wie chronische Entzündung bei Adipositas sie still und leise zerstört, indem sie ihre winzigen Kraftwerke, die Mitochondrien, schädigt.
Zwei Arten von Fettwächtern
Das viszerale Fettgewebe – Fett, das die inneren Organe umgibt – enthält zwei Haupttypen von Immunzellen, sogenannte Makrophagen. Ein Typ ist kurzlebig und wird ständig aus dem Blut nachgeliefert; diese „entzündlichen“ Makrophagen fördern tendenziell Schwellungen und Insulinresistenz. Der andere Typ sind langlebige, Gewebe-ansässige Makrophagen, die früh im Leben entstehen und normalerweise das Gewebe beruhigen, gesunde Fettspeicherung unterstützen und die Insulinsensitivität im ganzen Körper fördern. Durch Verfolgen dieser Zellen in Mäusen und den Vergleich der Genaktivität zeigten die Forschenden, dass Gewebe-ansässige Makrophagen reich an anti‑entzündlichen und insulinempfindlichmachenden Genen sind, während zugewanderte monocyten-abgeleitete Makrophagen Gene exprimieren, die die Blutzuckerregulation verschlechtern.
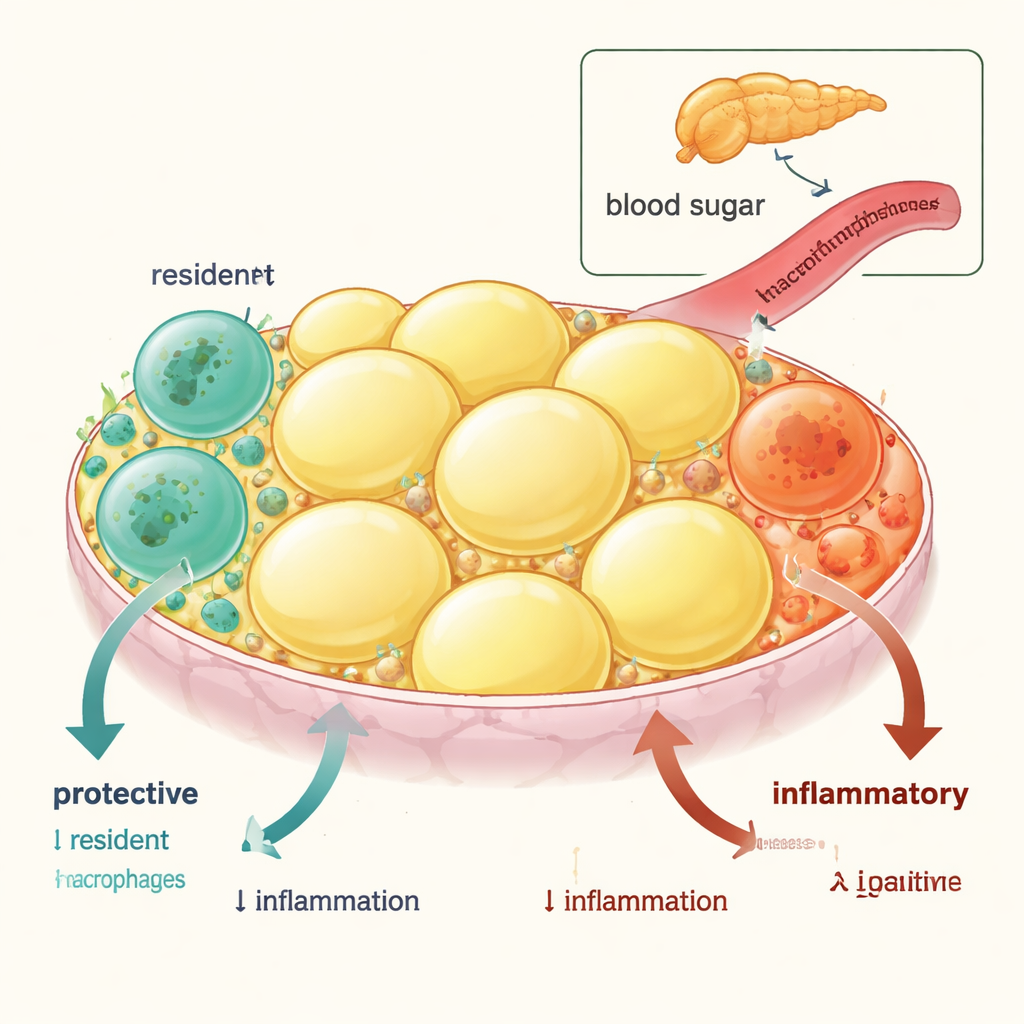
Wenn Entzündung die Guten tötet
Bei Adipositas verschiebt sich dieses schützende Gleichgewicht. Das Team fand heraus, dass sowohl bei adipösen Mäusen als auch bei adipösen oder diabetischen Menschen die Zahl der Gewebe-ansässigen Makrophagen im viszeralen Fett abnimmt, während entzündliche Makrophagen zunehmen. Sorgfältige Bildgebung und Zelltodmarker zeigten, warum: Gewebe-ansässige Makrophagen durchlaufen häufiger programmierte Zellsterben (Apoptose), während die entzündlichen Zellen das nicht tun. Bemerkenswerterweise erholte sich die residente Population bei adipösen Mäusen, die von einer fettreichen Diät genommen wurden, langsam durch lokale Proliferation, und die Stoffwechselgesundheit verbesserte sich – was zeigt, dass dieser Verlust durch den entzündlichen Zustand verursacht wird und reversibel ist.
Ein einzelnes Protein verbindet Mitochondrien mit Überleben
Ein entscheidender Hinweis war ein Protein namens SerpinB2, das vor allem für Funktionen bei der Blutgerinnung bekannt ist. Die Forschenden entdeckten, dass SerpinB2 in Gewebe-ansässigen Makrophagen sehr hoch exprimiert wird, jedoch viel geringer in entzündlichen. Bei adipösen Menschen und Mäusen reduzierten die residenten Makrophagen die SerpinB2‑Expression deutlich, und ein höherer Body‑Mass‑Index war mit weniger SerpinB2‑positiven Zellen assoziiert. Experimente in Zellen ohne SerpinB2 zeigten vermehrtes Austreten von Cytochrom c — einem Schlüsselmolekül — aus den Mitochondrien ins Zytoplasma, ein klassischer Auslöser der Apoptose. Diese SerpinB2‑defizienten Makrophagen hatten weniger antioxidative Abwehrmechanismen, mehr mitochondriale reaktive Sauerstoffspezies (ROS) und einen höheren Sauerstoffverbrauch, alles Anzeichen gestresster, überarbeiteter Mitochondrien, die Zellen in Richtung entzündliches Verhalten und Zelltod treiben.
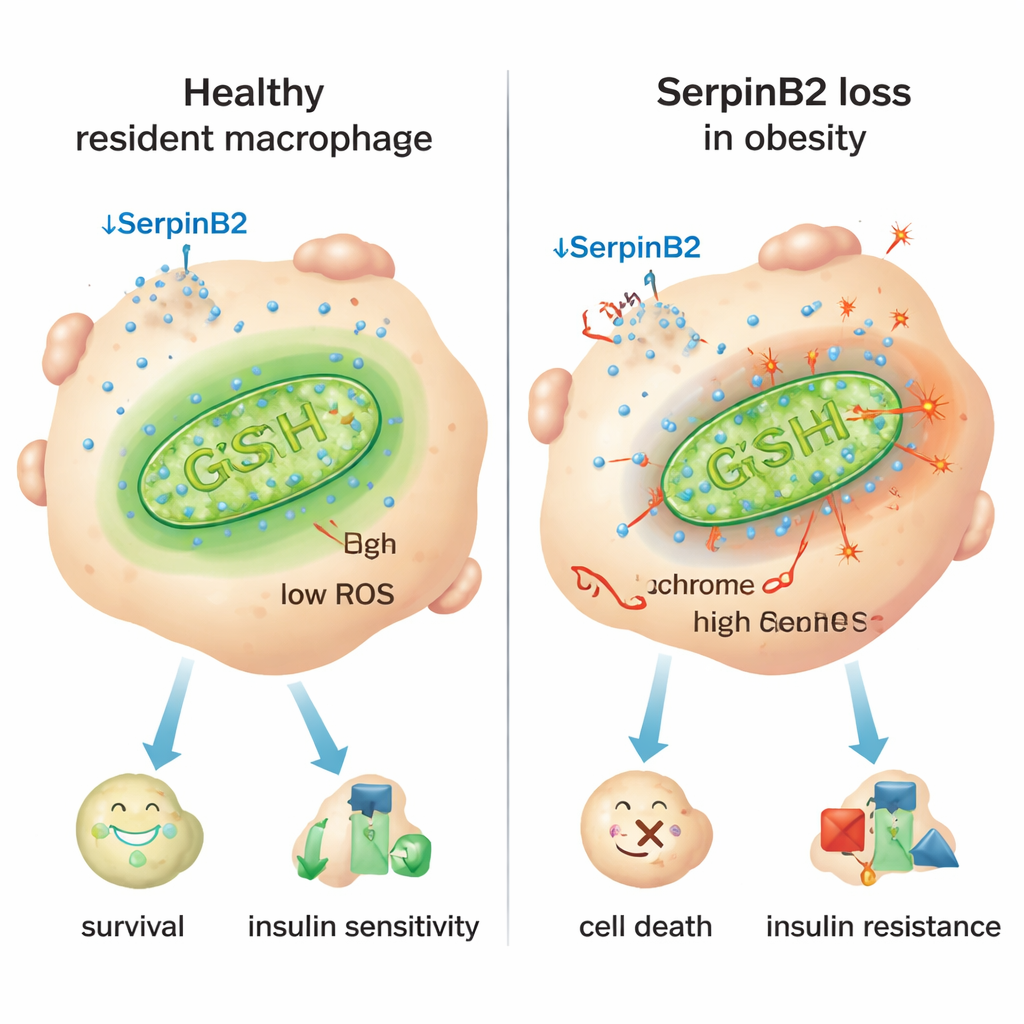
Der entzündliche Schalter und eine mögliche Gegenmaßnahme
Die Studie führte diesen mitochondrialen Stress auf chronische Entzündungssignale bei Adipositas zurück, insbesondere auf den Immunbotenstoff Interferon‑γ (IFN‑γ), der im Fettgewebe übermäßig produziert wird. IFN‑γ aktiviert einen Transkriptionsrepressor namens Ikaros, der an die Kontrollregion des SerpinB2‑Gens bindet und dessen Expression herunterfährt. In Mäusen, deren myeloide Zellen nicht auf IFN‑γ reagieren konnten, behielten die residenten Makrophagen SerpinB2, überlebten besser, und die Tiere zeigten niedrigere Blutzuckerwerte, bessere Insulinsensitivität und kleinere Fettzellen. Umgekehrt verschlimmerte die gezielte Deletion von SerpinB2 in Makrophagen die Glukoseintoleranz und Insulinresistenz, teils weil das Fettgewebe entzündlicher wurde und sich vergrößerte. Das Anheben der antioxidativen Glutathionspiegel mit dem Supplement N‑Acetylcystein (NAC) stellte den mitochondrialen Schutz wieder her, rettete das Überleben der residenten Makrophagen, verkleinerte Adipozyten und verbesserte die metabolischen Parameter selbst bei fehlendem SerpinB2.
Was das für die metabolische Gesundheit bedeutet
Für Laien ist die Kernaussage, dass nicht jedes Fett oder jede im Fettgewebe wohnhafte Immunzelle schädlich ist. Eine spezialisierte, langlebige Gruppe von Makrophagen im viszeralen Fett schützt tatsächlich vor unkontrollierter Entzündung und hohem Blutzucker, indem sie ihre Mitochondrien durch SerpinB2‑vermittelte antioxidative Mechanismen gesund hält. Bei Adipositas schalten chronische Entzündungssignale SerpinB2 aus, Mitochondrien geraten unter Stress, diese schützenden Zellen sterben ab und schädlichere Makrophagen übernehmen, was zur Insulinresistenz beiträgt. Die Arbeit legt nahe, dass Therapien, die residente Makrophagen erhalten — etwa durch Blockade der IFN‑γ/Ikaros‑Bremse auf SerpinB2 oder durch Unterstützung glutathionbasierter Antioxidantien — helfen könnten, metabolische Erkrankungen im Zusammenhang mit Adipositas zu verhindern oder zu behandeln.
Zitation: Vasamsetti, S.B., Sadaf, S., Uddin, M.A. et al. Tissue-resident macrophage survival depends on mitochondrial function regulated by SerpinB2 in chronic inflammation. Nat Commun 17, 1493 (2026). https://doi.org/10.1038/s41467-026-69196-4
Schlüsselwörter: viszerales Fett, Makrophagen, Mitochondrien, Insulinresistenz, SerpinB2