Clear Sky Science · de
Metabolisches Engineering der Doxorubicin-Biosynthese durch Optimierung von P450-Redoxpartnern und strukturelle Analyse von DoxA
Warum die Herkunftsgeschichte eines Krebsmedikaments wichtig ist
Doxorubicin ist eines der Hauptwirkstoffe der modernen Chemotherapie und wird zur Behandlung von Krebsarten von Leukämie bis Brusttumoren eingesetzt. Trotz jahrzehntelanger Anwendung ist die Herstellung dieses Arzneimittels erstaunlich umständlich: Die Industrie stellt es üblicherweise aus einer verwandten Verbindung her, anstatt das natürliche Mikroorganismus den letzten Schritt ausführen zu lassen. Diese Studie klärt, warum der produzierende Bakterienstamm Schwierigkeiten hat, die abschließenden chemischen Schritte zu vollenden, und zeigt, wie die Umgestaltung seiner internen Maschinerie die Produktion von voll ausgebildetem Doxorubicin deutlich steigern kann — was den Weg zu zuverlässigeren und potenziell preiswerteren Lieferungen öffnet.
Von Bodenbakterien zum lebensrettenden Arzneimittel
Doxorubicin gehört zur Gruppe der Anthracycline, einer Familie natürlicher Moleküle, die von Bodenbakterien der Gattung Streptomyces produziert werden. Diese Verbindungen teilen ein starres, flaches Kohlenstoffgerüst, das sich zwischen DNA-Basenpaare schiebt, sowie eine Zuckergruppe, die sich in die Rillen der DNA einlegt. Zusammen blockieren diese Merkmale das DNA-handhabende System der Zelle und lösen letztlich den Zelltod aus — nützlich gegen schnell wachsende Krebszellen. Der klassische Produzent, Streptomyces peucetius, stellt natürlicherweise überwiegend ein Vorläufermedikament namens Daunorubicin her und nur in geringem Umfang das wirksamere Doxorubicin, das sich durch nur eine zusätzliche sauerstofftragende Gruppe unterscheidet. Diese winzige strukturelle Änderung verbessert die Aktivität dramatisch, erweist sich für das Mikroben jedoch als überraschend schwer effizient zu erreichen.
Die richtige elektrische Verkabelung innerhalb der Zelle finden
Das entscheidende Enzym, das die letzten drei Oxidationsschritte am Wirkstoffgerüst katalysiert, heißt DoxA und gehört zur Familie der Cytochrom-P450-Enzyme. Wie eine winzige chemische Fabrik braucht DoxA einen stetigen Elektronenfluss, um Sauerstoff zu aktivieren und neue Sauerstoffatome in das Wirkstoffmolekül einzubauen. Innerhalb des Bakteriums werden diese Elektronen über eine Kette von Helferproteinen, sogenannten Redoxpartnern, geliefert. Das Genom von S. peucetius enthält mehrere Kandidaten, sodass unklar war, welche tatsächlich mit DoxA zusammenspielen. Durch den Vergleich der Genaktivität und des Stoffwechsels in einem Wildtyp-Stamm, einem Daunorubicin-reichen Mutanten und einem Doxorubicin-reichen Mutanten identifizierten die Forscher ein Ferredoxin (Fdx4) und eine Ferredoxin-Reduktase (FdR3) als die natürlichen Partner. Der Wiederaufbau dieses Trios in Reaktionsansätzen bestätigte, dass DoxA am besten funktioniert, wenn es in diese spezifische Elektronenübertragungskette eingesteckt ist — ähnlich wie das passende Netzteil für ein Gerät.
Das vom Enzym selbst verursachte Stocken lindern
Selbst mit der richtigen elektrischen Verkabelung neigt DoxA dazu, beim letzten Schritt, der Daunorubicin in Doxorubicin umwandelt, ins Stocken zu geraten. Frühere Arbeiten deuteten darauf hin, dass das Produkt selbst das Enzym verstopfen könnte. Das Team wandte sich einem benachbarten Gen, dnrV, zu, dessen Funktion zuvor ungeklärt war. Biochemische Tests zeigten, dass das DnrV-Protein eine Reihe von Anthracyclinen, einschließlich Doxorubicin, fest bindet, ohne sie chemisch zu verändern. Das Hinzufügen von DnrV zu DoxA-Reaktionen verbesserte den Reaktionsfluss stark und ermöglichte die vollständige Umwandlung der Vorläufer in das Endmedikament, während schädliche Nebenreaktionen vermieden wurden. Praktisch wirkt DnrV wie ein innerer Schwamm, der frisch erzeugtes Doxorubicin aufsaugt und verhindert, dass es das Enzym verstopft oder die DNA in der produzierenden Zelle schädigt.
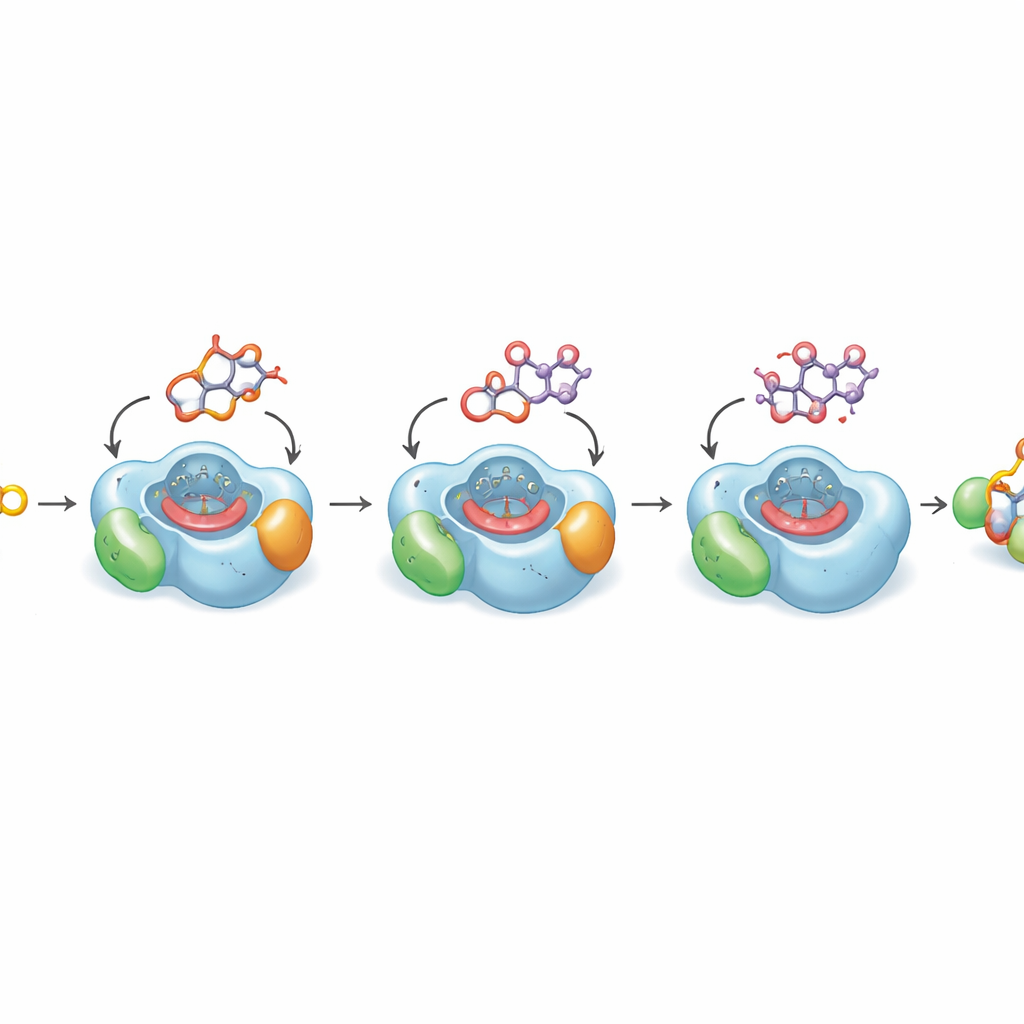
Warum der letzte Schritt so langsam ist
Um zu verstehen, warum die entscheidende letzte Oxidation von Natur aus träge abläuft, lösten die Autorinnen und Autoren hochauflösende Kristallstrukturen von DoxA in Komplex mit drei aufeinanderfolgenden Intermediaten. Diese Strukturen zeigen, wie der flache Wirkstoffkern und die angehängte Zuckergruppe in eine enge Tasche oberhalb der Hämgruppe des Enzyms passen, dem reaktiven Metallzentrum, das die Oxidation durchführt. Bei den früheren Schritten liegt das zu modifizierende Kohlenstoffatom nahe am Häm in einer idealen Position für die Reaktion. Beim letzten Substrat, Daunorubicin, jedoch biegt sich der Abschnitt des Moleküls, der hydroxyliert werden muss, vom Häm weg in eine kleine ölige Tasche — eine Anordnung, die Quantenberechnungen zufolge energetisch bevorzugt ist. Computersimulationen über Mikrosekunden bestätigen, dass das Molekül nur gelegentlich eine produktive Pose für diese letzte Sauerstoffeinfügung einnimmt. Diese strukturelle Verzerrung erklärt, weshalb die Umwandlung zu Doxorubicin naturgemäß ineffizient ist.
Den Bakterienstamm zur besseren Doxorubicin-Herstellung bauen
Mit diesen Erkenntnissen im Gepäck gestalteten die Forscher den Bakterienstamm gezielt neu, statt auf zufällige Mutagenese zu setzen. Sie führten ein DNA-Reparaturgen ein, um die Produktion zu stabilisieren, und installierten dann zusätzliche Kopien von doxA, den optimalen Redoxpartnern fdx4 und fdr3 sowie des hilfreichen Bindungsproteins dnrV unter sorgfältig ausgewählten Promotoren, um ihre Mengen auszubalancieren. Außerdem passten sie die Kulturbedingungen an und nutzten spezielle Harze, um toxische und klebrige Zwischenprodukte aufzunehmen. In Laborflaschen und in einem 20‑Liter-Bioreaktor produzierte der beste ingenieurmäßige Stamm 336 Milligramm Doxorubicin pro Liter Kultur mit einem Verhältnis von 81:19 zugunsten von Doxorubicin gegenüber Daunorubicin — eine Steigerung von etwa 180 % gegenüber dem Ausgangsstamm und eine wesentlich sauberere Produktmischung.
Was das für die zukünftige Versorgung mit Krebsmedikamenten bedeutet
Durch die Aufschlüsselung sowohl des elektrischen Versorgungssystems als auch der 3D-Struktur eines Schlüssel-Enzyms erklärt diese Arbeit, warum ein medizinisch wichtiges Mikroorganismus bei der Herstellung unseres wertvollsten Anthracyclins unterperformt. Die Abstimmung von DoxA mit seinen natürlichen Redoxpartnern, das Hinzufügen eines wirkstoffbindenden Hilfsproteins und die Neujustierung der Genexpression verwandelten einen zurückhaltenden Produzenten in einen robusten. Während weitere Enzymoptimierungen den letzten chemischen Schritt noch weiter beschleunigen könnten, bringt die Studie die vollbiologische Herstellung von Doxorubicin bereits deutlich näher an die industrielle Realität. Für Patientinnen und Patienten sowie Gesundheitssysteme könnten solche Fortschritte in eine sicherere, skalierbare und kosteneffizientere Versorgung mit einem wichtigen Chemotherapeutikum münden.
Zitation: Koroleva, A., Artukka, E., Yamada, K. et al. Metabolic engineering of doxorubicin biosynthesis through P450-redox partner optimization and structural analysis of DoxA. Nat Commun 17, 2358 (2026). https://doi.org/10.1038/s41467-026-69194-6
Schlüsselwörter: Doxorubicin-Produktion, Anthracyclin-Biosynthese, Enzym-Engineering, mikrobielle Wirkstoffherstellung, Cytochrom P450