Clear Sky Science · de
Atypische Proteinkinase C-Aktivierung treibt die intestinale Glukoseausscheidung bei Diabetes mellitus an
Den Darm in ein Zucker-Ventil verwandeln
Menschen mit Diabetes haben im Blut zu viel Zucker. Bariatrische Eingriffe wie der Magenbypass normalisieren den Blutzucker überraschend schnell, oft noch bevor nennenswerter Gewichtsverlust auftritt, aber wie das geschieht, war lange rätselhaft. Diese Studie offenbart ein darmbasiertes „Zucker-Ventil“ — eine Möglichkeit, wie der Darm Zucker aus dem Blut aufnehmen und einen Teil davon wieder in den Darmraum abgeben kann — und schlägt damit ein neues Wirkmechanismus-Ziel vor, das die Vorteile der Operation ohne Schnitt nachahmen könnte.
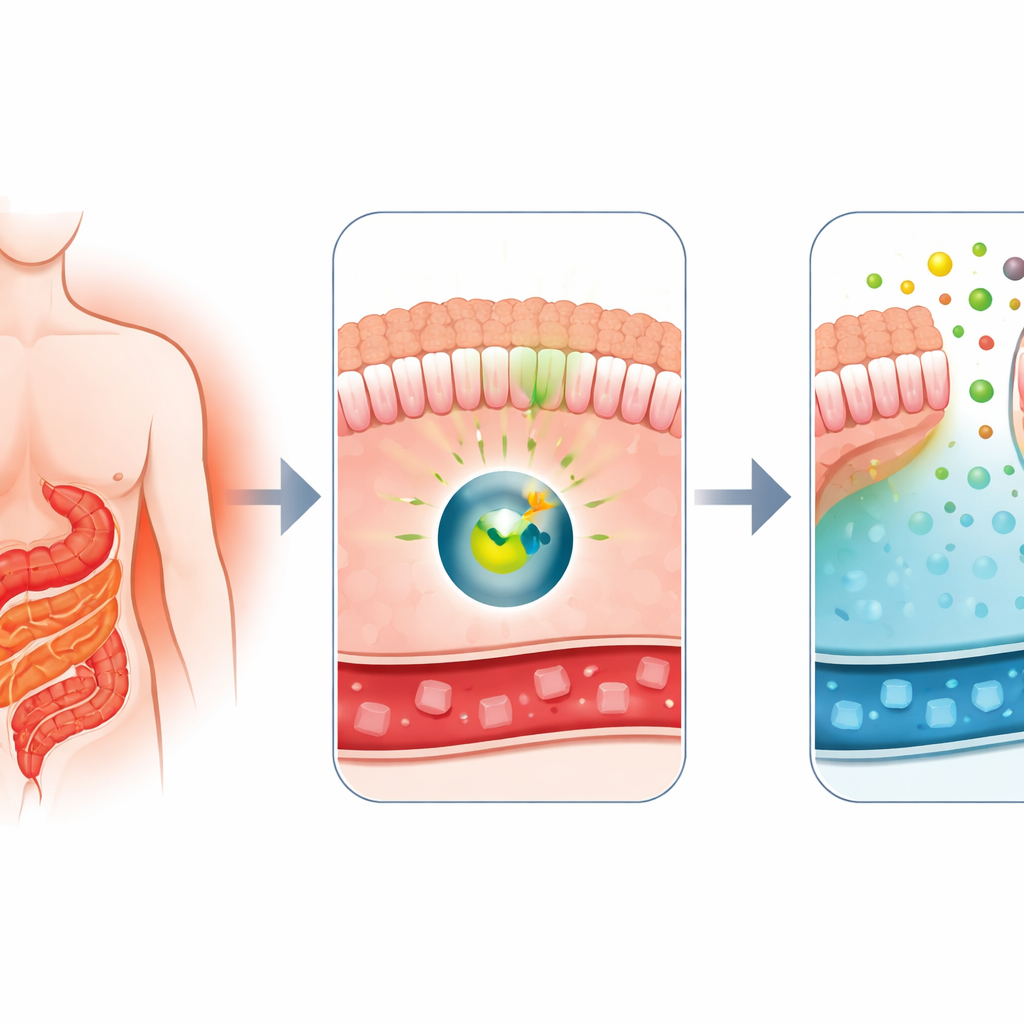
Warum die Operation den Blutzucker so schnell verändert
Ärzte wissen seit Langem, dass der Roux-en-Y-Magenbypass, eine häufige Gewichtsreduktionsoperation, auch eine der wirksamsten Behandlungen für Typ‑2‑Diabetes ist. Kurz nach der Operation verbessert sich der Blutzucker vieler Patienten oft dramatisch, noch bevor viel Gewicht verloren wurde. Frühere Arbeiten dieser Gruppe zeigten, dass nach dem Bypass Teile des Dünndarms beginnen wie ein Schwamm zu wirken, Glukose aus dem Blut aufzunehmen und einen Teil davon in den Darmlumen freizusetzen. Dieses ungewöhnliche Verhalten, bezeichnet als intestinale Glukoseausscheidung, schien von einem Transportprotein namens GLUT1 abhängig zu sein. Die große Frage war: Welcher molekulare Schalter veranlasst den Darm, in diesen zuckerreinigenden Zustand zu wechseln?
Mit Big Data einen molekularen Schalter finden
Um nach diesem Schalter zu suchen, nutzten die Forscher ein groß angelegtes computergestütztes Wirkstoffentdeckungssystem, das auf der Connectivity Map basiert — einer Datenbank darüber, wie Tausende von Chemikalien die Genaktivität in Zellen verändern. Sie verglichen Genexpressionsmuster aus fünf Situationen mit hoher intestinaler Glukoseausscheidung — darunter Gewebe von bypass-operierten Ratten und Zellen, die mit einem intestinalen Wachstumssignal behandelt wurden — mit Mustern, die von bekannten Arzneistoffen erzeugt werden. Eine Wirkstoffklasse stach beständig hervor: Aktivatoren der Proteinkinase C (PKC), einer Familie von Enzymen, die Signale innerhalb der Zelle weiterleiten. Bei genauerer Analyse konzentrierte sich das Team auf die „atypische“ Untergruppe der PKC-Enzyme, insbesondere auf ein Enzym namens PKCζ, dessen Aktivitätsmuster in Darmzellen dem nach Bypass ähnlichen, glukoseausscheidenden Zustand am nächsten kam.
Die Zuckerpumpe der Darmzellen in Aktion
Beim Heranzoomen auf einzelne Darmzellen mittels Einzelzell-RNA-Sequenzierung fanden die Autoren, dass der Bypass sowohl PKCζ als auch GLUT1 in bestimmten nährstoffaufnehmenden Zellen des distalen Dünndarms erhöht. In Zellkulturen und menschlichen Darmorganoiden führte eine künstliche Erhöhung von PKCζ oder die Behandlung mit Prostratin — einer pflanzlichen Verbindung, die diese atypischen PKC-Enzyme sicher aktiviert — dazu, dass GLUT1 an die Zelloberfläche gelangte. Dort wirkte GLUT1 wie eine zweiseitige Pumpe: Sie zog mehr Glukose aus der blutzugewandten Seite der Zellen und erlaubte überschüssige Glukose, in den Darmraum zu entweichen. Wichtig ist, dass diese Umlenkung von Zucker die zelluläre eigene Zuckerverbrennung (Glykolyse) nicht signifikant beschleunigte, was darauf hindeutet, dass der Haupteffekt die Beseitigung von Glukose und nicht die zusätzliche Energieproduktion war.
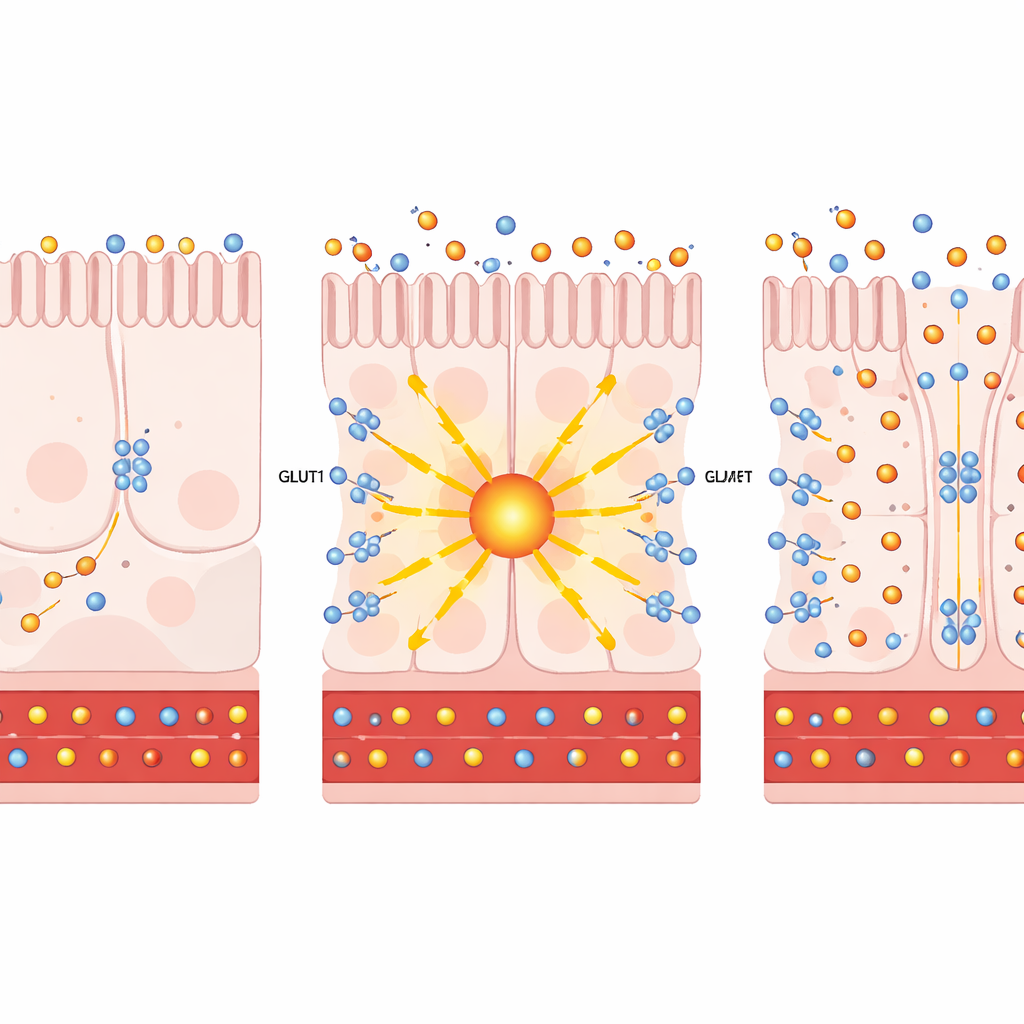
Von Zellen zu Mäusen: Operation ohne Skalpell nachahmen
Das Team prüfte anschließend, ob die Aktivierung dieses Weges in lebenden Tieren den Diabetes verbessern kann. Bei übergewichtigen, insulinresistenten Mäusen führte die gezielte Verabreichung von zusätzlichem PKCζ in den Darm zu langsamerer Gewichtszunahme, niedrigeren Nüchternblutzuckerwerten und besserer Glukosetoleranz. Radioaktive Zucker-Tracer zeigten, dass mehr Zucker vom distalen Darm aufgenommen und in das Darmlumen ausgespült wurde. Ein ähnliches Bild ergab sich in diabetischen Mausmodellen, die mit Prostratin behandelt wurden: Sie nahmen weniger zu, bewältigten Zuckerbelastungen besser und leiteten mehr Glukose in den Darm um — alles ohne Veränderungen der Insulinspiegel, der Nahrungsaufnahme oder der Darmbarriereintegrität. In Gewebeschnitten war GLUT1 sowohl an der blutzugewandten als auch an der darmzugewandten Seite der Zellen sichtbar und damit ideal positioniert, um Zucker aus dem Kreislauf zu ziehen und in den Darm zu drücken.
Was das für die zukünftige Diabetesbehandlung bedeuten könnte
Für Nicht‑Spezialisten lautet die Kernaussage: Der Darm kann zu einer gesteuerten Ausweichroute für überschüssigen Blutzucker gemacht werden. Durch die Aktivierung eines bestimmten Enzyms in Darmzellen — der atypischen PKC — gelang es den Forschern, die Zellen dazu zu bringen, mehr GLUT1‑Transporter an ihre Oberfläche zu bringen und sich wie ein reversibler Abfluss zu verhalten, der Zucker aus dem Blut zieht und einen Teil davon in den Darm abgibt. Bei Mäusen verbesserte diese darmgetriebene Glukosebeseitigung den Blutzucker und begrenzte die Gewichtszunahme, ohne Insulin übermäßig zu stimulieren, den Appetit zu verändern oder den Darm zu schädigen. Obwohl Prostratin und verwandte Verbindungen noch keine zugelassenen Diabetesmedikamente sind, weist diese Arbeit den aPKC–GLUT1‑Weg als vielversprechendes Ziel für künftige Medikamente aus, die einen Teil der metabolischen Vorteile eines Magenbypass ohne Operation nachbilden könnten.
Zitation: Kang, C.W., Hong, ZY., Oh, J.H. et al. Atypical protein kinase C activation drives intestinal glucose excretion in diabetes mellitus. Nat Commun 17, 2417 (2026). https://doi.org/10.1038/s41467-026-69193-7
Schlüsselwörter: intestinale Glukoseausscheidung, Typ-2-Diabetes, GLUT1-Transporter, atypische Proteinkinase C, Prostratin