Clear Sky Science · de
MerTK-ausgelöstes TGFβ1-autokrines Signal reguliert die Mikroglia-Antwort auf Neurodegeneration
Wie die Putztruppe des Gehirns Krankheiten formt
Wenn Nervenzellen im Gehirn und Sehnerv absterben, hinterlassen sie ein Trümmerfeld. Spezialisierte Immunzellen, sogenannte Mikroglia, fungieren als Putztruppe des Gehirns und „fressen“ diese Abfälle. Mikroglia machen jedoch mehr als nur sauber: ihre Reaktion kann Nervenschaltkreise schützen oder Erkrankungen wie Alzheimer verschlimmern. Diese Studie deckt eine verborgene Selbstkommunikationsschleife in Mikroglia auf, die durch Trümmer degenerierender Nervenfasern ausgelöst wird und mitbestimmt, wie stark diese Zellen auf Schäden reagieren.
Ein Auslöser in sterbenden Nervenfasern
Um diesen Prozess zu untersuchen, verwendeten die Forschenden ein Mausmodell, bei dem der Sehnerv gequetscht wird, sodass die langen Fortsätze der Augenneurone degenerieren, ohne dass die Zellkörper absterben. So lässt sich der Ablauf beim Achsabbruch sauber isolieren. Auf der Oberfläche dieser degenerierenden Fasern kehrt ein fettiges Molekül nach außen und wirkt als „Iss-mich“-Signal für nahegelegene Mikroglia. Diese Signale werden von einem Rezeptor auf Mikroglia namens MerTK erkannt, einem Mitglied einer kleinen Proteinfamilie, die Trümmer erkennt. Durch selektives Entfernen von MerTK in Mikroglia zeigte das Team, dass ohne diesen Rezeptor die Mikroglia ihre typische Reaktion auf Verletzung nicht entfalten: sie teilten sich weniger, bewegten sich weniger und schalteten weniger Gene ein, die mit Schadenkontrolle und Entzündung verknüpft sind.
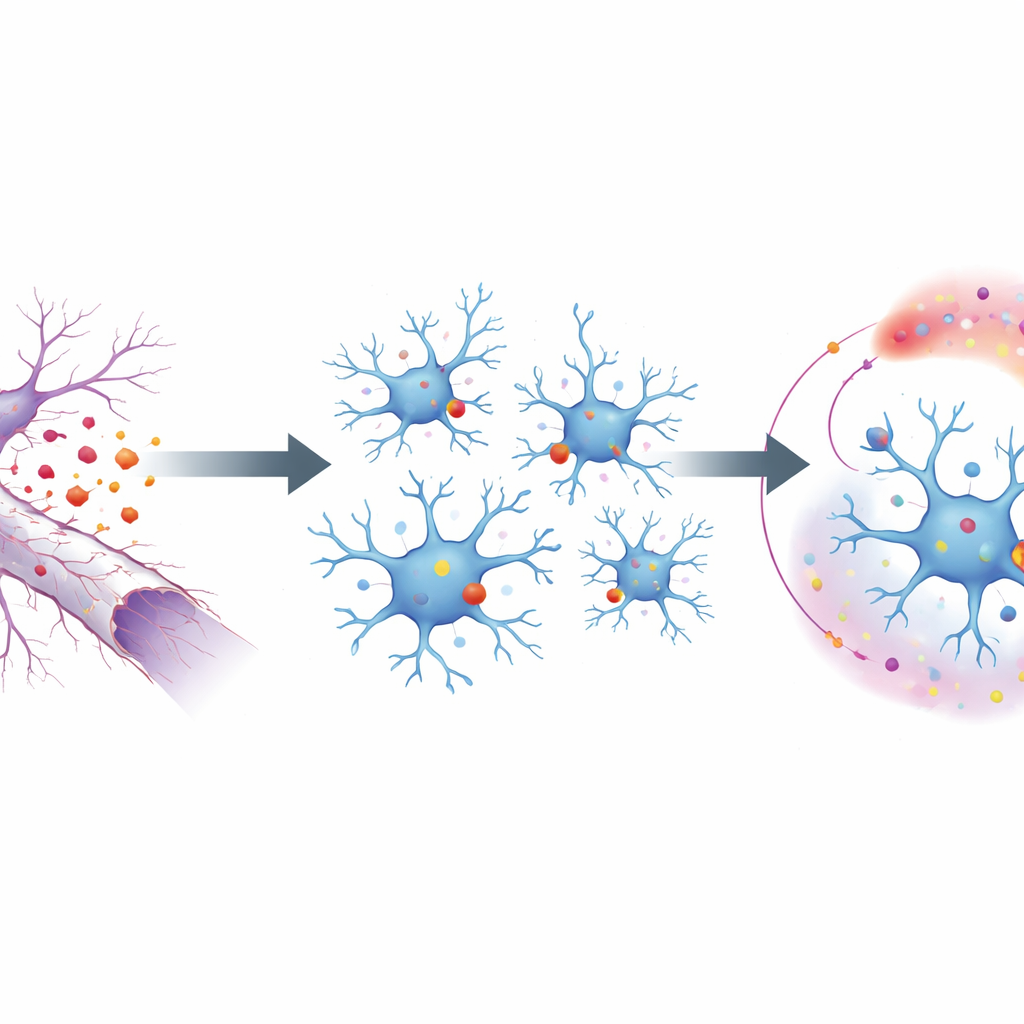
Vom Oberflächensignal zur genetischen Umprogrammierung
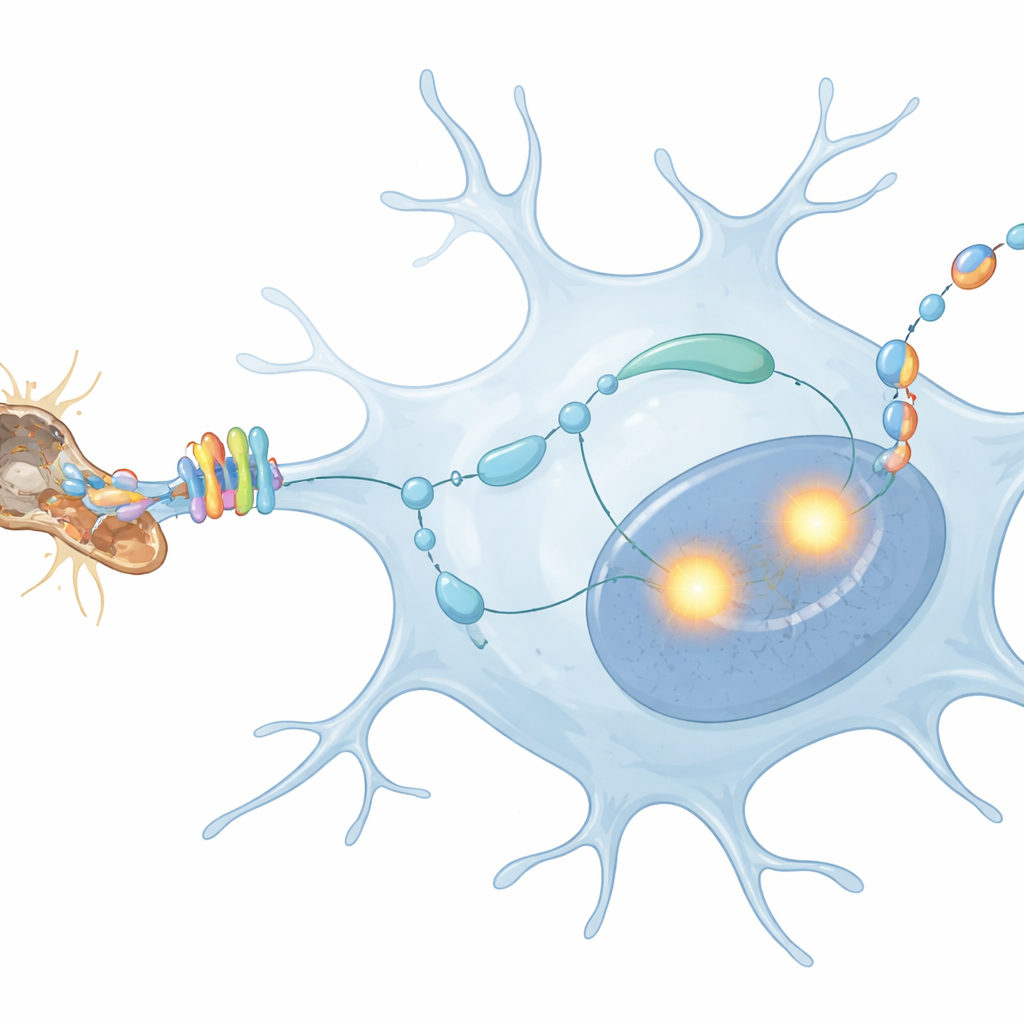
Ein Blick ins Innere der Mikroglia ließ die Forschenden verfolgen, wie das MerTK-Oberflächensignal in Veränderungen der Genaktivität umgewandelt wird. Sie fanden, dass MerTK eine molekulare Kaskade aktiviert, die Phospholipase C nennt, welche wiederum zwei Kontrollproteine im Zellkern, PU.1 und IRF8, hochfährt. Diese Faktoren wirken wie Vorarbeiter in der mikroglialen Produktionslinie und schalten viele Gene an, die für einen aktivierten Zustand nötig sind. Mithilfe von DNA-Bindungskarten entdeckte das Team, dass PU.1 und IRF8 direkt an eine spezifische Stelle im Gen binden, das TGFβ1 codiert, ein wirkungsvolles Signalmolekül. Wurde diese Bindungsstelle so verändert, dass die Vorarbeiter dort nicht mehr andocken konnten, konnten Mikroglia in verletzten Nerven die TGFβ1-Produktion nicht mehr hochfahren, obwohl andere Basisfunktionen intakt blieben.
Eine Selbstrückkopplung in Mikroglia
Die nächste Frage war, was TGFβ1 in diesem Kontext tatsächlich bewirkt. Die Studie zeigt, dass Mikroglia TGFβ1 produzieren und anschließend selbst darauf reagieren, wodurch eine autokrine, also selbstverstärkende, Rückkopplung entsteht. Wurden TGFβ1 oder seine Rezeptoren genetisch nur in Mikroglia entfernt, degenerierten die Axone nach Verletzung weiterhin, doch die Mikroglia zeigten nicht mehr ihr volles Aktivierungsprogramm. Sie vermehrten sich weniger und drückten weniger Gene für Schadensantwort und Entzündung aus, obwohl viele Marker ihrer hämostatischen Identität nach wie vor durch andere Signale unterdrückt wurden. Ein wichtiges downstream-Molekül der TGFβ-Signalübertragung, das phosphorylierte SMAD2, erschien nach Verletzung spezifisch in Mikroglia-Kernen und verschwand weitgehend, wenn TGFβ1 oder seine Rezeptoren ausgeschaltet wurden — ein Beleg dafür, dass die Selbstrückkopplung unterbrochen war.
Vom Maus-Sehnerv zu Alzheimer-Gehirnen
Um zu testen, ob dieser Pfad über ein künstliches Verletzungsmodell hinaus relevant ist, untersuchten die Autorinnen und Autoren ein häufig verwendetes Mausmodell der Alzheimer-Krankheit. In diesen Tieren wiesen Mikroglia, die sich um Amyloid-Plaques gruppierten, hohe Spiegel von PU.1, IRF8, TGFβ1 und aktiver TGFβ-Signalübertragung auf — ein Echo der Befunde im Sehnerv. Das Team wertete dann menschliche Daten aus einzelkernigen RNA-Sequenzierungen von Hirngewebe Alzheimer-Erkrankter aus. Dort stachen Mikroglia als die Hauptzellen hervor, die die menschlichen Entsprechungen von MerTK, PU.1, IRF8 und TGFB1 exprimieren. In postmortem Gehirnschnitten von Patientinnen und Patienten zeigten Mikroglia ebenfalls starke Anzeichen aktiver TGFβ-Signalübertragung, im Gegensatz zu Gewebe von Kontrollspendern. Zusammengenommen sprechen diese Beobachtungen dafür, dass dieselbe Selbstkommunikationsschleife auch beim Menschen in der Krankheit aktiv ist.
Warum dieses Selbstgespräch für die Gehirngesundheit wichtig ist
Diese Arbeit beschreibt eine Abfolge, in der Trümmer degenerierender Nervenfasern MerTK auf Mikroglia aktivieren, was wiederum PU.1 und IRF8 hochfährt, die ihrerseits Mikroglia zur Produktion von TGFβ1 antreiben, das wieder auf die Mikroglia zurückwirkt. Dieses Selbstgespräch schärft und erhält ihre Reaktion auf Neurodegeneration. Für eine nicht-fachliche Leserschaft lautet die Kernbotschaft: Die Putztruppe des Gehirns ist nicht nur passiv — sie hört aktiv auf eigene Signale, und diese Rückkopplung kann beeinflussen, ob ihr Handeln Neurone schützt oder Krankheiten wie Alzheimer vorantreibt. Das Verstehen und eventuell gezielte Einstellen dieses Kreislaufs könnte neue Wege eröffnen, schädliche Entzündungen zu dämpfen, ohne die nützliche Aufräumfunktion der Mikroglia zu beeinträchtigen.
Zitation: Huang, Y., Deng, Z., Zhou, Z. et al. MerTK-triggered TGFβ1 autocrine signal regulates microglial response to neurodegeneration. Nat Commun 17, 2312 (2026). https://doi.org/10.1038/s41467-026-69189-3
Schlüsselwörter: Mikroglia, Neurodegeneration, Alzheimer-Krankheit, Gehirnentzündung, TGF-beta-Signalübertragung