Clear Sky Science · de
Der redoxgetriebene Na+-Pumpmechanismus in der NADH‑Chinon‑Oxidoreduktase von Vibrio cholerae beruht auf dynamischen Konformationsänderungen
Wie Choleras Kraftwerk zum Arzneimittelziel wurde
Das Bakterium, das Cholera verursacht, Vibrio cholerae, überlebt und vermehrt sich, indem es in seiner Zellmembran ein winziges molekulares Kraftwerk betreibt. Diese Studie zeigt in bisher unerreichter Detailtiefe, wie einer seiner zentralen Motoren — ein Enzym namens Na⁺‑NQR — während seiner Arbeit die Form ändert, um Natriumionen aus der Zelle heraus zu pumpen. Das Verständnis dieser molekularen Maschine befriedigt nicht nur grundlegende Neugier darüber, wie Leben Nahrung in nutzbare Energie umwandelt, sondern weist auch Wege, Medikamente zu entwerfen, die schädliche Bakterien ausschalten, ohne menschliche Zellen zu beeinträchtigen.
Ein natriumgetriebener Motor in Bakterien
Viele marine und krankheitserregende Bakterien sind auf Na⁺‑NQR als ersten Schritt ihrer Atmungskette angewiesen, der Folge von Reaktionen, die Energie aus Nährstoffen gewinnt. Na⁺‑NQR sitzt in der inneren Membran und entnimmt Elektronen einem Brennstoffmolekül, NADH, die es über eine Kette farbiger „Hilfsmoleküle“ (Cofaktoren) an Chinon weiterreicht, ein weiteres kleines Molekül in der Membran. Während Elektronen fließen, nutzt das Enzym diese Energie, um Natriumionen (Na⁺) von innen nach außen zu transportieren und so ein Natriumgradient aufzubauen. Dieser Gradient ist wie eine geladene Batterie: Er treibt den bakteriellen Geißelmotor zum Schwimmen an, hilft bei der ATP‑Synthese (der Energiewährung der Zelle) und fördert die Aufnahme von Nährstoffen sowie den Efflux von Arzneistoffen. Da Na⁺‑NQR nur in Bakterien vorkommt und sich deutlich von verwandten Enzymen in unseren Mitochondrien unterscheidet, ist es ein attraktives Ziel für hochselektive Antibiotika.
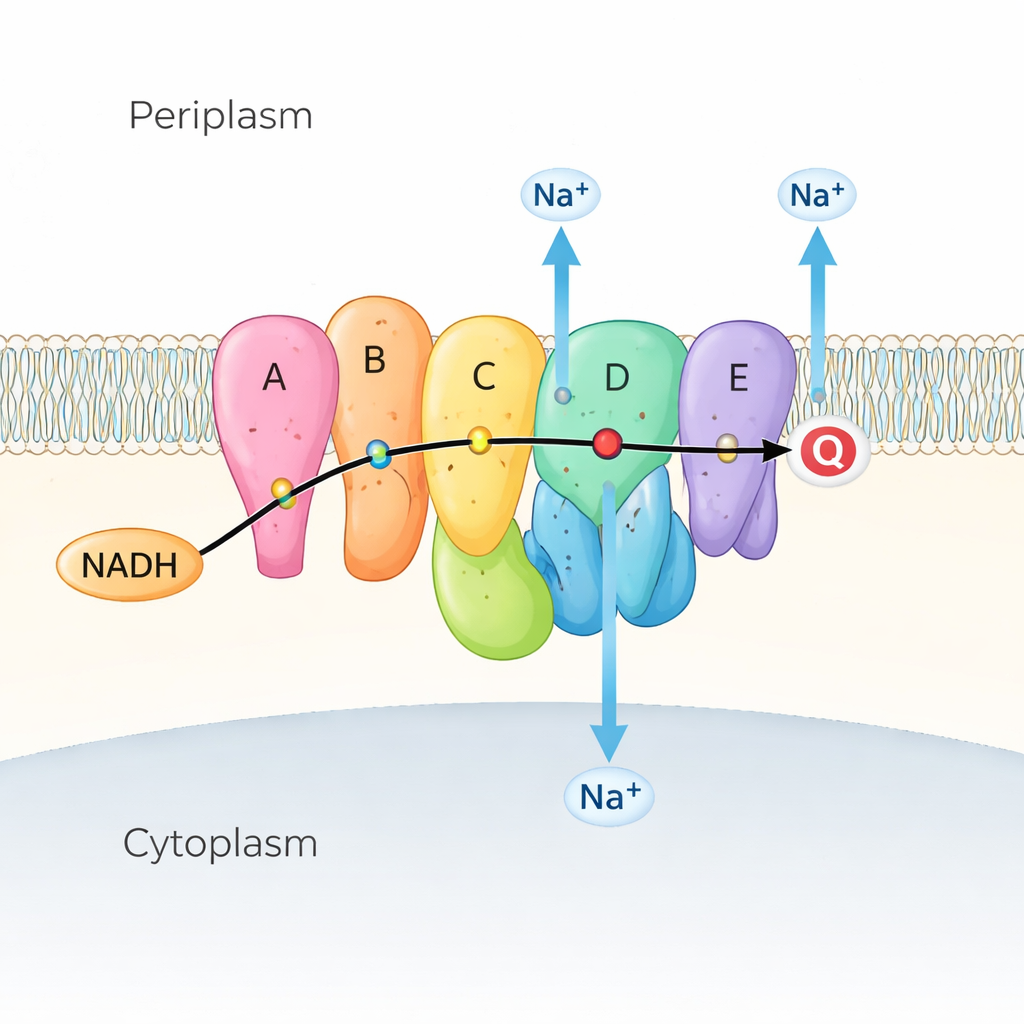
Die Maschine in Bewegung beobachten
Frühere Röntgen‑ und Kryo‑Elektronenmikroskopie‑Aufnahmen zeigten, wo die Untereinheiten und Cofaktoren von Na⁺‑NQR sitzen, offenbarten aber auch ein Rätsel: Einige kritische Elektronensprünge lagen zu weit auseinander, als dass Elektronen effizient übertragen werden könnten, sofern das Protein seine Form nicht verschiebt. Die Autoren gingen dieses Problem an, indem sie Na⁺‑NQR unter vielen leicht unterschiedlichen Bedingungen einfingen. Sie nutzten Mutanten, die bestimmte Cofaktoren entfernen, Wirkstoffe, die die Reaktion in bestimmten Stadien blockieren, und Lösungen mit und ohne Natrium. Mit hochauflösender Kryo‑EM und fortgeschrittener Bildanalyse konnten sie mehrere Konformationen desselben Enzyms trennen und rekonstruieren und verwandelten so statische Momentaufnahmen effektiv in einen Film seines Arbeitszyklus.
Ein flexibler Arm und eine schaltende Klemme
Ein zentrales Ergebnis betrifft eine flexible zytoplasmatische Untereinheit, NqrF, die zwei elektronentragende Cofaktoren hält. Das Team identifizierte drei Positionen für ihre „ferredoxin‑ähnliche“ Domäne — im Volksmund als „oben“, „mittig“ und „unten“ bezeichnet. Im seltenen, aber entscheidenden „unten“‑Zustand schwingt diese kleine Domäne in eine Tasche, die von zwei Membranuntereinheiten, NqrD und NqrE, gebildet wird, und bringt ihr Eisen‑Schwefel‑Cluster nahe genug heran, um ein Elektron weiterzureichen. Unterdessen verhält sich eine periplasmatische (äußere) Untereinheit namens NqrC wie eine bewegliche Klemme. In einer Konformation („stabil“) schmiegt sie sich an eine andere Membranuntereinheit, NqrB, positioniert, um Elektronen in Richtung des finalen Chinonakzeptors weiterzugeben. In einer zweiten („verschobenen“) Konformation bewegt sich NqrC in Richtung NqrD/E und bringt seinen Flavin‑Cofaktor näher, um ein Elektron von deren Eisen‑Schwefel‑Zentrum aufzunehmen. Diese Bewegungen zeigen, dass NqrF und NqrC als dynamische Kuriermoleküle agieren, die große Lücken in der Cofaktorkette überbrücken.
Wie Formänderungen Natrium pumpen
Das Herz der Natriumpumpe liegt in den gepaarten Untereinheiten NqrD und NqrE, die ein zentrales Bündel membranüberspannender Helices bilden. Anhand beider Strukturen und atomarer Molekulardynamik‑Simulationen zeigen die Autoren, dass, wenn das Eisen‑Schwefel‑Cluster in NqrD/E reduziert wird (ein Elektron aufnimmt), ein negativ geladenes Zentrum entsteht, das ein Na⁺‑Ion und einige Wassermoleküle von der zytoplasmatischen Seite anzieht und eine kurzlebige Bindungstasche bildet. Hydrophobe Aminosäuren oberhalb und unterhalb dieser Tasche verhalten sich wie innere und äußere Tore und kontrollieren den Zugang zum Ion. Wenn NqrD/E von einer „innenoffenen“ zu einer „außenoffenen“ Form umschalten, wandert das Na⁺ in Richtung Periplasma und wird schließlich freigesetzt, während das Eisen‑Schwefel‑Cluster wieder oxidiert wird. Simulationen zeigen, dass Na⁺ teilweise hydratisiert bleibt, aber niemals einen durchgehenden, wassergefüllten Kanal sieht, was darauf hinweist, dass das Enzym gegen unerwünschte Protonenlecks dicht verschlossen ist.
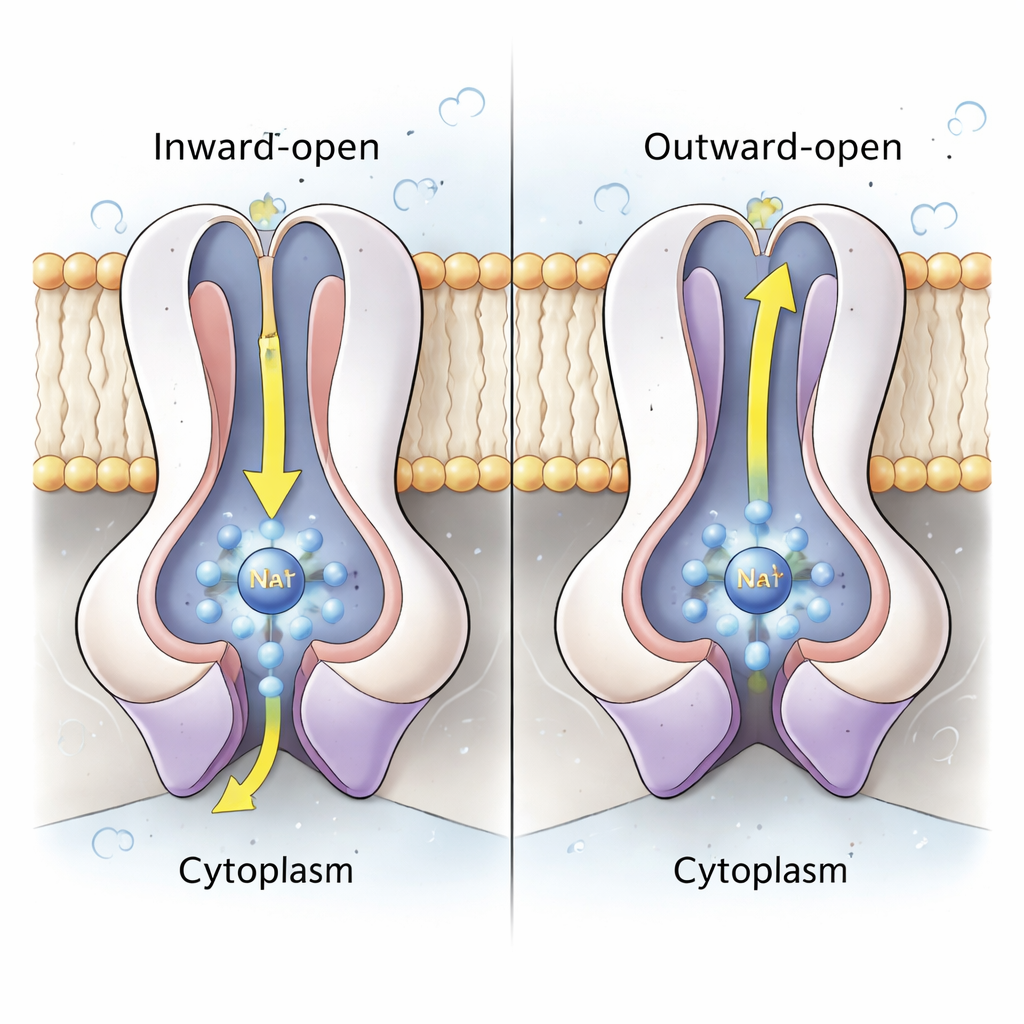
Ein koordinierter Zyklus, der die Richtung festlegt
Durch die Kombination aller strukturellen Zustände und Simulationen schlagen die Forscher einen sechsstufigen Zyklus vor. Zuerst bindet NADH und spendet Elektronen an NqrF, das dann ein Elektron an NqrD/E weiterreicht, wodurch die Na⁺‑Aufnahme aus dem Zytoplasma ausgelöst und die zentrale Tasche geladen wird. Der daraus resultierende Konformationswechsel von NqrD/E zur außenoffenen Form stößt sowohl Na⁺ ins Periplasma als auch fördert die Bewegung von NqrC in die Position zur Elektronenaufnahme. In den anschließenden Schritten werden Elektronen weiter an die finalen Flavin‑ und Riboflavin‑Cofaktoren und schließlich an Chinon übertragen, das zwei Elektronen aufnehmen muss, um zu Chinol zu werden. Wichtig ist, dass dieselben Formänderungen, die Na⁺ bewegen, zugleich NqrF und NqrC abwechselnd lockern und versteifen, sodass ein Vorwärtsfluss der Elektronen wahrscheinlich nur ist, wenn Na⁺ nach außen gepumpt wird, und ein Rückrutschen verhindert wird. Diese Kopplung hilft dem Enzym, Na⁺ gegen einen vorhandenen Gradienten zu pumpen und die bakterielle „Batterie“ geladen zu halten.
Warum das für Medizin und Biologie wichtig ist
Für Nicht‑Fachleute zeigt diese Arbeit, wie Leben aus Proteinen hochpräzise choreografierte Maschinen baut, in denen winzige Ladungsänderungen große, nutzbare Bewegungen auslösen. Für die Infektionsforschung klärt sie, dass die Na⁺‑Translokation in Na⁺‑NQR überwiegend durch den NqrD/E‑Kern erfolgt und nicht durch die zuvor verdächtigte Untereinheit NqrB. Diese Erkenntnis präzisiert, wo künftige Wirkstoffe am besten binden sollten, um den Motor, der Vibrio cholerae und andere Krankheitserreger antreibt, zu stören und dabei menschliche Enzyme zu schonen. Darüber hinaus liefert die Studie einen strukturellen Bauplan dafür, wie Redoxreaktionen mit Ionenpumpen verknüpft werden können — ein Gestaltungsprinzip, das die Natur in vielen Formen bioenergetischer Maschinerie wiederverwendet.
Zitation: Ishikawa-Fukuda, M., Seki, T., Kishikawa, Ji. et al. The redox driven Na+-pumping mechanism in Vibrio cholerae NADH-quinone oxidoreductase relies on dynamic conformational changes. Nat Commun 17, 1394 (2026). https://doi.org/10.1038/s41467-026-69182-w
Schlüsselwörter: Natriumpumpe, bakterielle Atmung, Na+-NQR, cryo‑EM, Antibiotika‑Ziele