Clear Sky Science · de
Ein synthetisches System für RNA‑reaktive Pyroptose basierend auf dem Typ‑III‑E CRISPR Nuklease‑Protease‑System
Tödliche Zellexplosionen als gezieltes Werkzeug
Unser Körper verteidigt sich manchmal, indem er infizierte oder beschädigte Zellen in einer feurigen Form des Selbstmords zur Explosion bringt, die als entzündliche Zellnekrose bekannt ist. Dieser Ausbruch entfernt nicht nur gefährliche Zellen, sondern ruft auch das Immunsystem herbei. Die neue Studie stellt einen synthetischen Genkreis namens DAMAGE vor, der die RNA‑Botschaften innerhalb einer Zelle lesen und entscheiden kann, ob diese Zelle zerstört werden soll. Indem die Forscher ein mikrobielles Abwehrsystem mit unserer eigenen Zelltodmaschinerie verbinden, zeigen sie einen Weg auf, um gezielt virusinfizierte, krebsartige oder gealterte Zellen zu vernichten und dabei gesunde Nachbarzellen zu verschonen. 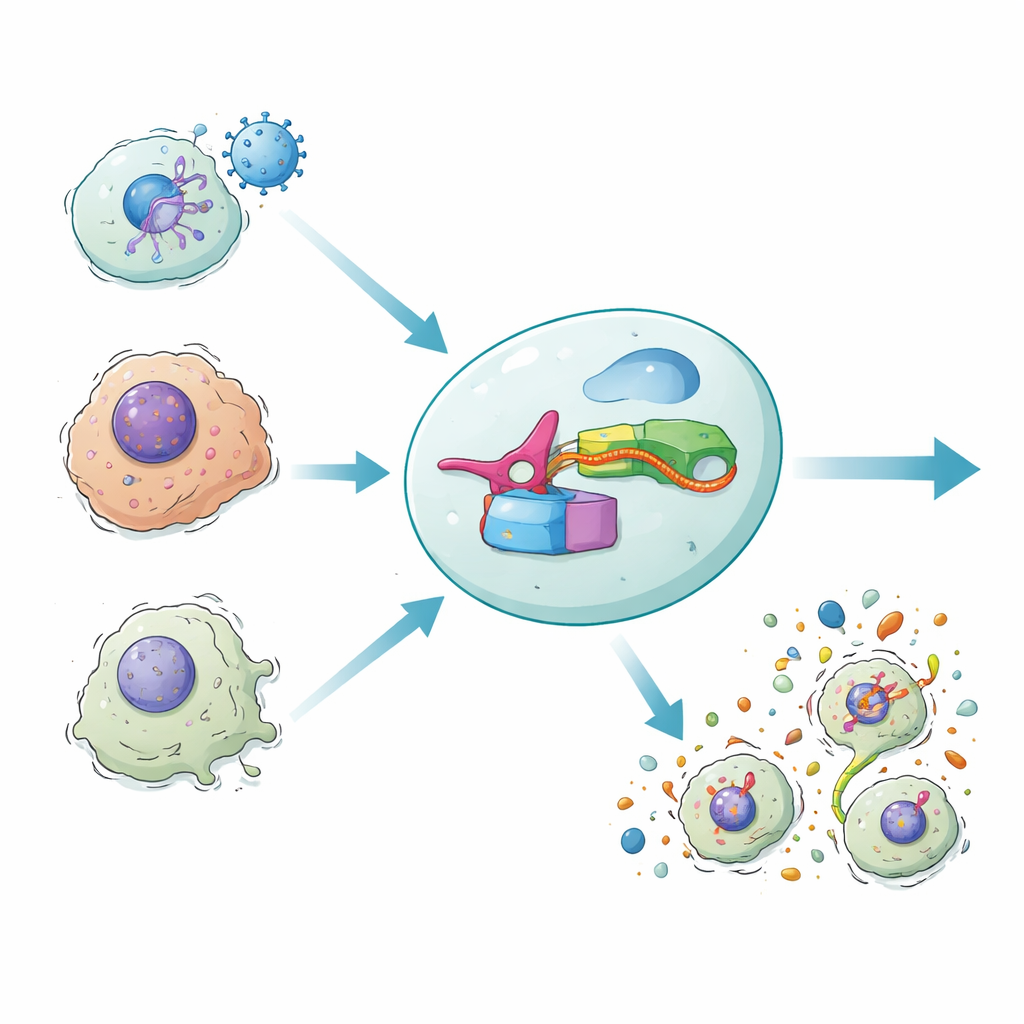
Wie Zellen sich normalerweise sprengen
Bei der entzündlichen Zellnekrose sitzt eine Familie von Proteinen, bekannt als Gasdermine, in Zellen wie geladene Ladungen. Jedes Gasdermin hat eine „tödliche“ vordere Hälfte, die Löcher in Zellmembranen schlagen kann, und eine „Sicherheitskappe“ als hintere Hälfte, die das Tötungselement in Schach hält. Wenn Immunsensoren Gefahr erkennen, schneiden Enzyme die Gasdermine in zwei Teile und befreien so die vordere Hälfte, damit sie Poren in der äußeren Membran bildet. Die Zelle schwillt an, platzt und schleudert Alarmsignale aus, die Immunzellen mobilisieren. Diese kraftvolle Reaktion hilft, Infektionen und Tumoren zu bekämpfen, doch ihr natürliches Kontrollnetzwerk ist verästelt und schwer für therapeutische Zwecke umzubauen.
Bakterielle Abwehrmechanismen zum Lesen von RNA nutzen
Bakterien haben kompakte Abwehrmodule entwickelt, die heute durch CRISPR‑Technologie bekannt sind. Eines davon, das Typ‑III‑E‑System, verwendet ein Protein namens Cas7‑11, das mit Hilfe einer kurzen Guide‑RNA an spezifische RNA‑Sequenzen binden kann. Wenn Cas7‑11 eine passende Ziel‑RNA findet, schaltet es ein Begleitenzym, Csx29, ein, das ein Partnerprotein, Csx30, schneidet. Die Autoren erkannten, dass Csx30 als anpassbares „Scharnier“ zwischen zwei Proteinabschnitten dienen könnte. Sie fügten dieses Scharnier zwischen die tödliche und die Sicherheits‑Hälfte menschlicher Gasdermine ein und schufen künstliche Vollstrecker, die nur dann auseinandergerissen werden, wenn der CRISPR‑ähnliche Sensor die gewählte RNA innerhalb einer Zelle erkennt.
Ein programmierbarer Todes‑Schalter für kranke Zellen
Dieses Design, genannt DAMAGE (für Death Manipulation Gene), besteht aus fünf Teilen: dem Cas7‑11‑Sensor, dem Csx29‑Schneider, einer Gasdermin–Csx30‑Fusion, einer Guide‑RNA und der Ziel‑RNA innerhalb der Zelle. Wenn die richtige RNA‑Botschaft erscheint, bindet Cas7‑11 sie, aktiviert Csx29, und Csx29 zerschneidet das Csx30‑Scharnier in dem Fusionsprotein. Die tödliche Gasdermin‑Hälfte wird freigesetzt, bohrt Poren in die Membran und die Zelle stirbt in einem entzündlichen Ausbruch. Durch einfaches Wechseln der Guide‑RNA leitete das Team DAMAGE auf verschiedene zelluläre Ziele um. Sie zeigten, dass es RNA des respiratorischen Synzytialvirus, Hochrisiko‑Humanpapillomavirus in Zervixkarzinomzellen und mehrere krebsfördernde KRAS‑Mutationen erkennen konnte, die sich vom normalen RNA‑Sequenz nur durch einen einzigen Buchstaben unterschieden. In jedem Fall wurden Zellen, die die verdächtige RNA trugen, selektiv eliminiert, während benachbarte Kontrollzellen intakt blieben. 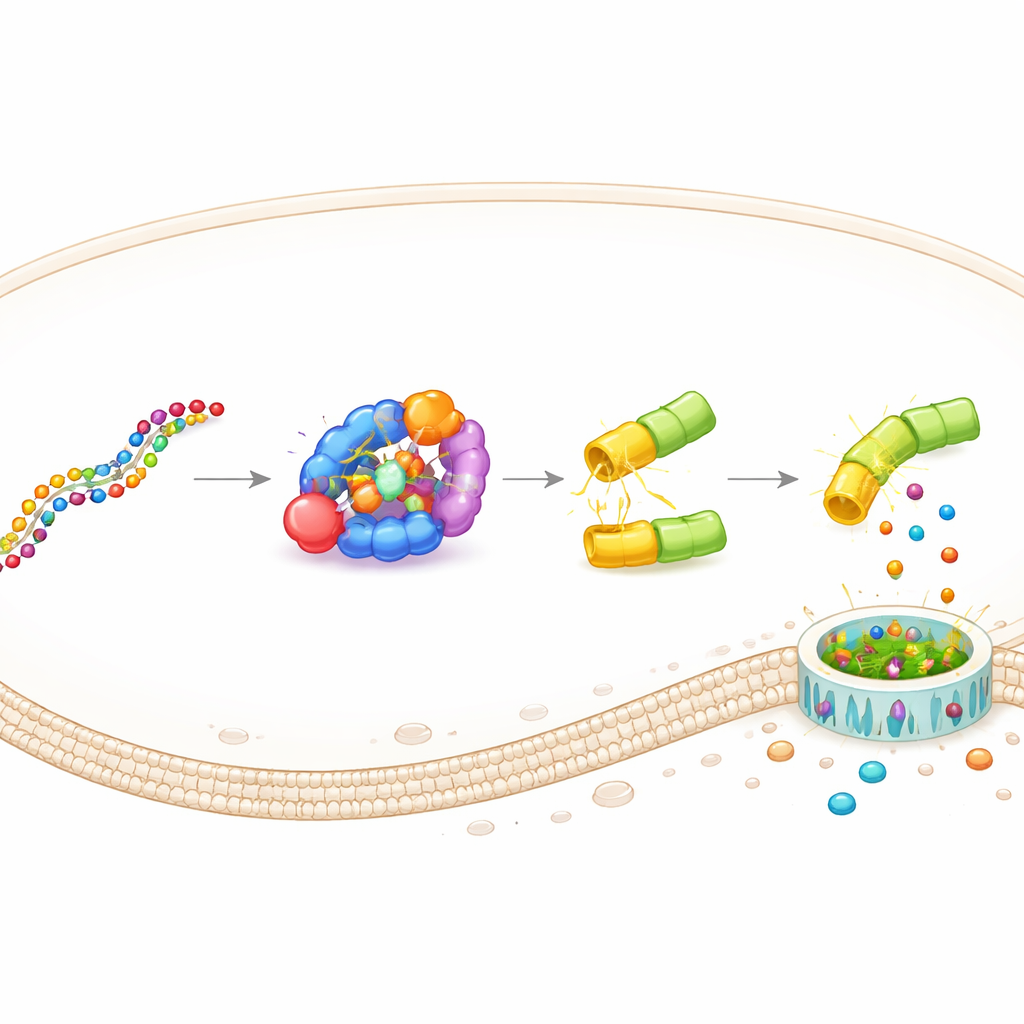
Gezielte Suche nach gealterten Zellen
Die Forscher fragten außerdem, ob DAMAGE seneszente Zellen aufspüren könnte – gealterte oder gestresste Zellen, die die Teilung einstellen, sich in Geweben ansammeln und zu Gebrechlichkeit sowie chronischen Erkrankungen beitragen. Solche Zellen erhöhen häufig die Produktion zweier Kontrollproteine, p16 und p21. Durch Programmierung von Guides gegen die RNAs für p16 und p21 schuf das Team eine Variante namens DAMAGE‑Aging. Dieser Schaltkreis tötete Zellen mit hohen Mengen dieser Botschaften, während Zellen, in denen p16 genetisch entfernt worden war, verschont blieben, was bestätigte, dass das System die momentane RNA‑Abundanz liest und nicht fixe DNA‑Veränderungen. Wirkstoffbehandlungen, die p16‑ oder p21‑Spiegel erhöhten, machten Zellen anfälliger für dieses gezielte Selbstzerstörungsprogramm.
Verpackung des Systems für künftige Therapien
Um einen Schritt näher an die praktische Anwendung zu kommen, komprimierten die Autoren die vielen DNA‑Bausteine von DAMAGE zu einer gestrafften Konstruktion, DAMAGE‑Plus, und zeigten, dass sie weiterhin zuverlässig funktionierte. Sie transkribierten dieses Konstrukt dann in synthetische mRNA, verpackten es in Lipidnanopartikel ähnlich denen der COVID‑19‑Impfstoffe und lieferten es in Kulturzellen ein. Die mRNA‑Version setzte den Schaltkreis erfolgreich zusammen und löste gezielten entzündlichen Zelltod in Zellen aus, die virale oder krebsbezogene RNAs trugen. Obwohl das Gesamtsystem noch sperrig ist und bislang nur in Zelllinien getestet wurde, deuten diese Ergebnisse darauf hin, dass programmierbares, RNA‑gesteuertes Zelltöten eines Tages über injizierbare mRNA‑Formulierungen einsetzbar sein könnte.
Eine neue Art, zelluläre Botschaften zu lesen und darauf zu reagieren
Einfach gesagt ist DAMAGE ein molekularer Türsteher, der die interne RNA‑„ID“ jeder Zelle überprüft und nur diejenigen hinauswirft, die gefährlich erscheinen – virusinfiziert, mutationsbeladen oder seneszent – indem er sie in eine explosive Form der Selbstzerstörung zwingt. Die Arbeit demonstriert, dass bakterielle RNA‑Sensoren präzise mit menschlicher Zelltodmaschinerie gekoppelt werden können und sogar Ein‑Buchstaben‑Unterschiede in genetischen Botschaften unterscheiden. Zwar ist noch viel an Engineering nötig, bevor ein solches System sicher bei Tieren oder Menschen eingesetzt werden kann, doch skizziert es eine kraftvolle neue Strategie: die lebendige RNA‑Kommunikation innerhalb von Zellen zu lesen und sie direkt in Lebens‑oder‑Todes‑Entscheidungen umzusetzen.
Zitation: He, M., Wang, W., Zhou, H. et al. A synthetic system for RNA-responsive pyroptosis based on type III-E CRISPR nuclease-protease. Nat Commun 17, 2565 (2026). https://doi.org/10.1038/s41467-026-69179-5
Schlüsselwörter: Pyroptose, CRISPR, RNA‑gerichtete Therapie, Krebsimmuntherapie, zelluläre Seneszenz