Clear Sky Science · de
hnRNPM arbeitet mit BCAS2 zusammen, um alternatives Spleißen während der Eizellentwicklung zu modulieren
Warum die Qualität der Eizelle wichtig ist
Jedes menschliche Leben beginnt mit einer einzelnen Eizelle, doch Wissenschaftler entdecken noch immer, wie diese ungewöhnlich großen Zellen sich auf den Moment der Befruchtung vorbereiten. Lange bevor Spermien eintreffen, legen heranreifende Eizellen tausende RNA-Botschaften an, die ihre Reifung und die ersten Tage der Embryonalentwicklung steuern werden. Diese Studie zeigt, wie ein wenig bekanntes Protein in Zusammenarbeit mit einem Partner diese Botschaften in Maus-Eizellen sorgfältig bearbeitet — und was geschieht, wenn dieses Bearbeitungssystem versagt.
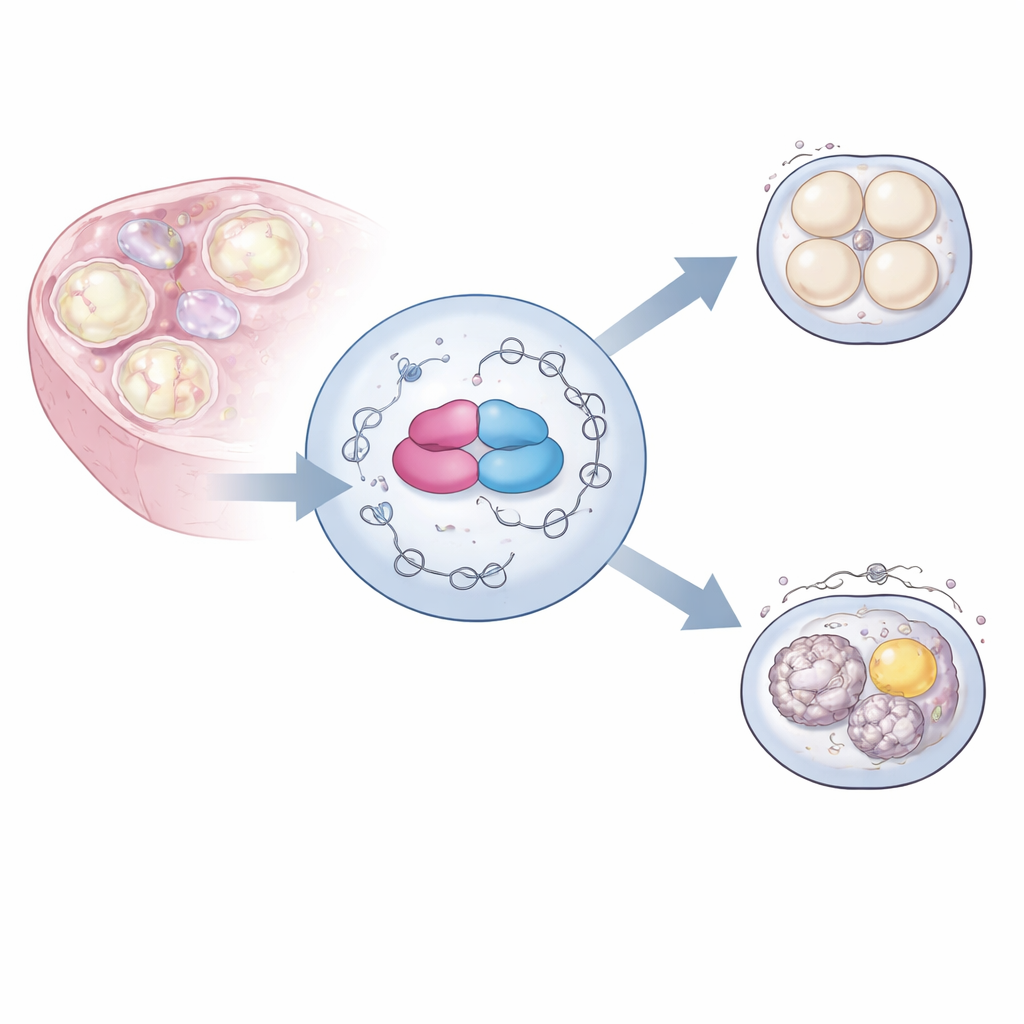
Torbeschützer der genetischen Botschaften
Eizellen wachsen über Wochen im Eierstock, während ihre DNA weitgehend inaktiv bleibt. In dieser Zeit sammeln sie eine umfangreiche Bibliothek mütterlicher RNA-Nachrichten, die zuvor aus dem Genom kopiert wurden. Diese Botschaften müssen in unterschiedlicher Weise zugeschnitten und zusammengesetzt werden, ein Prozess, der als alternatives Spleißen bezeichnet wird, um zur richtigen Zeit die passende Mischung von Proteinvarianten zu erzeugen. Die Autoren konzentrierten sich auf ein Protein namens hnRNPM, das zu einer großen Familie RNA-bindender Proteine gehört, und auf seinen Partner BCAS2, die beide im weiblichen Fortpflanzungssystem in hoher Menge vorkommen. Frühere Arbeiten deuteten an, dass diese Proteine viele RNAs in Eizellen binden, doch ihre genaue Rolle bei der Bestimmung der Fruchtbarkeit blieb unklar.
Was schiefgeht, wenn dieser Editor fehlt
Um die Funktion von hnRNPM zu untersuchen, entferzte das Team mithilfe genetischer Techniken gezielt das Hnrnpm-Gen aus den Vorläufern von Maus-Eizellen. Die Eierstöcke dieser Weibchen wirkten normal und produzierten eine ähnliche Anzahl von Eizellen wie die Kontrollen. Doch wenn diese Eizellen im Labor befruchtet wurden, entwickelten sie sich fast nie über die ersten Zellteilungen hinaus, womit die Weibchen vollständig unfruchtbar waren. Eine genauere Untersuchung der unreifen Eizellen zeigte dunkle Klumpen im normalerweise klaren Zytoplasma. Elektronenmikroskopie zeigte, dass ein feines internes Gerüst, das sogenannte zytoplasmatische Gitter, weitgehend fehlte, und dass wichtige Organellen wie Mitochondrien und Fetttröpfchen abnormal verklumpt statt gleichmäßig verteilt waren. Diese Veränderungen wiesen auf ein tiefgreifendes Problem mit der internen Organisation der Eizelle hin.
Gestörte Zellteilungsmaschinerie
Die gleichen mutierten Eizellen hatten auch Schwierigkeiten, die Meiose abzuschließen, die spezialisierte Zellteilung, die die Chromosomenzahl halbiert. Wenn Forscher die Eizellen in Kultur reifen ließen, konnten sie die Meiose zwar einleiten, blieben aber meist vor deren Abschluss stecken. Unter dem Mikroskop waren die Strukturen, die Chromosomen auseinanderziehen — die Spindeln — verdreht, multipolar oder schlecht verankert. Ein Protein namens Pericentrin, das hilft, die Spindelpole zu organisieren, erschien verspätet und an falschen Stellen. Zusammengenommen führten diese Defekte dazu, dass die Eizellen Chromosomen nicht zuverlässig ausrichten und trennen konnten, was wahrscheinlich die Ursache für das vollständige Entwicklungsversagen nach der Befruchtung ist.
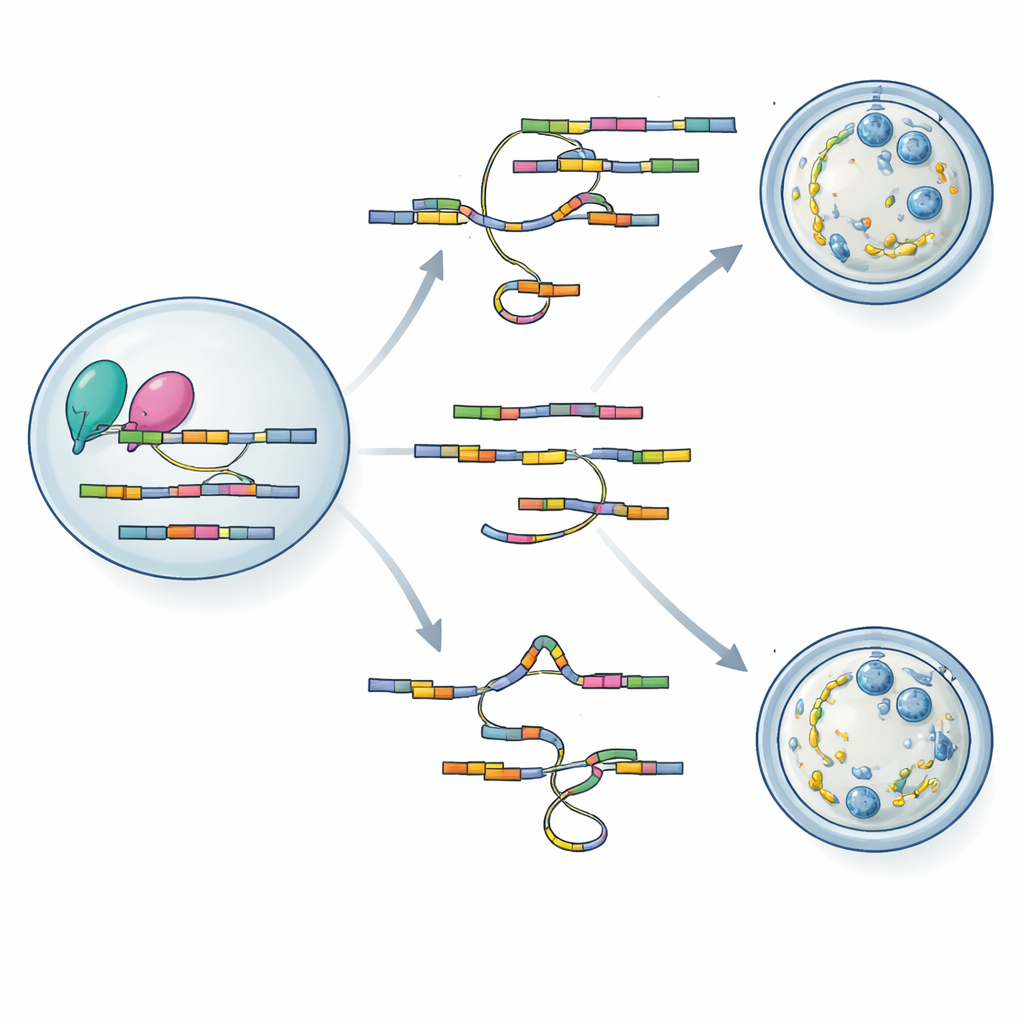
Lesen und Umschreiben von RNA-Anweisungen
Um zu verstehen, wie der Verlust von hnRNPM zu so umfassenden Defekten führt, wandte sich das Team zwei leistungsfähigen Sequenzierverfahren zu, die für winzige Eizellenproben angepasst wurden. Mit SCAN-seq, das voll-längige RNA-Moleküle von einzelnen Oozyten liest, entdeckten sie mehr als tausend Spleißveränderungen in mutierten Eizellen, darunter viele zuvor unbekannte RNA-Varianten. Gene, die am Aufbau des zytoplasmatischen Gitters, an der Kontrolle des Spindelverhaltens und an der Regulierung des meiotischen Zellzyklus beteiligt sind, waren besonders betroffen. Eine zweite Methode, LACE-seq, kartierte genau, wo hnRNPM auf RNAs bindet, und zeigte eine Präferenz für GU-reiche Abschnitte innerhalb von Exons. Durch Überlagerung der beiden Datensätze zeigten die Autoren, dass hnRNPM direkt auf vielen der Botschaften sitzt, deren Spleißen sich ändert, wenn das Protein fehlt, und verbanden so seine Bindungsaktivität mit der Spleißgenauigkeit.
Ein Kooperationsmodell zur Kontrolle der Eizelle
Proteinandersuchungen zeigten, dass hnRNPM physisch mit BCAS2 und mit Kernkomponenten der Spleißmaschinerie assoziiert ist. Die beiden Partner binden viele der gleichen RNA-Ziele und verändern sie oft in ähnlicher Weise, wenn eines der Proteine gestört ist. Auffällig war, dass der Verlust von hnRNPM die BCAS2-Proteinspiegel verringerte und BCAS2s Bindung an gemeinsame RNA-Ziele schwächte, was darauf hindeutet, dass hnRNPM nicht nur Botschaften bearbeitet, sondern auch hilft, seinen Partner auf diesen Botschaften zu stabilisieren. Die Autoren schlagen ein Modell vor, in dem hnRNPM und BCAS2 einen kooperativen Komplex bilden, der während des Eizellenwachstums wichtige mütterliche RNAs anpasst und so die korrekte Assemblierung des zytoplasmatischen Gitters und eine zuverlässige meiotische Teilung sicherstellt.
Was das für die Fruchtbarkeit bedeutet
Einfach gesagt zeigt diese Arbeit, dass ein molekulares Redaktionsteam — hnRNPM und BCAS2 — im Hintergrund wirkt, um Eizellen auf das Leben nach der Befruchtung vorzubereiten. Fehlt dieses Team, bricht das interne Gerüst der Eizelle zusammen, ihre Chromosomen-Sortiermaschine versagt, und obwohl die Eizelle in normaler Anzahl produziert wird, kann sie die Embryonalentwicklung nicht unterstützen. Da hnRNPM bei Mäusen und Menschen hochgradig ähnlich ist, deuten diese Befunde auf ein konserviertes Qualitätskontrollsystem hin, das bestimmten Formen unerklärter weiblicher Infertilität zugrunde liegen könnte und neue Ansatzpunkte für Diagnose oder Behandlung bietet.
Zitation: Zhou, S., Liu, D., Gan, S. et al. hnRNPM cooperates with BCAS2 to modulate alternative splicing during oocyte development. Nat Commun 17, 2681 (2026). https://doi.org/10.1038/s41467-026-69176-8
Schlüsselwörter: Eizellentwicklung, alternatives Spleißen, weibliche Infertilität, RNA-bindende Proteine, zytoplasmatisches Gitter