Clear Sky Science · de
Ensembles intrinsisch ungeordneter Proteine in atomarer Auflösung mit AlphaFold
Warum formwandelnde Proteine wichtig sind
Unsere Zellen enthalten viele Proteine, die niemals eine einzige, starre Gestalt einnehmen. Diese „intrinsisch ungeordneten“ Proteine verhalten sich eher wie biegsame Nudeln als wie ordentlich gefaltete Maschinenteile, sind aber dennoch zentral für Prozesse von der Zellsignalgebung bis zu neurodegenerativen Erkrankungen. Weil sie ständig bewegen und biegen, ist es extrem schwierig, ihre gesamte Formvielfalt auf atomarer Ebene zu erfassen — das erfordert meist jahrelange Experimente und aufwändige Berechnungen. Dieser Artikel stellt einen neuen Weg vor, KI und physikalische Prinzipien zu kombinieren, um diese unruhigen Moleküle deutlich effizienter zu kartieren.
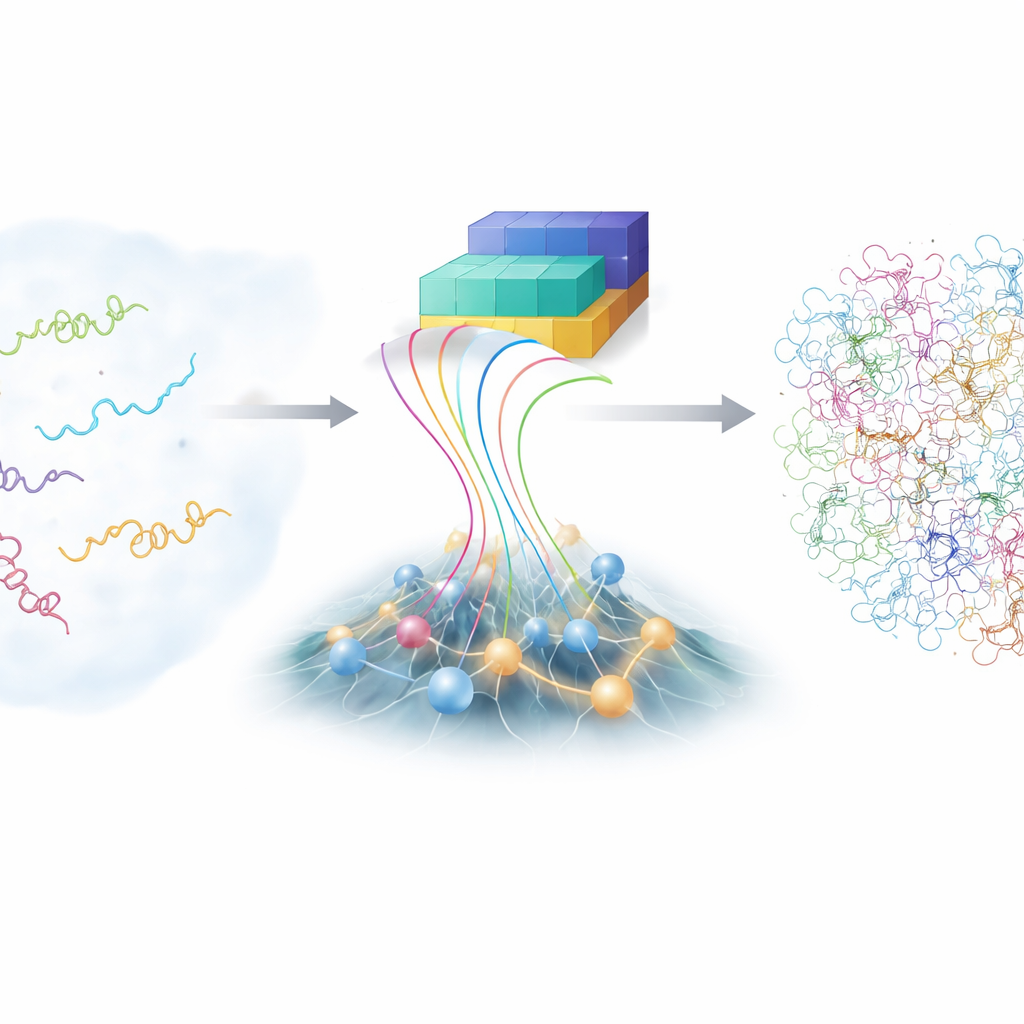
Die Herausforderung unruhiger Moleküle
Im Gegensatz zu Lehrbuchdarstellungen, die eine einzige ordentliche Struktur zeigen, durchstreifen intrinsisch ungeordnete Proteine (IDPs) eine weite Landschaft möglicher Gestalten. Diese Flexibilität hilft ihnen, viele verschiedene Partner zu erkennen, macht sie aber auch berüchtigt schwer untersuchbar. Traditionelle Labortechniken wie fortgeschrittene Kernspinresonanz und Röntgenstreuung liefern Mittelwerte über viele Konformationen, nicht aber jede einzelne Form. Computersimulationen in voller atomarer Detailtreue können prinzipiell jedem Atom folgen, während ein IDP sich windet, sind aber extrem rechenintensiv und abhängig von fein abgestimmten physikalischen Modellen. Daher verfügt die Wissenschaftsgemeinschaft nur über eine begrenzte Sammlung genauer, detaillierter IDP‑Ensembles als Lerngrundlage.
Kluge Annahmen mit physikalischen Regeln verbinden
In den letzten Jahren hat die AlphaFold‑Familie tiefenlernender Werkzeuge die Biologie überrascht, indem sie Proteinstrukturen aus Aminosäuresequenzen vorhersagt. Für ungeordnete Proteine ist AlphaFolds übliche Stärke — das Erraten einer einzigen besten Gestalt — jedoch weniger hilfreich, weil IDPs eben nicht nur eine haben. Was AlphaFold liefert, sind reichhaltige Informationen darüber, wie wahrscheinlich es ist, dass verschiedene Teile der Kette näher beieinander oder weiter auseinander liegen. Die Autoren entwickelten ein neues Rahmenwerk namens bAIes, das diese KI‑abgeleiteten Informationen als weiche Leitlinien behandelt und mit einem schnellen, physikbasierten Modell verbindet, das bewusst von einer „Random‑Coil“-Sicht ausgeht, in der die Kette alle möglichen Biegungen und Drehungen ohne Bevorzugung einer bestimmten Struktur erkundet.
Von zufälligen Verwicklungen zu realistischen Ensembles
Zunächst konstruierten die Forschenden ein effizientes physikalisches Modell, das das Verhalten einer völlig ungeordneten Proteinkette reproduziert, basierend auf Statistiken, die aus Tausenden bekannter Proteinstrukturen gewonnen wurden. Dieses Modell dient als „Prior“ — die Basiserwartung, wie sich ein IDP bewegt, wenn sonst nichts bekannt ist. Anschließend liest bAIes AlphaFolds Vorhersagen darüber aus, welche Restpaarungen dazu neigen, nahe zu kommen. Anstatt das Protein in ein einzelnes Muster zu pressen, verwandelt es diese Hinweise in sanfte Distanzrestriktionen mit eingebauter Unsicherheit, sodass die Kette die KI‑Vorschläge nur dann erfüllt, wenn sie mit dem umfassenderen physikalischen Bild vereinbar sind.
Abgleich mit realen Experimenten
Um zu prüfen, ob dieser Ansatz funktioniert, wendete das Team bAIes auf eine Auswahl von 21 Proteinen an, die von fast vollständig zufälligen Coils bis zu komplexeren Systemen mit transienten Helices und mehreren Domänen reichten. Für jedes verglichen sie die resultierenden computererzeugten Ensembles mit einer breiten Palette experimenteller Messungen, die sowohl lokale Details als auch globale Größe und Form untersuchen. Bei sehr flexiblen Proteinen wie dem Alzheimer‑assoziierten Peptid Aβ40 war das einfache Random‑Coil‑Modell bereits nahe an der Realität, und bAIes bewahrte diese gute Übereinstimmung. Bei teilweise strukturierten Proteinen verbesserte bAIes die Übereinstimmung mit Experimenten, indem es korrekt erfasste, wo kurze helikale Segmente und kompakte Bereiche auftauchen und wieder verschwinden. Entscheidend ist, dass die Methode robust blieb, selbst wenn AlphaFold übermäßig selbstsicher war und fälschlich stabile Faltungen vorhersagte, wo Lösungsexperimente Unordnung zeigen, weil bAIes explizit Fehler in der KI‑Eingabe zulässt.
Besser oder vergleichbar mit existierenden Methoden
Die Autoren stellten bAIes dann gegenüber aufwendigen All‑Atom‑Simulationen auf spezialisierten Supercomputern, führenden grobkörnigen Modellen, die Proteine in Perlen vereinfachen, und neuen Deep‑Learning‑Generatoren, die auf Simulationsdaten trainiert wurden. In mehreren Tests entsprach bAIes durchgängig oder übertraf diese Ansätze bei der Reproduktion experimenteller Daten, während es deutlich weniger Rechenaufwand erforderte als vollständige Simulationen. Es funktionierte zudem über einfache IDPs hinaus, handhabte Proteine mit mehreren starren Domänen, die durch flexible Verbindungsstücke gekoppelt sind, und stellte ihre Gesamtkonfigurationen in Lösung wieder her. Wenn die Forschenden die bAIes‑Ensembles weiter mit experimentellen Daten feinabstimmten, verbesserte sich die Übereinstimmung noch weiter, was zeigt, dass die Methode einen kraftvollen Ausgangspunkt für integrative Modellierung bieten kann.
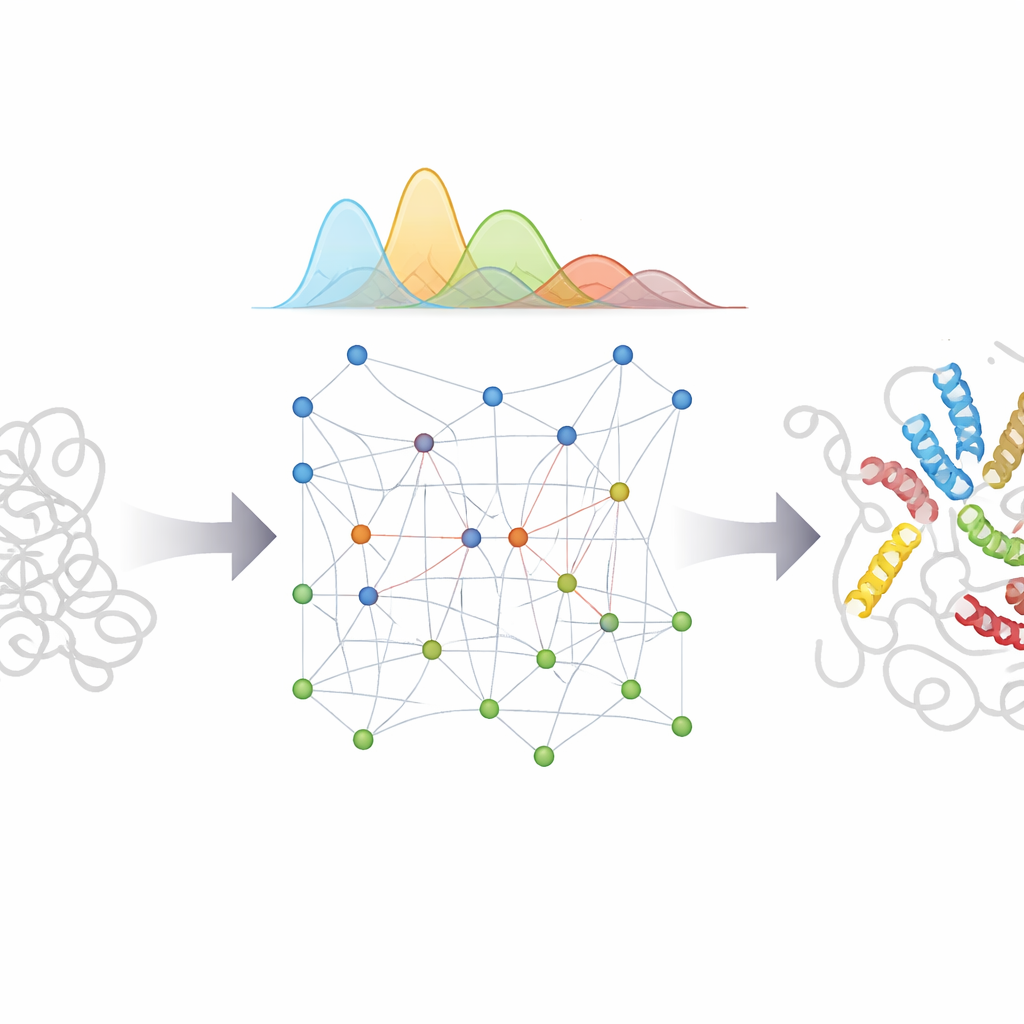
Was das für Biologie und Medizin bedeutet
Indem AlphaFolds Mustererkennungsstärke mit einem sorgfältig entworfenen physikalischen Modell und einer bayesschen Behandlung von Unsicherheit verknüpft wird, bietet bAIes einen praktischen Weg zu detaillierten „Filmen“ ungeordneter Proteine statt einzelner Schnappschüsse. Diese atomar detaillierten Ensembles können Forschenden helfen zu verstehen, wie flexible Regionen Partner erkennen, wie Fehlfaltung und Aggregation bei Krankheiten wie Parkinson und Alzheimer beginnen und wie kleine Moleküle an schwer fassbare, sich verschiebende Ziele binden könnten. Da die Methode effizient ist und als Open‑Source‑Software verfügbar ist, kann sie weit verbreitet eingesetzt werden, um realistische Ensembles vieler ungeordneter Proteine zu erzeugen, Experimente zu leiten und künftige KI‑Systeme zu unterstützen, die nicht nur eine Struktur, sondern die gesamte Bandbreite der Formen vorhersagen wollen, die die flexibelsten Moleküle des Lebens annehmen können.
Zitation: Schnapka, V., Morozova, T.I., Sen, S. et al. Atomic resolution ensembles of intrinsically disordered proteins with Alphafold. Nat Commun 17, 2399 (2026). https://doi.org/10.1038/s41467-026-69172-y
Schlüsselwörter: intrinsisch ungeordnete Proteine, AlphaFold, Bayessche Modellierung, Protein‑Ensembles, Strukturelle Biologie