Clear Sky Science · de
Einfluss von Lösungsmittelkräften und gebrochener Symmetrie auf die Assemblierung entworfener Proteine an einer Flüssig‑Fest‑Grenzfläche
Warum diese winzige Welt auf einer Oberfläche wichtig ist
Von Solarzellen bis zu medizinischen Sensoren werden viele künftige Technologien darauf angewiesen sein, präzise Strukturen an den Grenzflächen zwischen biologischen Molekülen und Feststoffen aufzubauen. Diese Studie untersucht, wie maßgeschneiderte Protein‑„Stäbchen“ sich auf Mineraloberflächen in Salzwasser anordnen. Die überraschende Erkenntnis ist, dass das Wasser unmittelbar an der Oberfläche und subtile Asymmetrien im darunterliegenden Kristall die Ausrichtung dieser Proteine vollständig verändern können – manchmal entstehen Muster, die klassische Theorie für unmöglich gehalten hätte.
Proteine entwerfen, die zu einem Kristall passen
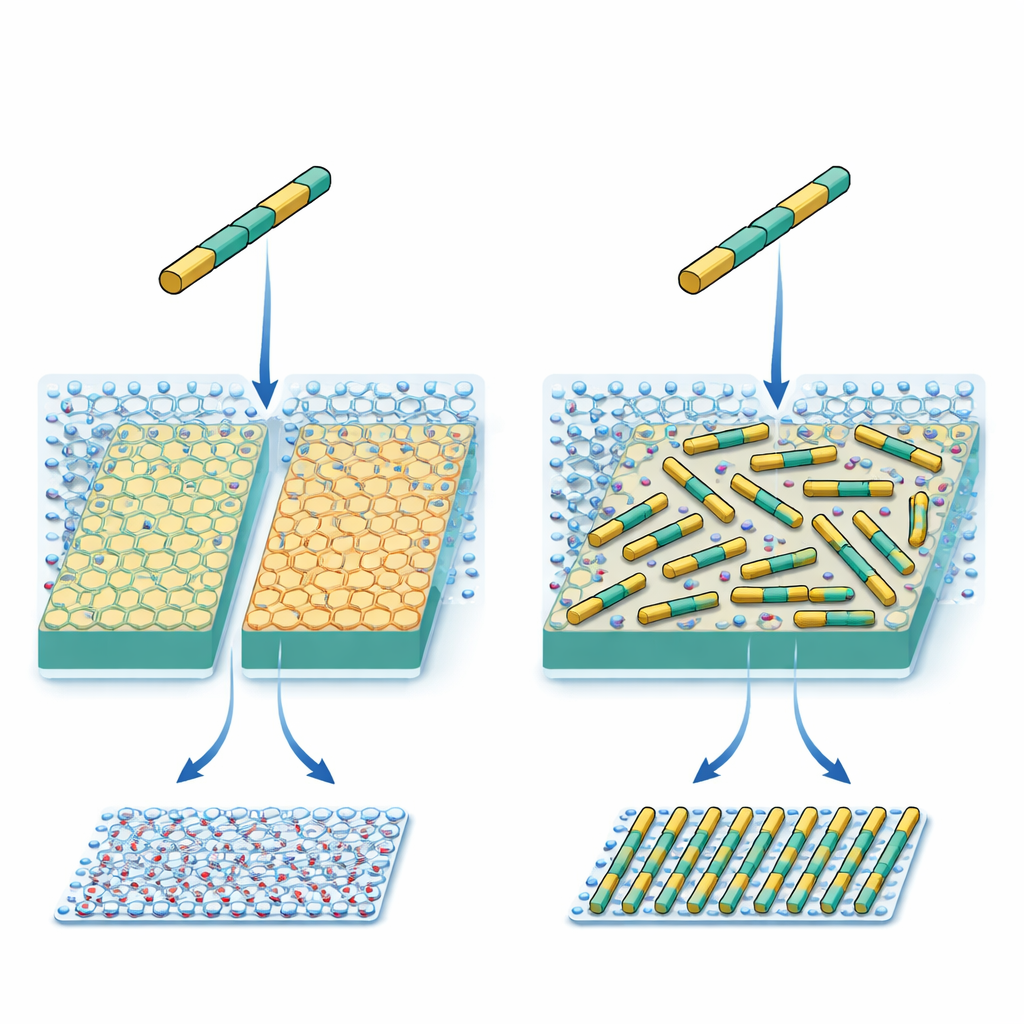
Die Forschenden arbeiten mit einem künstlichen Protein in Form eines kurzen, steifen Stäbchens. Seine Oberflächenchemie und der Abstand geladener Gruppen wurden so gestaltet, dass sie zum Muster der Kaliumionen auf einem häufigen Mineral namens Glimmer (Mica) passen. Im Prinzip sollte jedes Proteinstäbchen drei äquivalente Richtungen auf der Kristalloberfläche bevorzugen, wie die Ausrichtung entlang drei Speichen eines Rades. Frühere Arbeiten zeigten jedoch, dass die Proteine trotz dieser sorgfältigen Gestaltung mehrere unerwartete Muster statt nur des vorgesehenen bildeten. Diese Inkonsistenz deutete darauf hin, dass eine wichtige Kraft in den aktuellen Designregeln fehlt.
Zwei nahezu identische Oberflächen, zwei sehr unterschiedliche Ergebnisse
Um den Vorgang nachzuverfolgen, nutzte das Team hochauflösende, schnelle Rasterkraftmikroskopie (high‑speed AFM), mit der einzelne Proteinstäbchen in Echtzeit beobachtet werden können, während sie sich auf einer Oberfläche bewegen und assemblieren. Sie verglichen zwei eng verwandte Glimmer‑Formen. Beide zeigen dasselbe exponierte Kaliumgitter, doch ihre inneren Atomstrukturen unterscheiden sich leicht, was wiederum beeinflusst, wie sich Wasser in Schichten direkt über der Oberfläche organisiert. Bei moderaten Salzkonzentrationen bildeten die Stäbchen auf beiden Oberflächen einen dichten, aber lokal ungeordneten Teppich mit nur kleinen Bereichen geordneter Ausrichtung. Als die Salzkonzentration jedoch sehr hoch erhöht wurde, spaltete sich das Verhalten: Auf dem einen Glimmertyp blieben die Stäbchen in drei Richtungen ungeordnet, während sie sich auf dem anderen spontan zu langen, parallelen, gleichmäßig beabstandeten Reihen über die gesamte Oberfläche formten.
Wasserschichten und gebrochene Symmetrie
Computergestützte Modellierung der Minerale und des umgebenden Wassers half, diese gespaltene Persönlichkeit zu erklären. Auf der symmetrischeren Glimmerform bewahren die erste und zweite Wasserschicht ein regelmäßiges, hexagonales Muster. Auf der weniger symmetrischen Form brechen interne Atome und eingebettete Gruppen im Kristall jene dreiway‑Symmetrie, und dieses gebrochene Muster wird in die angrenzenden Wasserschichten übertragen, die sich streifenartige Regionen ausbilden. Die Proteine stehen nicht in direktem Kontakt mit blankem Kristall; sie interagieren auch mit diesem strukturierten Wasser. Dadurch wird eine Orientierung der Stäbchen leicht günstiger als die beiden anderen, obwohl die entworfene Protein‑Kristall‑Anpassung eigentlich Gleicheit der drei Richtungen erwarten ließe.
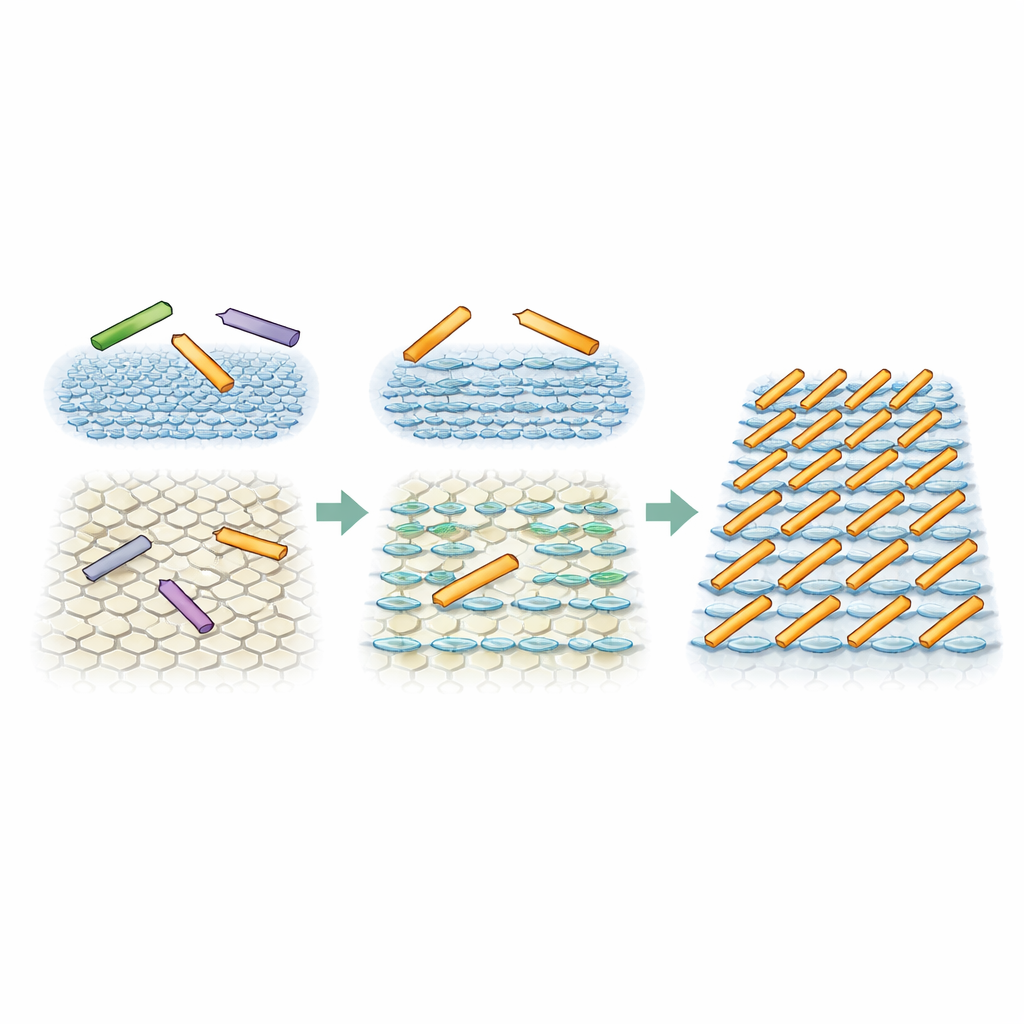
Simulationen zeigen eine unerwartete Phase
Um zu prüfen, ob eine subtile Richtungspräferenz durch die Oberflächenumgebung die beobachteten Muster wirklich erklären kann, führten die Forschenden Monte‑Carlo‑Simulationen mit einfachen starren Rechtecken durch, die die Proteinstäbchen repräsentieren. In einem Simulationssatz waren alle drei Orientierungen gleichermaßen wahrscheinlich und ahmten so die voll symmetrische Oberfläche nach. In diesem Fall blieben die Stäbchen in einem hochdichten, aber ungeordneten Zustand, mit nur vorübergehender oder begrenzter Ausrichtung — genau wie auf einem der Glimmertypen beobachtet. In einem zweiten Satz wurde eine Richtung nur mäßig bevorzugt — etwa doppelt so wahrscheinlich wie die beiden anderen — um den Einfluss der gestreiften Wasserschichten darzustellen. Unter diesen Bedingungen und wenn sich die Stäbchen ausreichend bewegen konnten, entwickelte sich das System auf natürliche Weise zu einem Zustand mit parallelen, gleichmäßig beabstandeten Reihen. Dies ist eine so genannte smektische Phase, die nach etablierten Theorien für nicht wechselwirkende Stäbchen in zwei Dimensionen nicht erwartet würde, doch der kleine richtungsgebende Impuls von der Grenzfläche machte sie stabil.
Neu denken, wie wir bioinspirierte Materialien entwerfen
Kurz gesagt zeigt diese Arbeit, dass fein abgestimmte Protein‑Oberflächenchemie allein nicht ausreicht, um vorherzusagen, wie entworfene Proteine sich auf realen Materialien anordnen. Das Wasser zwischen Protein und Feststoff und die Weise, wie der Kristall Symmetrie subtil bricht, können die Assemblierung in Muster lenken, die im Lehrbuch nicht vorgesehen sind. Durch die Kombination von hochschneller Mikroskopie, maschinellem Lernen zur Quantifizierung von Ordnung und physikbasierten Simulationen skizziert die Studie einen Weg, diese verborgenen Lösungsmittel‑ und Symmetrieeffekte in künftige Protein‑Design‑Werkzeuge zu integrieren. Für alle, die zuverlässige hybride bio‑anorganische Materialien entwickeln wollen, ist die Botschaft klar: Entwerfen Sie nicht nur für das Protein und die Oberfläche, sondern auch für die strukturierte Wasserschicht, die sie verbindet.
Zitation: Yadav Schmid, S., Helfrecht, B., Stegmann, A. et al. Impact of solvent forces and broken symmetry on the assembly of designed proteins at a liquid-solid interface. Nat Commun 17, 2446 (2026). https://doi.org/10.1038/s41467-026-69170-0
Schlüsselwörter: Protein‑Selbstorganisation, Flüssig‑Fest‑Grenzflächen, interfaciale Wasserstruktur, smektische Ordnung, bioinspirierte Materialien