Clear Sky Science · de
Ein multivalenter Adaptermechanismus treibt den Kernimport von Proteasomen an
Wie Zellen ihre Schaltzentralen sauber halten
Im Inneren jeder Zelle fungiert der Zellkern wie eine Kommandozentrale, gefüllt mit DNA und den Proteinen, die steuern, welche Gene ein- oder ausgeschaltet werden. Damit diese Schaltzentrale reibungslos funktioniert, verlassen sich Zellen auf leistungsstarke molekulare „Schredder“ namens Proteasome, die abgenutzte oder fehlfunktionierende Proteine abbauen. Diese Studie zeigt, wie Zellen die überraschend knifflige Aufgabe meistern, diese sperrigen Proteasome zur rechten Zeit durch die engen Tore in den Zellkern zu transportieren.
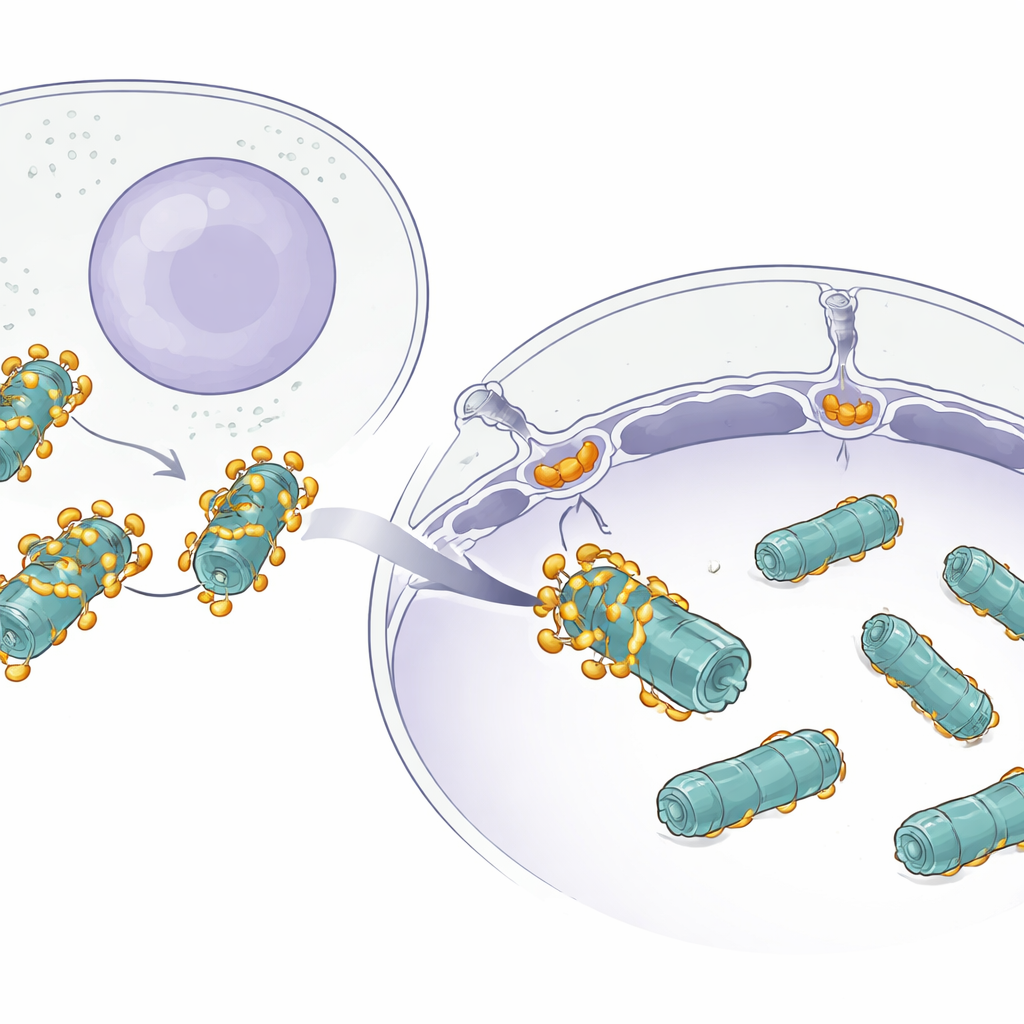
Die Herausforderung, große Maschinen zu bewegen
Viele Proteine pendeln zwischen dem Zytoplasma und dem Zellkern durch riesige Durchgänge in der Kernhülle, den sogenannten Kernporen. Kleine Proteine rutschen leicht hindurch, aber große Maschinen wie Proteasome sind anders: Sie sind massive, fassförmige Komplexe, die aus vielen Teilen aufgebaut sind. Während bereits bekannt war, dass kleine Frachtmoleküle Hilfsproteine namens Importine für den Kernzugang nutzen, war unklar, wie etwas so Großes wie ein Proteasom effizient hindurchkommt, ohne stecken zu bleiben oder verloren zu gehen.
Ein formwandelnder Helfer wird sichtbar
Das Team konzentrierte sich auf ein kleines, bewegliches Protein namens AKIRIN2, von dem frühere Arbeiten gezeigt hatten, dass es für den Kernimport von Proteasomen unverzichtbar ist. Zellen, die ohne AKIRIN2 teilen, können keine Proteasome in den Kern bringen und sterben schnell, weil beschädigte Kernproteine sich ansammeln. Mithilfe einer Kombination von Methoden – darunter ein umfangreicher Mutationsscan, der fast jede Aminosäure in AKIRIN2 veränderte, hochauflösende Kryo-Elektronenmikroskopie zur 3D-Darstellung des Komplexes und sorgfältige biochemische Tests – kartierten die Forscher, welche Regionen von AKIRIN2 wichtig sind und welche Funktion sie haben. Sie entdeckten ein zuvor wenig beachtetes „flügelartiges“ Segment und eine coiled-Coil-Region, die AKIRIN2 zur Dimerisierung (Paarbildung) befähigt; beide spielen Schlüsselrollen beim Greifen von Proteasomen und anderen Partnern.
Ein mehrhändiger Transportgriff entsteht
Die Strukturbilder zeigten, dass mehrere Kopien von AKIRIN2 an einer Seite des Proteasoms wie viele Hände zusammen das gleiche Objekt ergreifen. Jedes AKIRIN2-Paar bindet an spezifische Stellen an der Außenseite des Proteasoms und interagiert gleichzeitig mit unterschiedlichen Importinen. Ein Importin, IPO9, hält AKIRIN2 auf ungewöhnliche Weise, indem es sich um das Protein schmiegt und dabei seine Form ändert, während der Komplex sich zusammensetzt. Andere Importine, ebenfalls paarweise arbeitend, erkennen kurze Kernlokalisationssignale, die AKIRIN2 trägt. Da mehrere AKIRIN2-Moleküle am selben Proteasom sitzen, präsentieren sie zusammen viele dieser Signale gleichzeitig. Dieser multivalente „Henkel“ erlaubt einer Vielzahl von Importinen, gleichzeitig anzudocken und dem riesigen Proteasom genügend Zugkraft zu geben, um durch die Kernpore gezogen zu werden.
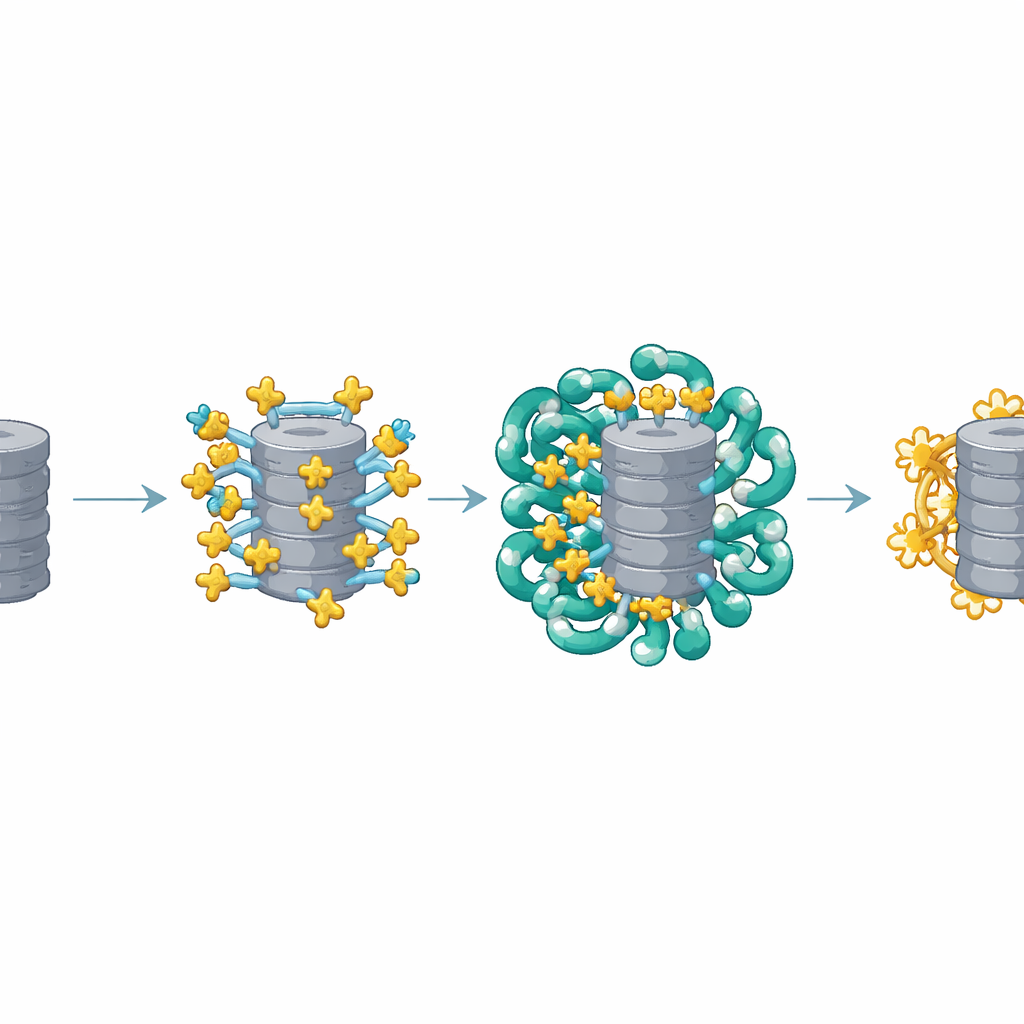
Ein intelligenter Auf- und Abbauzyklus
Rekonstitutionsversuche in einem vereinfachten Reagenzglas-System zeigten, dass Proteasome nur dann effizient in Kerne gelangen, wenn sowohl AKIRIN2 als auch Importine gemeinsam vorhanden sind. Je mehr AKIRIN2, desto stärker und schneller der Import. Sobald sich die Proteasome im Kern befinden, muss die Transportmaschinerie entfernt werden, damit die Proteasome arbeiten können. Hier nutzt die Zelle eine zweistufige Freisetzung. Ein kleiner Schalterprotein namens Ran, in seiner GTP-gebundenen Form, löst die meisten Importine von ihrer Fracht. AKIRIN2 und ein Teil von IPO9 halten zäher fest, aber der Kern hat eine Rückfalloption: Kernlokale Proteasome bauen AKIRIN2 direkt ab, ohne die sonst übliche Ubiquitin-Markierung. Messungen über den Zellzyklus zeigen, dass AKIRIN2 während der Zellteilung am höchsten ist, wenn neue Kerne entstehen, und dann zu Beginn von G1 abfällt, was zu diesem gezielten Aufräumen passt.
Warum das über ein einzelnes Protein hinaus wichtig ist
Zusammen zeigen diese Ergebnisse, dass AKIRIN2 als flexibles Gerüst wirkt, das viele Importine an ein einzelnes Proteasom bringt und so ein schwieriges Transportproblem in eine koordinierte Gruppenleistung verwandelt. Indem Kernlokalisationssignale auf einem Adapter statt auf dem Proteasom selbst gebündelt werden, können Zellen kontrollieren, wann und wie stark große Maschinen in den Kern gelangen, ohne die Maschinen selbst umbauen zu müssen. Ähnliche Adapterstrategien scheinen auch bei anderen großen Proteinassemblies verwendet zu werden, und sogar Viren nutzen verwandte Tricks, um in den Kern einzudringen. Das Verständnis dieser allgemeinen Transportlogik vertieft unser Bild davon, wie Zellen das Proteingleichgewicht in ihrem empfindlichsten Kompartiment aufrechterhalten, und könnte langfristig auf neue Ansätze hinweisen, wenn Proteinabbau oder Kernfunktionen gestört sind.
Zitation: Brunner, H.L., Kalis, R.W., Grundmann, L. et al. A multivalent adaptor mechanism drives the nuclear import of proteasomes. Nat Commun 17, 2359 (2026). https://doi.org/10.1038/s41467-026-69162-0
Schlüsselwörter: nuklearer Transport, Proteasom, AKIRIN2, Importin, Proteinabbau