Clear Sky Science · de
Ein integrierender struktureller Biologieansatz enthüllt die dynamische Organisation des quartären Chaperon‑Komplexes R2SP
Wie Zellen komplexe molekulare Maschinen bauen
In jeder Zelle arbeiten viele Proteine nicht allein – sie müssen sich zu komplexen Maschinen zusammensetzen, bevor sie ihre Funktion erfüllen können. Das Zusammensetzen dieser Bauteile ist entscheidend für gesundes Atmen, Bewegung und sogar Fruchtbarkeit. Diese Arbeit untersucht einen solchen Montagehelfer, eine molekulare „Baucrew“ namens R2SP, und zeigt, wie sie organisiert ist und wie sie funktioniert. Das Verständnis von R2SP ist wichtig, weil bei Ausfall seiner Bestandteile winzige haarartige Strukturen auf Zellen, die Zilien, nicht richtig funktionieren, was zu chronischen Atemwegsproblemen und anderen Erkrankungen führt.
Die zellulären Baucrews R2TP und R2SP
Zellen verlassen sich auf Teams von Helferproteinen, sogenannte Chaperon‑Komplexe, die andere Proteine in die korrekten mehrteiligen Formen führen. Ein lange untersuchtes Team, R2TP, kommt in vielen Geweben vor und hilft beim Aufbau großer Maschinen wie RNA‑Synthese‑Komplexen und DNA‑Schadenssensoren. R2SP ist ein naher Verwandter von R2TP: Beide basieren auf demselben ringförmigen Motor aus zwei Partnerproteinen, RUVBL1 und RUVBL2, die das Energiemolekül ATP verbrauchen. Unterschiedlich sind die Adapter, die Klienten an diesen Motor ankoppeln. R2TP nutzt Adapter namens RPAP3 und PIH1D1, während R2SP SPAG1 und PIH1D2 verwendet. Diese kleinen Teileunterschiede führen zu unterschiedlichen Klientenlisten und verknüpfen R2SP besonders mit dem Aufbau der beweglichen Zilien, die Schleim und Flüssigkeiten über Gewebe fegen.
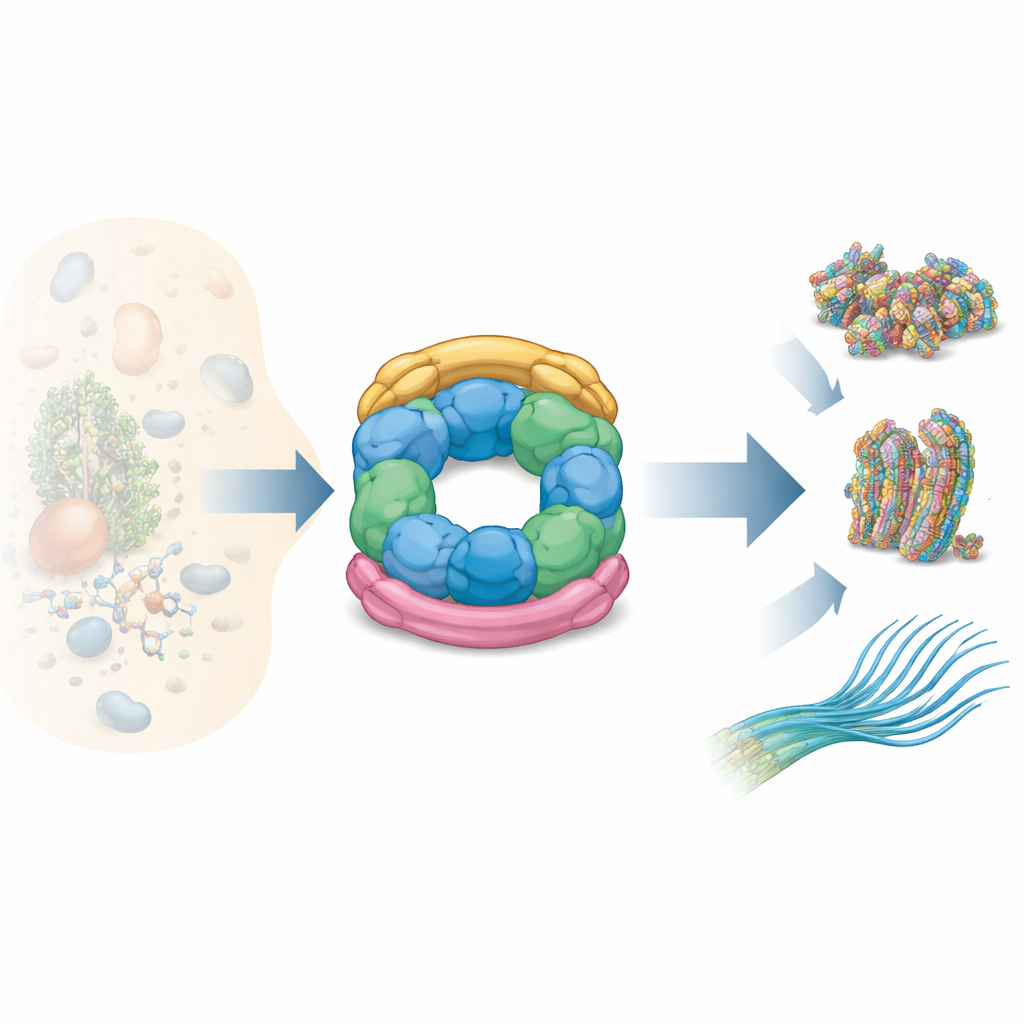
Wie die R2SP‑Teile zusammenpassen
Die Autoren kombinierten mehrere Strukturtechniken – Kernspinresonanz, Kryo‑Elektronenmikroskopie und Querlinkungs‑Massenspektrometrie – mit biochemischen Tests, um die Bauweise von R2SP zu kartieren. Sie zeigten, dass das C‑Terminus‑Ende von SPAG1 den RUVBL1/RUVBL2‑Ring auf eine Weise umgreift, die der Bindung von RPAP3 in R2TP ähnelt, jedoch mit wichtigen Anpassungen in Form und Kontaktstellen. Ein zweiter Adapter, PIH1D2, sitzt unter dem Ring und reicht zugleich bis zu den flexiblen Seitendomänen des Motors. Diese Seitendomänen wirken wie Gelenkarme, die Bewegungen vom ATP‑verbrauchenden Kern zu gebundenen Klienten weiterleiten. Die Daten zeigen, dass SPAG1 und PIH1D2 nicht unabhängig andocken: Sie kooperieren und bilden eine gekoppelte Einheit, die den Ring von oben und unten einspannt und so eine charakteristische dreidimensionale Architektur stabilisiert.
Ein dynamischer Ring, der den Gang wechselt
Über statische Bilder hinaus fragten die Forschenden, wie sich R2SP verhält. Mithilfe von Interaktionsmessungen fanden sie heraus, dass der RUVBL1/RUVBL2‑Motor entweder als einzelner Ring oder als gestapelter Doppelring vorliegen kann. Wenn SPAG1 und PIH1D2 binden, verschiebt sich dieses Gleichgewicht stark zugunsten der Einerringform, die mit bis zu drei Adapterpaaren bestückt werden kann. Gleichzeitig steigern die Adapter deutlich die ATP‑Hydrolyseaktivität des Motors und verändern die Geschwindigkeiten, mit denen ATP‑artige Moleküle an die aktiven Stellen binden und wieder freigesetzt werden. Verglichen mit dem R2TP‑System begünstigen SPAG1 und PIH1D2 andere Schritte bei der Nucleotidfreisetzung, was darauf hindeutet, dass R2SP den Energiekreislauf des Kernmotors auf eigene Weise einstellt. Diese fein gesteuerte Energienutzung dürfte die schrittweise Assemblierung der Klientkomplexe antreiben, die für bewegliche Zilien erforderlich sind.
Eine flexible Plattform zum Aufbau von Zilienbestandteilen
Indem sie alle strukturellen Restriktionen in ein einziges Modell integrierten, schlagen die Autor*innen vor, dass R2SP wie eine flexible, vielarmige Plattform wirkt. Der SPAG1‑Schwanz verankert sich fest oben auf dem Ring, während andere Regionen von SPAG1 und die beiden Domänen von PIH1D2 sich zur offeneren, armähnlichen Seite des Motors erstrecken. An dieser Seite dürften Klientproteine und Helferchaperone wie HSP70 und HSP90 andocken. Da bis zu drei SPAG1–PIH1D2‑Einheiten an einen Ring binden können und die flexiblen Arme ständig in Bewegung sind, ähnelt der gesamte Komplex einem Oktopus, dessen Tentakel mehrere Kliententeile zugleich greifen, koordinieren und weiterreichen können, damit sie zu größeren ziliären Strukturen zusammengesetzt werden.
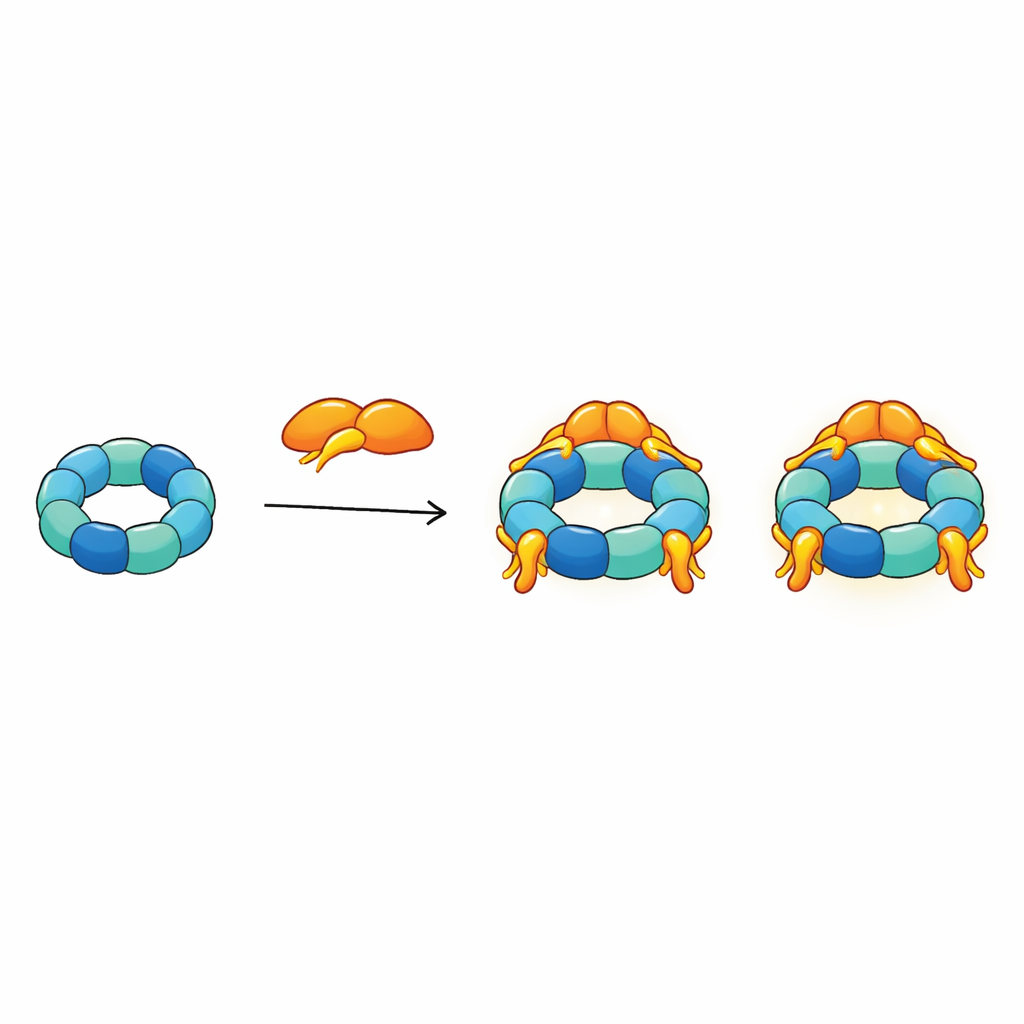
Was das für Gesundheit und Krankheit bedeutet
Für Nicht‑Spezialisten lautet die Kernbotschaft: R2SP ist eine spezialisierte Variante einer allgemeinen zellulären Bau‑Maschine, umverdrahtet durch den Austausch von nur zwei Adapterproteinen. Dieser Austausch verändert sowohl die Kontrolle des zentralen Motors als auch die Positionierung der Klienten und erklärt, warum R2SP sich auf den Aufbau von Bestandteilen beweglicher Zilien konzentriert, während R2TP anderen zellulären Fabriken dient. Fehler in SPAG1 sind bereits als Ursache der primären ziliären Dyskinesie bekannt, einer Erkrankung, die durch wiederkehrende Infektionen und Fruchtbarkeitsprobleme gekennzeichnet ist. Indem diese Studie die detaillierte Anordnung und Arbeitsprinzipien von R2SP offenlegt, legt sie den Grundstein dafür zu verstehen, wie bestimmte Mutationen die Zilienassemblierung stören und möglicherweise künftig gezielte Behandlungen ermöglichen, die diese zentrale molekulare Baucrew wiederherstellen oder modulieren.
Zitation: Santo, P.E., Chagot, ME., Gizardin-Fredon, H. et al. An integrative structural biology approach reveals the dynamic organization of the R2SP quaternary chaperone complex. Nat Commun 17, 2605 (2026). https://doi.org/10.1038/s41467-026-69157-x
Schlüsselwörter: molekulare Chaperone, Protein‑Komplex‑Assemblierung, bewegliche Zilien, strukturelle Biologie, RUVBL1 RUVBL2