Clear Sky Science · de
Strukturelle Grundlage der TACO1-vermittelten effizienten mitochondrialen Translation
Die Kraftwerke der Zelle reibungslos am Laufen halten
Mitochondrien werden oft als die Kraftwerke unserer Zellen bezeichnet, weil sie das Energiemolekül ATP erzeugen. Dafür müssen sie eine kleine, aber unverzichtbare Gruppe von Proteinen herstellen, und zwar an ihren eigenen spezialisierten Proteinfabriken, den Mitoribosomen. Diese Studie zeigt, wie ein wenig bekanntes Hilfsprotein, TACO1, diese Fabriken feinjustiert, damit sie besonders dann zuverlässig weiterarbeiten können, wenn sie auf besonders „ungeschickte“ Abschnitte in der Proteinsequenz stoßen, die dazu neigen, die Maschinerie zum Stillstand zu bringen.
Energiefabriken mit eigener Hardware
Anders als die meisten Proteinbiosyntheseprozesse, die im wässrigen Zellinneren ablaufen, erfolgt die mitochondriale Proteinsynthese auf Mitoribosomen, die an der inneren Membran der Mitochondrien verankert sind — derselben Membran, die viele energieerzeugende Enzyme beherbergt. Mithilfe modernster Kryo‑Elektronenmikroskopie an intakten menschlichen Mitochondrien erstellten die Autorinnen und Autoren nahezu atomare Momentaufnahmen dieser Mitoribosomen in ihrer natürlichen Umgebung. Sie beobachteten, dass alle erfassten Mitoribosomen an die innere Membran gebunden waren und so positioniert, dass neu entstehende Proteinketten direkt in eine Membraninsertase gespeist werden konnten, eine Art molekularer Schlitz, der frische Proteine in die Membran einführt, wo sie für die Energieproduktion benötigt werden. 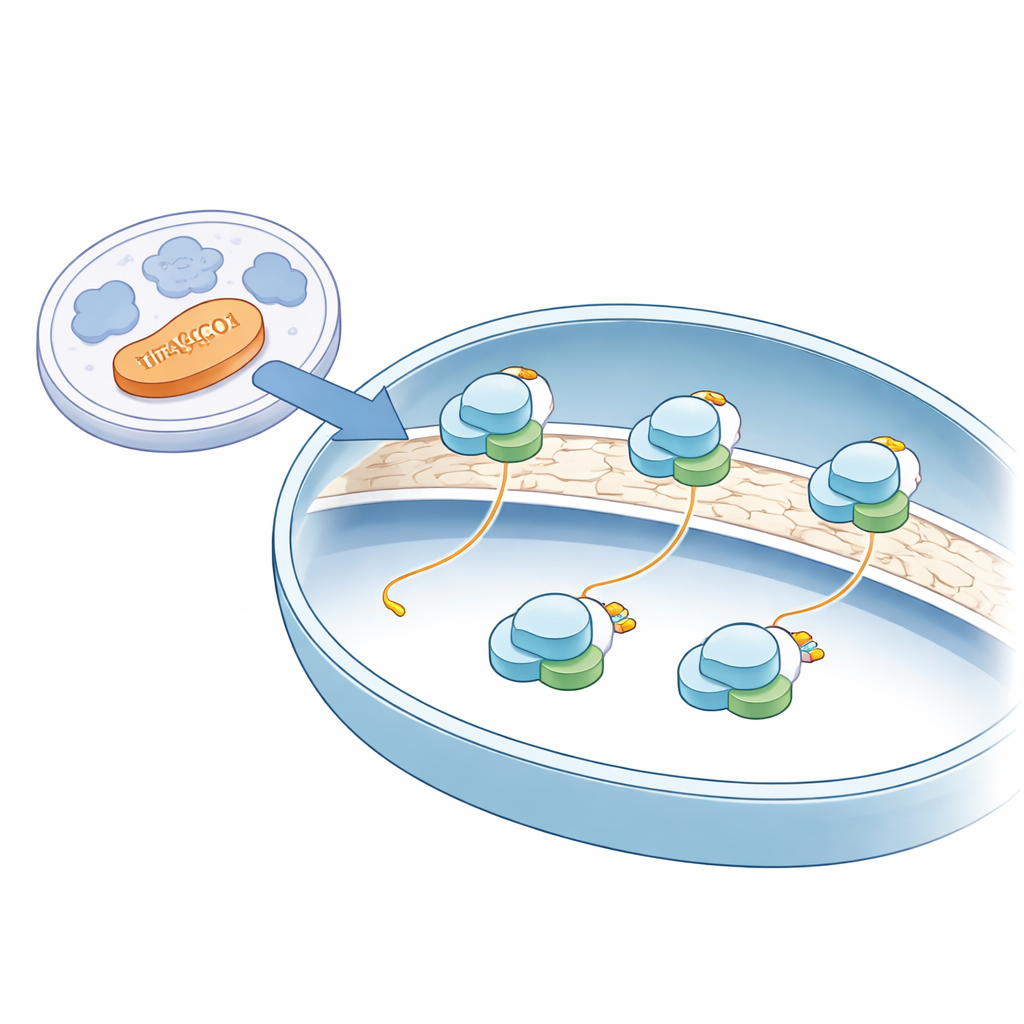
Ein verborgener Helfer tritt in den Fokus
Mitten zwischen Ribosomenbestandteilen, RNA‑Strängen und wachsenden Proteinketten bemerkten die Forschenden eine zusätzliche Dichtezone, die in früheren, stärker künstlichen Präparaten nie gesehen worden war. Durch sorgfältige Verfeinerung ihrer Karten und den Vergleich von Formen mit vorhergesagten Proteinstrukturen identifizierten sie diese unbekannte Komponente als TACO1, ein Protein, das bereits mit menschlichen mitochondriellen Erkrankungen in Verbindung gebracht wurde, dessen physikalische Rolle aber bislang unklar geblieben war. Die Bilder zeigten, dass TACO1 sich neben dem Bereich des Ribosoms positioniert, an dem die nächste Aminosäure‑tragende tRNA (die A‑Stelle) ankommt, und Kontakte sowohl zu ribosomaler RNA als auch zu mehreren Ribosomenproteinen herstellt. Diese Lage erlaubt es TACO1, fast wie eine Stütze zu wirken und die ankommende tRNA zu stabilisieren, während das Ribosom eine neue Bindung bildet, um die Proteinkette zu verlängern.
Verkehrsstaus auf der Proteinfertigungsstraße verhindern
Der Proteinaufbau verläuft zyklisch: ein Elongationsfaktor (mtEF‑Tu) liefert eine beladene tRNA, das Ribosom prüft und verwendet sie, und der Faktor verlässt das Ribosom, damit der nächste Schritt stattfinden kann. Die Autorinnen und Autoren fanden heraus, dass TACO1 ungefähr in demselben Bereich bindet, den auch mtEF‑Tu verwendet, und dass beide Faktoren nicht gleichzeitig das Ribosom besetzen können. In normalen Zellen erschienen viele Mitoribosomen in einem Zustand, in dem die neue tRNA vollständig eingebracht ist und die Elongation voranschreitet. In Mitochondrien von Zellen ohne TACO1 beobachtete das Team dagegen eine Anhäufung von Ribosomen, die in einem früheren Zustand feststeckten, in dem mtEF‑Tu noch gebunden ist und die neue tRNA sich nicht vollständig eingereiht hat. Biochemische Experimente bestätigten, dass mtEF‑Tu ohne TACO1 länger auf aktiv translierenden Ribosomen verweilt und die große und kleine Untereinheit eher auseinanderdriften — Anzeichen für gestoppte oder fehlgeschlagene Translation. 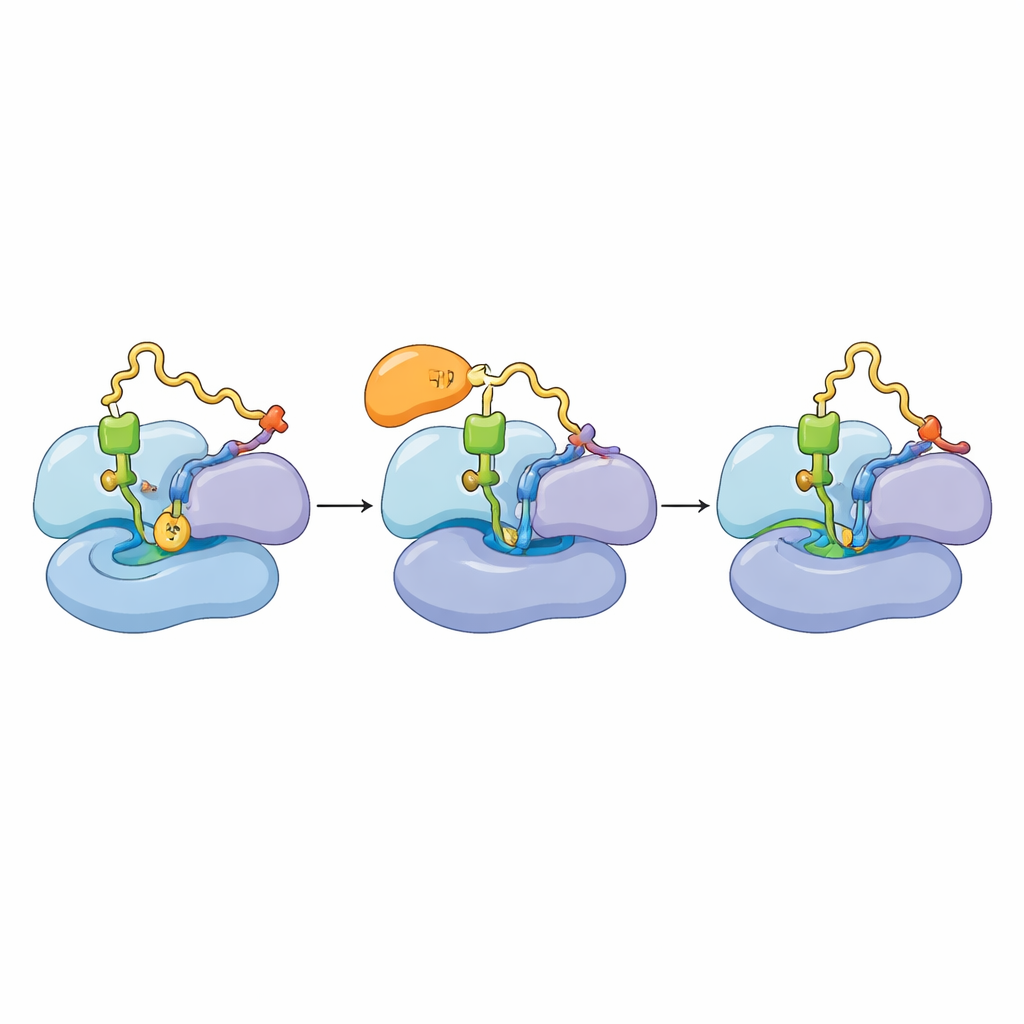
Warum bestimmte Proteinstrecken so problematisch sind
Eine der wichtigsten Aufgaben von TACO1 scheint zu sein, dem Ribosom beim Übersetzen von Abschnitten mit vielen Prolin‑Aminosäuren zu helfen, die die Bindungsbildung natürlicherweise verlangsamen, weil Prolin eine starre Ringstruktur besitzt. Frühere Arbeiten zeigten, dass TACO1 entscheidend für die Produktion von Cytochrom‑c‑Oxidase‑Untereinheit 1 ist, einem zentralen Bestandteil der Energieelektronenkette, der ein seltenes Triple‑Prolin‑Motiv enthält, und dass sein Verlust zum Zusammenbruch dieses Energiekomplexes und zu einer menschlichen Hirnerkrankung namens Leigh‑Syndrom führt. In Bakterien und im zytoplasmatischen Proteinsynthesesystem der Zelle übernehmen andere Hilfsfaktoren eine ähnliche Anti‑Stall‑Funktion, doch mitochondrien fehlen diese konventionellen Faktoren. Die neuen strukturellen Daten zeigen, dass TACO1 als mitochondrien‑spezifische Lösung entstanden ist: Indem es mtEF‑Tu zur Seite drängt, die ankommende tRNA stabilisiert und die Bindungsbildung unterstützt, hilft es dem Mitoribosom, diese schwierigen Sequenzabschnitte zu überwinden, statt stehenzubleiben.
Eine alte Strategie mit modernen Gesundheitsfolgen
Über den Menschen hinaus findet man verwandte Proteine zu TACO1 in vielen Bakterien und anderen Organismen, und einige dieser bakteriellen Formen können ebenfalls Ribosomen‑Staus auflösen. Diese Konservierung legt nahe, dass die Nutzung eines TACO1‑ähnlichen Faktors zur Rettung langsamer oder blockierter Ribosomen eine alte Strategie ist, um die Proteinsynthese effizient zu halten. Für den Menschen liefert die Arbeit eine konkrete, visuelle Erklärung dafür, warum Mutationen in TACO1 die Energieproduktion und das Nervensystem so schwer schädigen können, und sie deutet an, dass die Manipulation von TACO1 oder verwandten Proteinen eines Tages Wege eröffnen könnte, die mitochondriale Translation zu beeinflussen — sei es zur Behandlung mitochondrialer Erkrankungen oder zum gezielten Angriff auf schädliche Bakterien, die auf ähnliche Stau‑Auflösesysteme angewiesen sind.
Zitation: Wang, S., Brischigliaro, M., Zhang, Y. et al. Structural basis of TACO1-mediated efficient mitochondrial translation. Nat Commun 17, 2521 (2026). https://doi.org/10.1038/s41467-026-69156-y
Schlüsselwörter: mitochondriale Translation, TACO1, Mitoribosom, Ribosomen-Stau, Leigh-Syndrom