Clear Sky Science · de
Kombinierte Bakteriophagen- und Antibiotikatherapie bei refraktärer peritonealer Dialyse-assoziierter Peritonitis verursacht durch Klebsiella pneumoniae
Warum diese Infektionsgeschichte wichtig ist
Menschen mit Nierenversagen sind häufig auf Peritonealdialyse angewiesen, eine häusliche Behandlung, die das Blut sanft über die Bauchfell‑Höhle reinigt. Eine schwere Komplikation dieser Therapie ist Peritonitis – eine Infektion im Bauchraum –, die schmerzhaft, schwer zu behandeln und potenziell lebensbedrohlich sein kann. Da manche Bakterien gegenüber Standardmedikamenten zunehmend schwerer zu besiegen sind, suchen Ärztinnen und Ärzte nach neuen Wegen, diese vulnerablen Patientengruppen zu schützen. Dieser Bericht beschreibt, wie ein Team aus Klinikern und Forschenden ein Bakterien angreifendes Virus zusammen mit Antibiotika einsetzte, um eine hartnäckige Infektion bei einem Peritonealdialyse-Patienten erfolgreich zu behandeln, und was sie durch engmaschige Beobachtung seines Ansprechens gelernt haben.
Eine schwer behandelbare Bauchinfektion
Der Patient war ein 71‑jähriger Mann mit Nierenversagen, der mittels kontinuierlicher ambulanter Peritonealdialyse versorgt wurde. Über mehrere Jahre hatte er wiederholt Peritonitiden, zuerst verursacht durch übliche Hautkeime, die am Kunststoffkatheter haften und einen schleimigen Film, ein Biofilm, bilden können. Um diesen Kreislauf zu durchbrechen, ersetzten die Ärzte seinen Peritonealdialysekatheter in einem einzigen Eingriff, sobald das Dialysat wieder klar ablief – eine Strategie, die als simultaner Katheterwechsel bezeichnet wird. Kurz darauf entwickelte er jedoch eine neue und besorgniserregendere Infektion: die Dialysatflüssigkeit wurde erneut trüb, und Untersuchungen ergaben Klebsiella pneumoniae, ein gramnegatives Bakterium, das mit schwereren Verläufen, einem höheren Risiko für den Verlust des Katheters und einer erhöhten Sterblichkeit bei Dialysepatienten in Verbindung gebracht wird.
Wenn Antibiotika nicht ausreichen
Laboruntersuchungen zeigten, dass dieser Klebsiella‑Stamm gegenüber einigen starken Antibiotika weiterhin empfindlich war, darunter Amikacin und Imipenem. Die Ärzte verabreichten diese Wirkstoffe zwei Wochen lang direkt in die Bauchhöhle, kombiniert mit unterstützenden Medikamenten und einer Tablette zur Vorbeugung gegen Pilzinfektionen. Trotz dieser Maßnahmen blieb das Dialysat trüb und die Zahl der weißen Blutkörperchen – Immunzellen, die bei Infektionen stark ansteigen – war weiterhin sehr hoch. Die Bakterien wuchsen weiterhin in Kultur, womit die Definition einer refraktären Peritonitis erfüllt war; Leitlinien empfehlen in diesem Fall üblicherweise die Entfernung des Katheters und die Umstellung des Patienten auf Hämodialyse. Da regelmäßige Fahrten zur Hämodialyse für diesen Patienten äußerst schwierig gewesen wären, prüfte das Team eine experimentelle Alternative: eine gezielte Bakteriophagentherapie gegen seine Klebsiella‑Isolat.
Viren nutzen, die Bakterien jagen
Bakteriophagen, kurz Phagen, sind Viren, die Bakterien infizieren und abtöten, aber keine menschlichen Zellen angreifen. Aus einer großen Phagenbibliothek wählten die Forschenden zwei Phagen aus, die den Klebsiella‑Stamm des Patienten erkannten. Die genetische Sequenzierung bestätigte, dass diese Phagen rein lytisch waren – also darauf ausgelegt, ihre bakteriellen Wirte zu zerstören und nicht mit ihnen zu koexistieren – und dass sie keine Gene trugen, die mit Toxinen oder Antibiotikaresistenzen assoziiert sind. Im Labor tötete ein Phage allein die Bakterien zwar schnell, ließ jedoch innerhalb weniger Stunden resistente Überlebende entstehen. Der zweite Phage konnte diese Entkommenen beseitigen. Zusammen als Cocktail angewendet unterdrückten sie das bakterielle Wachstum für einen vollen Tag oder länger. In Kombination mit niedrigen Dosen von Imipenem beseitigte der Phagencocktail die Bakterien stärker als jede der Behandlungen allein und zeigte damit eine deutliche Synergie zwischen der Virusmischung und dem Antibiotikum.
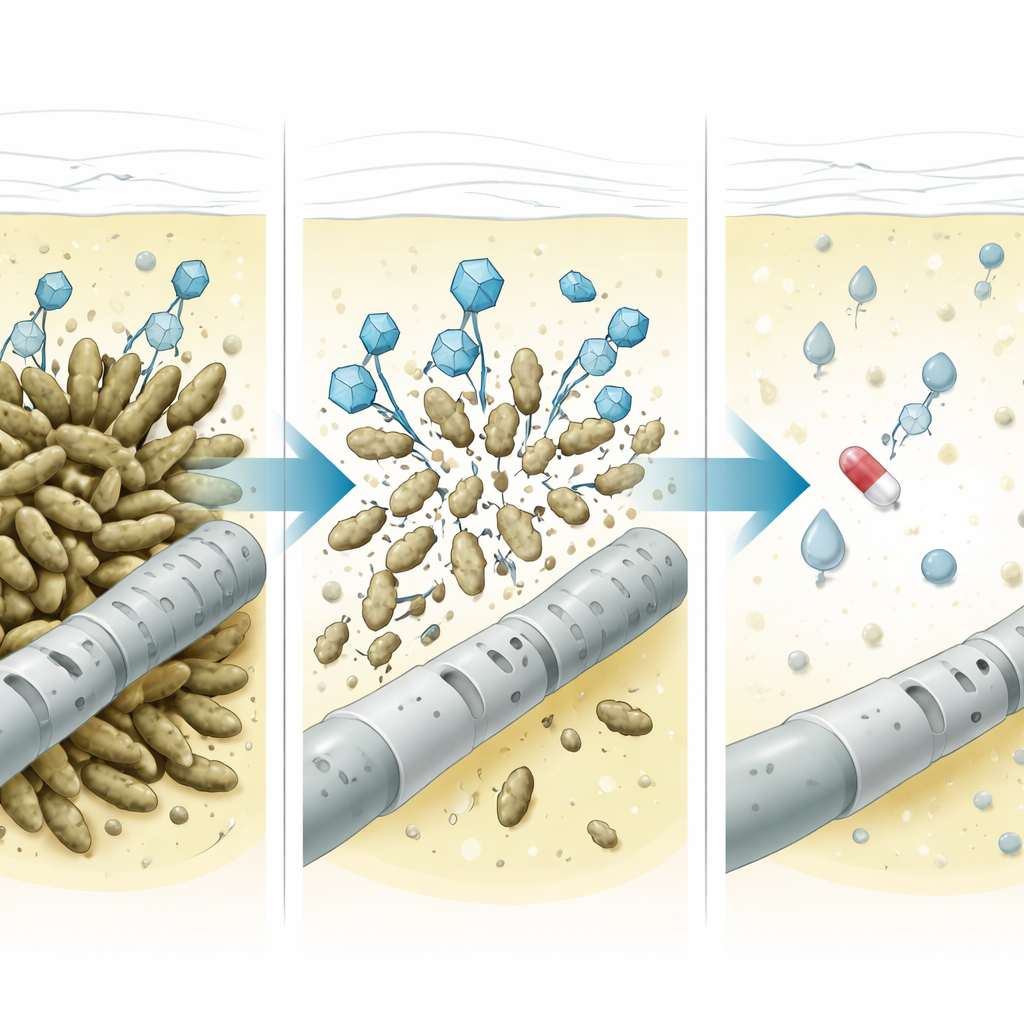
Was im Bauchraum geschah
Die Ärzte gaben den Phagencocktail zwei Tage pro Tag (zweimal täglich) für drei Tage in die Peritonealhöhle ein, während sie die intraperitoneale Gabe von Imipenem und orale Fluconazol‑Prophylaxe fortsetzten. Anschließend verfolgten sie sorgfältig mehrere Parameter im Drainat. Die weißen Blutkörperchen schwankten zunächst, sackten dann aber schnell ab, und Klebsiella wuchs nicht mehr in Kultur. Interleukin‑6, ein Protein, das lokale Entzündung widerspiegelt, war anfangs sehr hoch, stieg kurzzeitig während der Phagenbehandlung – wahrscheinlich als Folge des Zerfalls der Bakterien und der Freisetzung deren Inhalts – und fiel dann stetig auf niedrige Werte. Lipopolysaccharid, ein Bestandteil der Außenhülle gramnegativer Bakterien und ein starker Auslöser von Immunreaktionen, zeigte ein ähnliches Muster: hoch vor der Therapie, ein kleiner Anstieg während des bakteriellen Zerfalls, dann ein Abfall auf nicht nachweisbare Werte. Das Team suchte auch nach neutralisierenden Antikörpern – Immunmolekülen, die Phagen blockieren könnten – und fand im Peritonealflüssigkeit keine relevante Zunahme. Die Phagenkonzentrationen selbst sanken innerhalb eines Tages um etwa zehntausendfach und waren nach 48 Stunden nicht mehr nachweisbar, was mit dem Szenario übereinstimmt, dass die Viren ihre Wirkung taten und anschließend verschwanden.
Anhaltspunkte aus anderen Fällen
Um diese Einzelerfahrung einzuordnen, werteten die Autorinnen und Autoren alle veröffentlichten Fälle von menschlichen Infektionen durch Klebsiella pneumoniae aus, die mit Phagen behandelt worden waren. Sie fanden 14 Patienten weltweit mit Infektionen in den Harnwegen, Lungen, Knochen, Gelenken und Hirnhäuten. Bei 13 dieser Patienten besserten sich die Symptome oder die Infektion klärte sich, nur ein Fall sprach nicht an. Die meisten Patienten erhielten Phagen zusammen mit Antibiotika, wenige wurden ausschließlich mit Phagen behandelt. In diesen Berichten traten schwere Nebenwirkungen selten auf, was die Vorstellung stützt, dass sorgfältig hergestellte Phagentherapien bei enger Überwachung sicher eingesetzt werden können.
Was das für die zukünftige Versorgung bedeuten könnte
Nach drei Wochen kombinierter Phagen‑ und Antibiotikatherapie heilte die abdominale Infektion des Patienten aus, seine Entzündungsmarker normalisierten sich und er wurde ohne weitere Antibiotikagabe entlassen. Bei der Nachuntersuchung nach einem Monat zeigte sich kein Rückfall, und er konnte weiterhin peritoneal dialysiert werden. Dieser einzelne Fall kann nicht beweisen, dass Phagentherapie bei jedem Dialysepatienten mit refraktärer Peritonitis wirkt; die Autorinnen und Autoren betonen die Notwendigkeit größerer Studien, besserer Erregernachweismethoden und einer vertieften Untersuchung, wie Phagen mit dem Immunsystem interagieren. Dennoch zeigt ihre Erfahrung, dass personalisierte Phagencocktails, durchdacht kombiniert mit wirksamen Antibiotika, eine wertvolle Rettungsoption sein können, wenn Standardbehandlungen versagen und die Entfernung des Katheters die Lebensqualität eines Patienten stark beeinträchtigen würde.
Zitation: Yang, X., Wu, N., Jiang, X. et al. Combined bacteriophage and antibiotic therapy for refractory peritoneal dialysis-related peritonitis caused by Klebsiella pneumoniae. Nat Commun 17, 2468 (2026). https://doi.org/10.1038/s41467-026-69154-0
Schlüsselwörter: Phagentherapie, Peritonealdialyse, Klebsiella pneumoniae, Antibiotikaresistenz, Peritonitis