Clear Sky Science · de
Molekularer Mechanismus des Phosphatimports durch den bakteriellen PstSCAB-Transporter
Warum winzige Nährstoffe für uns wichtig sind
Jede lebende Zelle, von menschlichen Neuronen bis zu Bodenbakterien, ist auf Phosphor angewiesen. Dieses Element hilft, Energie zu speichern, DNA aufzubauen und Zellmembranen intakt zu halten. In der Umwelt ist jedoch verfügbares Phosphat — die Form von Phosphor, die Zellen tatsächlich aufnehmen können — oft knapp. Viele krankheitserregende Bakterien sind auf eine hocheffiziente molekulare Maschine angewiesen, den PstSCAB-Transporter, um Phosphat bei Mangel aufzuspüren. Zu verstehen, wie diese Maschine genau arbeitet, ist nicht nur eine Frage der Grundlagenforschung; es könnte Wege eröffnen, Infektionen zu schwächen, indem man Bakterien diesen lebenswichtigen Nährstoff vorenthält.
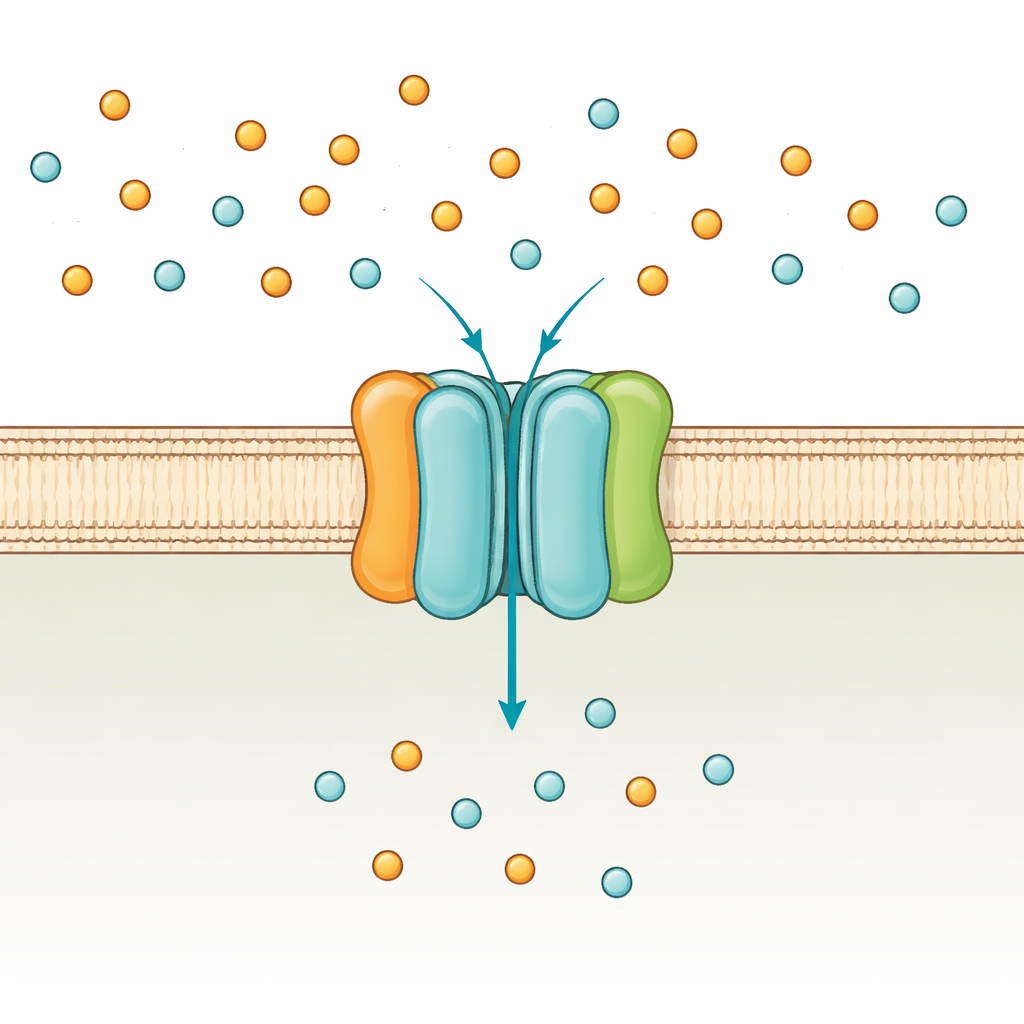
Der Phosphat-Wächter der Zelle
Bakterien wie Escherichia coli nutzen zwei Hauptwege zur Phosphataufnahme: ein niedrig-affines System, das funktioniert, wenn Phosphat reichlich vorhanden ist, und das hoch-affine PstSCAB-System, das bei Mangel aktiviert wird. PstSCAB sitzt in der Zellmembran und wird von ATP angetrieben, der universellen Energiewährung der Zelle. Es besteht aus fünf Teilen: zwei membranintegrierten Untereinheiten (PstA und PstC), die den Durchgang bilden, einem löslichen „Fänger“-Protein außerhalb der Membran (PstS), das Phosphat greift, und einem Paar interner Untereinheiten (PstB), die ATP verbrennen, um den Transport anzutreiben. Da dieses System auch viele Gene steuert, die mit bakterieller Virulenz verknüpft sind, können Mutationen in PstSCAB Krankheitserreger schwächen, die Harnwegsinfektionen, Sepsis bei Nutztieren und Tuberkulose verursachen.
Die Maschine in Aktion einfangen
Bisher hatten Wissenschaftler nur Teilansichten von PstSCAB, meist nur vom Fängerprotein PstS allein. In dieser Studie verwendeten die Forscher hochauflösende Kryo-Elektronenmikroskopie, um den gesamten Transporter in mehreren Schlüsselphasen seines Arbeitszyklus zu visualisieren. Sie rekonstituierten die bakteriellen Proteine in künstliche Membran-„Nanodiscs“ und froren sie so schnell ein, dass die Moleküle inmitten ihrer Bewegung eingefangen wurden. Durch gezielte Modifikationen der Proteine und das Hinzufügen oder Weglassen von ATP erhielten sie Strukturen von drei Hauptzuständen: eine ruhende, nach innen geöffnete Form ohne angedockten Fänger, einen Prätranslokationszustand, in dem Phosphat-beladenes PstS an den Membrankomplex andockt, und ein ATP-gebundenes katalytisches Zwischenprodukt, in dem Phosphat im Inneren des Transporters gehalten wird.
Wie Formänderungen Phosphat bewegen
Die Aufnahmen zeigen, wie koordinierte Formänderungen Phosphat von außen nach innen bewegen. Im Ruhezustand öffnet sich der von PstA und PstC gebildete Durchgang nur zur Zellinnenseite; die Außenseite ist durch eine Reihe von „Tor“-Resten verschlossen, sodass Phosphat noch nicht von außen eindringen kann. Wenn das Phosphat-beladene PstS im Prätranslokationszustand andockt, schmiegt es sich zwischen flexible Schleifen von PstA und PstC, doch auffällig ist, dass die Membranuntereinheiten kaum ihre Form ändern. Die eigentliche Verschiebung erfolgt, wenn PstS beginnt, seine beiden Lappen zu öffnen, um Phosphat freizugeben, und gleichzeitig sich die beiden PstB-Untereinheiten zusammenschwingen, um ATP zu binden. Diese ATP-Bindung klemmt PstB zu einem Dimer zusammen und zieht an verbindenden Helices in PstA und PstC, wodurch der gesamte Kanal in eine nach außen gerichtete Konformation geklappt wird, die eine spezifische Phosphatbindungs-Tasche der Außenseite öffnet.
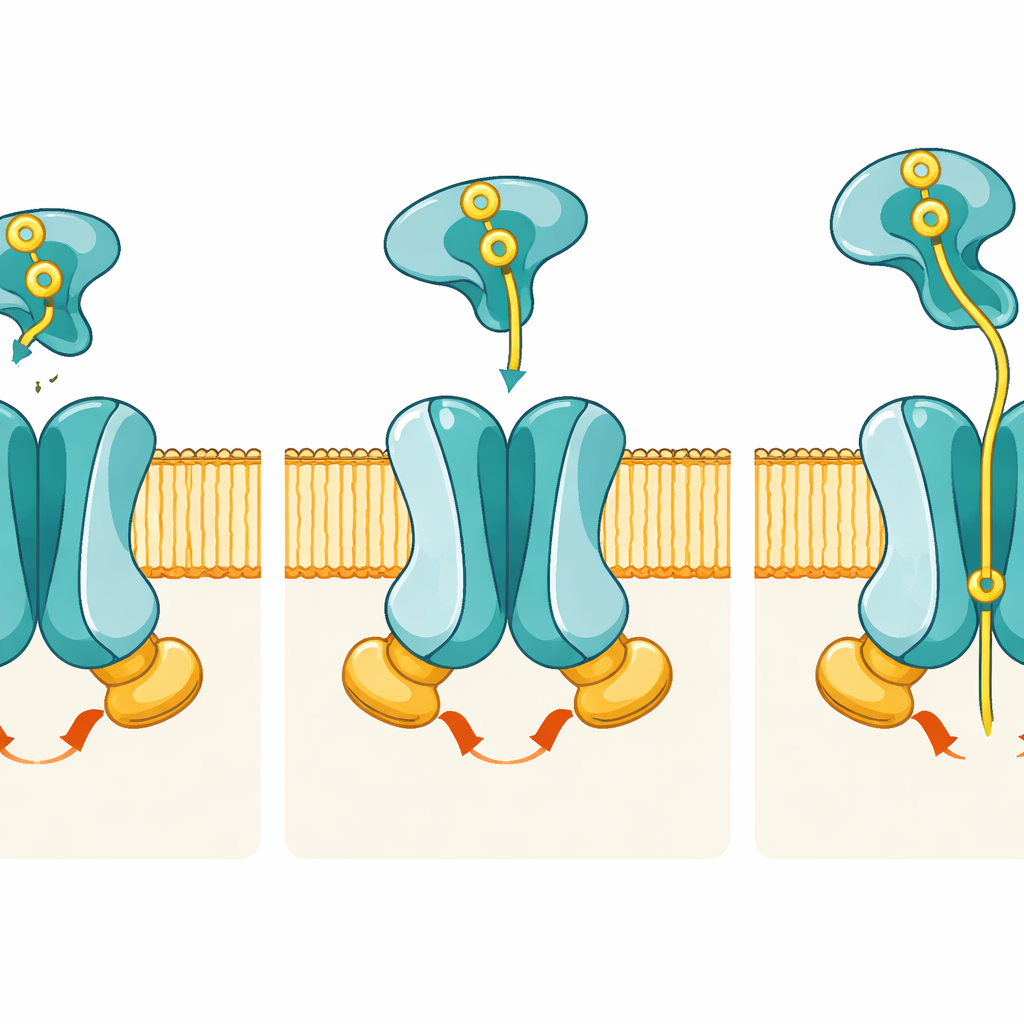
Eine maßgeschneiderte Tasche für Phosphat
In der nach außen gerichteten, ATP-gebundenen Struktur finden die Autoren eine Dichte in der Mitte der Membranregion, die zu einem Phosphat-Ion passt. Dieses Ion wird von positiv geladenen Aminosäuren gehalten — insbesondere zwei Argininen, je eine von PstA und eine von PstC — die wie molekulare Fingerspitzen das negativ geladene Phosphat umgreifen. Computersimulationen zeigen, dass Phosphat in dieser Tasche über Mikrosekunden stabil gebunden bleibt, und genetische Experimente bestätigen ihre Bedeutung: Wenn diese Schlüsselreste mutiert werden, verbrennt der Transporter zwar weiterhin ATP, nimmt Phosphat aber nur sehr schlecht auf. Diese Trennung von „wo Energie verbraucht wird“ und „wo die Fracht erkannt wird“ unterstreicht, wie präzise die Maschine auf Phosphat abgestimmt ist.
Von Strukturaufnahmen zur medizinischen Aussicht
Zusammen zeichnen die Strukturen und ergänzenden biochemischen Tests einen vollständigen Zyklus nach: PstS fängt Phosphat außen ein, dockt an den nach innen gerichteten Transporter an und löst dann — gekoppelt an ATP-Bindung und -Spaltung durch PstB — eine Umklappung aus, die Phosphat in die Membrantasche und schließlich ins Zellinnere überführt. Nach der Hydrolyse von ATP entspannt sich die Maschine wieder in den Ruhezustand und ist bereit für eine neue Runde. Für den fachfremden Beobachter ist die Kernbotschaft, dass wir nun einen atomaren Bauplan dafür haben, wie viele Bakterien in phosphatearmen Umgebungen überleben und ihre Virulenz regulieren. Diese detaillierte Karte kann die Entwicklung von Wirkstoffen, Antikörpern oder Peptiden leiten, die den Transporter blockieren oder sein Fängerprotein hemmen und so ein lebenswichtiges Nährtor in ein verwundbares therapeutisches Ziel verwandeln.
Zitation: Xiao, H., Li, S., Qi, R. et al. Molecular mechanism of phosphate import by the bacterial PstSCAB transporter. Nat Commun 17, 2294 (2026). https://doi.org/10.1038/s41467-026-69153-1
Schlüsselwörter: Phosphattransport, bakterielle Nährstoffaufnahme, ABC-Transporter, PstSCAB, antibakterielle Ziele