Clear Sky Science · de
Ein per mRNA übermitteltes Konsensus-Allergen löst eine neutralisierende IgG-Antwort gegen Nahrungs- und Pollenallergene aus
Warum viele Allergien gleichzeitig behandelbar sein könnten
Für Menschen, die nicht nur auf ein Nahrungsmittel oder Pollen, sondern auf viele verwandte Auslöser reagieren, fühlt sich der Alltag oft wie ein Minenfeld an. Ein Bissen von einer Pfirsich, eine Handvoll Nüsse oder eine Frühlingsbrise voller Pollen kann dieselbe gefährliche Reaktion auslösen. Diese Studie untersucht einen neuen Ansatz, um solche Kreuzallergien mit einem einzigen, konstruierten Protein zu beruhigen, das per mRNA geliefert wird — derselben Basistechnologie, die in einigen COVID-19-Impfstoffen verwendet wird — und das Immunsystem darauf zu trainieren, eine ganze Familie verwandter Allergene gleichzeitig zu blockieren.
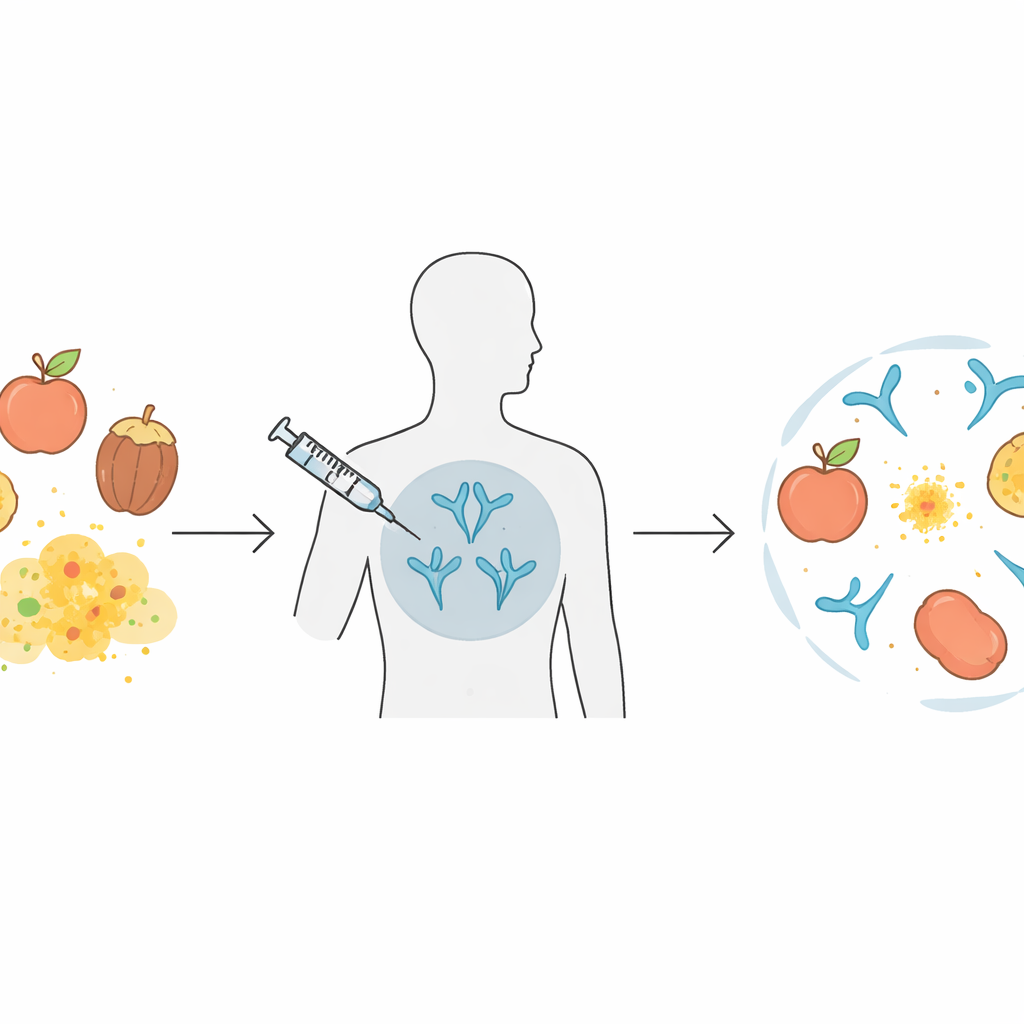
Wie aus einer Allergie viele werden können
Viele Menschen mit Nahrungsmittelallergien sind nicht nur gegen einen Stoff empfindlich. Sie können auf mehrere Früchte, Nüsse, Gemüse und sogar Pollen reagieren, weil diese Quellen ähnliche Proteine teilen. In dieser Arbeit liegt der Fokus auf einer Familie pflanzlicher Proteine, den sogenannten nicht-spezifischen Lipidtransferproteinen (nsLTPs), die in Lebensmitteln wie Pfirsichen, Äpfeln, Nüssen und in Pollen bestimmter Bäume und Unkräuter verbreitet sind. In mediterranen Ländern kann das sogenannte „LTP-Syndrom“ Patienten dazu bringen, auf eine breite Liste von Lebensmitteln zu reagieren, teils mit lebensbedrohlicher Anaphylaxie. Aktuelle Allergie-Immuntherapien zielen üblicherweise auf Extrakte aus einer einzigen Quelle ab und erfassen möglicherweise nicht alle kreuzreaktiven Verwandten, was lange Behandlungsdauern und unvollständigen Schutz bedeutet.
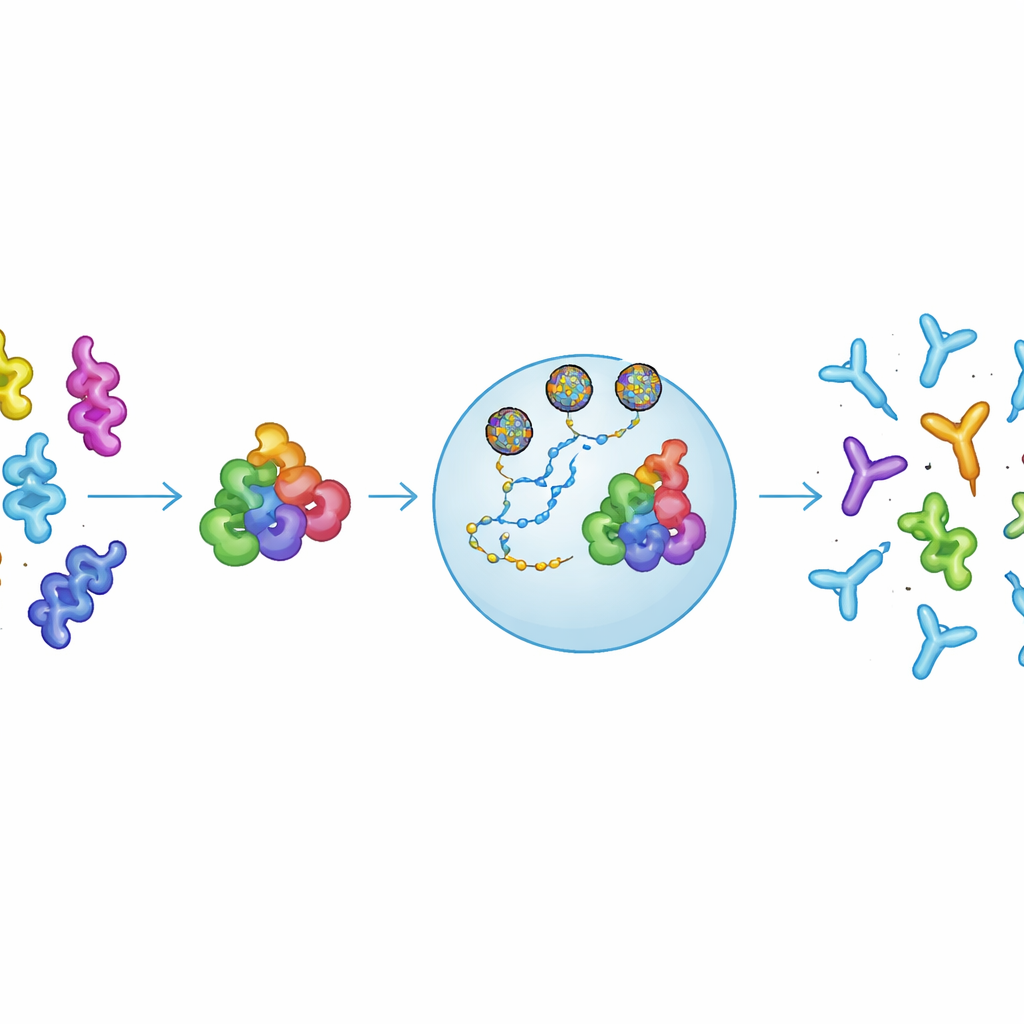
Ein „Konsensus“-Allergen entwerfen
Die Forschenden wollten ein einzelnes Protein entwerfen, das viele verschiedene nsLTP-Allergene gleichzeitig nachahmt. Sie verglichen Aminosäuresequenzen von nsLTPs, die sowohl in Lebensmitteln als auch in Pollen vorkommen, und bauten eine Konsensus-Version, genannt cnsLTP1, die kein natürliches Protein kopiert, aber gemeinsame strukturelle Merkmale der Familie einfängt. Labortests zeigten, dass dieses konstruierte Protein sich wie natürliche nsLTPs faltete, beim Erhitzen und Abkühlen stabil blieb und vor allem von IgE-Antikörpern von bereits gegen nsLTPs allergischen Patienten erkannt wurde. Diese Erkennung deutet darauf hin, dass cnsLTP1 dieselben wichtigen „allergieauslösenden Stellen“ präsentiert wie reale Allergene — eine Voraussetzung, um das Immunsystem so umzulenken, dass es anders reagiert.
Das Immunsystem mit mRNA- und Proteinimpfstoffen trainieren
Das Team testete cnsLTP1 in Mäusen mit zwei verschiedenen Verabreichungswegen: einem traditionellen Proteinimpfstoff mit Adjuvantien und einem mRNA-Impfstoff, verpackt in Lipidnanopartikeln, ähnlich zusammengesetzt wie zugelassene mRNA-Impfstoffe. Bei immunologisch naiven Mäusen riefen beide Ansätze starke Antikörperantworten gegen cnsLTP1 hervor, insbesondere IgG-Subklassen, die bei Mäusen eine schützende, allergieblockierende Rolle spielen. Der mRNA-basierte Impfstoff neigte dazu, mehr einer bestimmten IgG-Form zu erzeugen und dies nach weniger Dosen zu erreichen. Gegen cnsLTP1 erzeugte Antikörper banden nicht nur an das konstruierte Protein, sondern auch an ein breites Panel verschiedener Nahrungs- und Pollen-nsLTPs — häufig breiter als Antikörper, die gegen einzelne natürliche Allergene wie Pfirsich- oder Beifuß-nsLTPs erzeugt wurden. Das bedeutet, dass das Konsensus-Design dem Immunsystem erfolgreich beigebracht hat, viele verwandte Allergene zu erkennen.
Allergische Reaktionen im Labor blockieren und Tests an allergischen Mäusen
Um zu prüfen, ob diese Antikörper tatsächlich allergische Reaktionen stören können, mischten die Forschenden Mausserum mit Allergenen und fügten dann humanes Serum von Patienten mit schweren nsLTP-Allergien hinzu. Sie fanden heraus, dass durch cnsLTP1 induzierte Antikörper das IgE-Binden an mehrere nsLTPs blockieren konnten und die Degranulation von humanisierten basophilen Zell-ähnlichen Zellen — ein zellbasiertes Modell für allergische Aktivierung — verringerte. In einem anspruchsvolleren Test verwendete das Team ein Mäusemodell, das bereits gegen Pfirsich-nsLTP sensibilisiert und anfällig für Anaphylaxie war. Der mRNA-Impfstoff wurde gut vertragen und steigerte IgG-Antikörper gegen mehrere nsLTPs, reduzierte jedoch unter den spezifisch getesteten Bedingungen nicht deutlich anaphylaktische Symptome wie Temperaturabfall oder Marker der Mastzellaktivierung. Das deutet darauf hin, dass zwar das Immunsystem umgestaltet wurde, das Regime aber noch nicht stark genug oder fein abgestimmt war, um schwere Reaktionen vollständig zu verhindern.
Was das für die künftige Allergiebehandlung bedeuten könnte
Die Studie liefert einen Proof of Concept, dass ein einzelnes, konstruiertes „Konsensus“-Allergen, das per mRNA geliefert wird, breite, kreuzreaktive und funktionell blockierende IgG-Antikörper gegen eine ganze Familie verwandter Nahrungs- und Pollenproteine auslösen kann. Obwohl das aktuelle Protokoll die allergischen Mäuse noch nicht vor Anaphylaxie schützte, deuten die Befunde auf eine flexible Plattform hin, die durch Anpassung von Dosis, Adjuvantien oder Verabreichungsweg verbessert werden könnte. Langfristig könnten solche konsensusbasierten mRNA-Therapien die Behandlung von Clustern verwandter Allergien — etwa durch nsLTPs, andere Pflanzenproteinfamilien oder sogar rasch mutierende Erreger — mit kürzeren, präziseren und breiter schützenden Behandlungen ermöglichen.
Zitation: Møiniche, M., Johansen, K.H., Parrón-Ballesteros, J. et al. An mRNA-delivered consensus allergen induces a neutralizing IgG response against food and pollen allergens. Nat Commun 17, 2402 (2026). https://doi.org/10.1038/s41467-026-69134-4
Schlüsselwörter: Nahrungsmittelallergie, Pollenallergie, mRNA-Immuntherapie, Kreuzreaktivität, Lipidtransferproteine