Clear Sky Science · de
MG53 vermittelt die Kommunikation zwischen Skelettmuskel und Leber und verbessert den Alkoholabbau bei alkoholischer Lebererkrankung
Muskeln, die der Leber helfen
Übermäßiger Alkoholkonsum kann die Leber nach und nach vergiften, zu Fettablagerungen, Vernarbung und schließlich Leberversagen führen. Gleichzeitig verlieren viele starke Trinker Muskelmasse und -kraft, ein Zustand, der als Muskelschwund bezeichnet wird. Diese Studie zeigt, dass unsere Muskeln in dieser Entwicklung nicht nur Nebenakteure sind: Sie geben ein schützendes Protein ab, das zur Leber gelangt und dort den Alkoholabbau sicherer macht. Das Verständnis dieser verborgenen Zusammenarbeit zwischen Muskel und Leber könnte neue Behandlungswege für die alkoholische Lebererkrankung eröffnen, für die derzeit wirksame Therapien noch knapp sind.
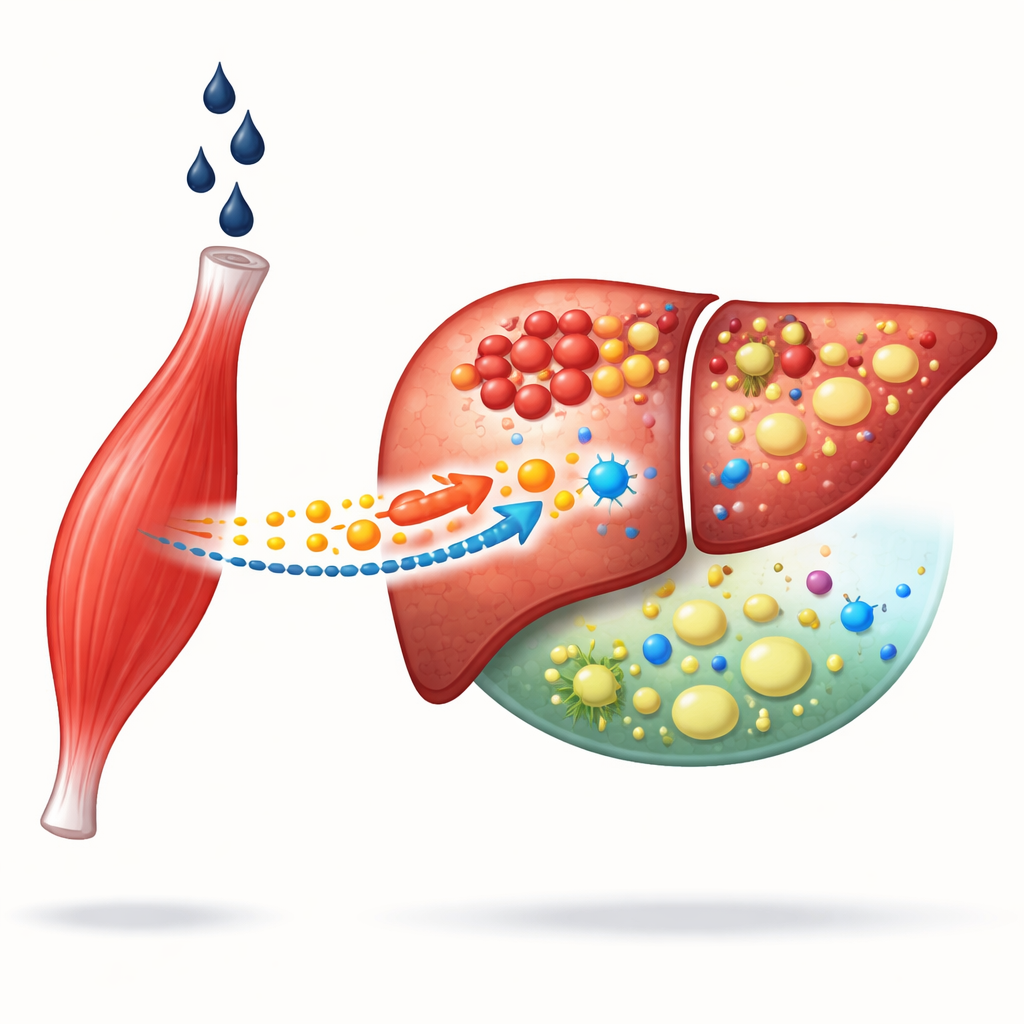
Wenn Trinken sowohl Muskel als auch Leber schädigt
Die alkoholische Lebererkrankung entwickelt sich über Jahre starken Alkoholkonsums und steht in engem Zusammenhang mit Muskelverlust. Patienten mit schwächerer Muskulatur haben tendenziell stärkere Leberschäden und ein höheres Komplikationsrisiko. Die Autorinnen und Autoren begannen mit der Analyse nationaler Gesundheitsdaten und menschlicher Leberproteindatenbanken. Sie stellten fest, dass Menschen mit geringer Muskelmasse etwa doppelt so häufig alkoholbedingte Leberprobleme hatten, insbesondere Männer. Unter vielen zirkulierenden Proteinen fiel eines als starker Kandidat auf, das die Muskelgesundheit mit Leberergebnissen verbinden könnte: MG53, ein vorwiegend vom Skelettmuskel gebildetes Protein, das als eine Art „molekulares Pflaster“ für die Reparatur beschädigter Zellmembranen bekannt ist.
Ein reisender Beschützer von Muskel zur Leber
Unter normalen Bedingungen produzieren Leberzellen ihr eigenes MG53 nicht und sind auf das aus dem Blutstrom Ankommende angewiesen. Bei Menschen und Mäusen mit alkoholischer Lebererkrankung beobachteten die Forschenden sinkende MG53-Spiegel im Blut, während die Werte in der Leber anstiegen, was darauf hindeutet, dass das Protein aus dem Kreislauf in das verletzte Lebergewebe eingelagert wird. Genetisch veränderte Mäuse ohne MG53 waren deutlich anfälliger für alkoholbedingte Schäden: Ihre Lebern wurden fettreicher, stärker entzündet, stärker vernarbt und die Überlebensraten sanken drastisch. Als das fehlende Protein durch eine im Labor hergestellte Version ersetzt wurde, verbesserten sich viele dieser Probleme, was darauf hindeutet, dass MG53 ein entscheidender Bestandteil der körpereigenen Abwehr gegen chronische Alkohlschäden ist.
Wie MG53 den Alkoholabbau verstärkt
Für einen sicheren Alkoholabbau sind zwei Schlüsselenzyme der Leber erforderlich: Alkoholdehydrogenase (ADH) und Aldehyddehydrogenase 2 (ALDH2). Diese Enzyme wandeln Alkohol in ein hochreaktives Zwischenprodukt und dieses dann in eine weniger schädliche Substanz um, die der Körper ausscheiden kann. Dieser Prozess ist auf Zink angewiesen, ein Spurenelement, das bei starken Trinkern oft erschöpft ist. Die Studie zeigt, dass MG53 physisch an beide Enzyme bindet und ihnen Zink zuführt, wobei es wie ein Metall-Chaperon wirkt — ein Träger, der die Enzyme mit dem benötigten Metall belädt, damit sie effizient arbeiten. Bei Mäusen ohne MG53 sanken die Zinkwerte in der Leber weiter, Alkohol und seine toxischen Abbauprodukte häuften sich im Blut an und der oxidative Stress nahm zu. Die Zugabe rekombinanten MG53 stellte die Zinkspiegel wieder her, steigerte die Enzymaktivität und verringerte toxische Alkoholzwischenprodukte.
Eine intelligentere Wirkstoffverpackung entwickeln
Um diese Erkenntnisse in eine mögliche Therapie zu übersetzen, entwickelten die Forschenden winzige, biobasierte Nanopartikel, die MG53 zusammen mit Zink verpacken. Diese MG53@Zn-Partikel bestehen aus einer Hülle aus humanem Serumalbumin und sind so dimensioniert, dass sie sich in der Leber anreichern. In Zellkulturen, die sehr hohen Alkoholwerten ausgesetzt waren, gelangten die Partikel in Leberzellen, verringerten oxidativen Stress und Fettablagerungen und schützten das Überleben der Zellen besser als MG53 allein. Bei Mäusen, die eine kombinierte chronische‑plus‑Binge‑Alkoholdiät erhielten, verbesserte wiederholte Gabe von MG53@Zn‑Nanopartikeln das Überleben, stellte die Zinkvorräte der Leber wieder her, senkte Marker für Leberschädigung und Entzündung, reduzierte Vernarbung und beseitigte Alkohol sowie sein toxisches Zwischenprodukt effizienter. Wichtig ist, dass die Nanopartikel in einem einmonatigen Behandlungszeitraum bei gesunden Mäusen als sicher erschienen.
Was das für die künftige Versorgung bedeutet
Für die Allgemeinheit ist die zentrale Botschaft, dass Muskel und Leber enger zusammenarbeiten, als man zuvor vermutet hatte. Ein aus dem Muskel freigesetztes Protein kann zur Leber reisen, Zink zu alkoholverarbeitenden Enzymen transportieren und dem Organ helfen, mit dem Stress starken Trinkens umzugehen. Durch die Entwicklung eines Nanopartikels, der sowohl dieses Protein als auch Zink direkt in die Leber liefert, skizzieren die Forschenden eine vielversprechende Strategie zur Behandlung der alkoholischen Lebererkrankung. Zwar beschränken sich diese Ergebnisse bislang auf Tiermodelle und überwiegend männliche Probanden, doch sie weisen in Richtung künftiger Therapien, die die körpereigenen Reparatursysteme unterstützen, anstatt nur Symptome nach bereits eingetretenen schweren Schäden zu behandeln.
Zitation: Shu, T., Zeng, X., Wang, J. et al. MG53 mediates skeletal muscle-liver cross-talk and enhances alcohol metabolism in alcoholic liver disease. Nat Commun 17, 2722 (2026). https://doi.org/10.1038/s41467-026-69132-6
Schlüsselwörter: alkoholische Lebererkrankung, MG53, Muskel–Leber-Kommunikation, Zinkstoffwechsel, Nanopartikeltherapie