Clear Sky Science · de
Ein isolierbares Phosphaalumen(3), das kleine Moleküle über einzigartige Reaktivitätsmodi aktivieren kann
Hartnäckige Bindungen mit einem neuen chemischen Werkzeug aufbrechen
Chemiker suchen ständig nach Wegen, störrische Moleküle zur Reaktion zu bewegen. Viele alltägliche Stoffe, von Wasserstoffgas bis Kohlendioxid, sind ausgesprochen stabil und damit schwer in nützliche Produkte zu überführen. Diese Arbeit berichtet über ein neu entworfenes Molekül aus Aluminium und Phosphor, das solche widerwilligen Partner greifen und ihre Bindungen aufspalten kann. Das Verständnis und die Kontrolle dieser Art der Bindungsaktivierung könnte eines Tages helfen, Abgasströme in Ausgangsstoffe zu verwandeln oder mildere, metallarme Routen zur Herstellung von Feinchemikalien und Materialien zu bieten.
Eine Design‑Bindung zwischen Aluminium und Phosphor
Im Zentrum der Studie steht eine seltene Verbindung zwischen zwei Hauptgruppenelementen: Aluminium und Phosphor. Die Forscher stellten ein Molekül her, in der Arbeit als „3“ bezeichnet, in dem diese beiden Atome durch eine enge Doppelbindung verknüpft sind. Um dieses reaktive Paar vor Zerfall zu schützen, umgaben sie es mit einem voluminösen organischen Gerüst, das es vor ungewollten Reaktionen abschirmt. Über zwei verschiedene Syntheserouten gelangte man zu diesem Komplex in isolierbarer Form und wuchs Einkristalle, die sich für Röntgenbeugung eigneten; damit wurde bestätigt, dass Phosphor kurz und doppelbindungsähnlich an Aluminium gebunden ist, während jedes Atom von stickstoffhaltigen Liganden gestützt wird. Rechnungen zeigten, dass die Elektronen zwischen Aluminium und Phosphor ungleich verteilt sind, wodurch die Bindung polarisiert und für Angriffe anderer Moleküle bereit ist.
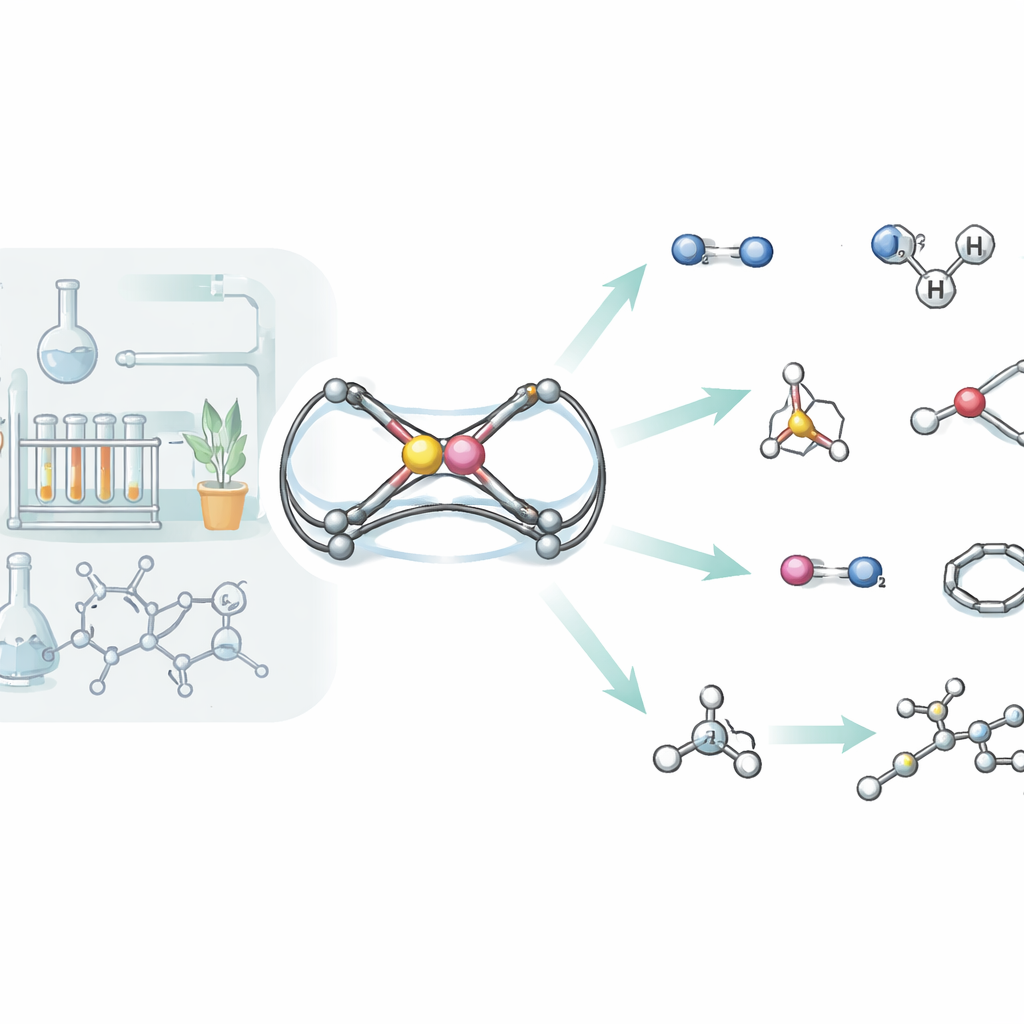
Wie das neue Molekül mit Wasserstoffgas umgeht
Wasserstoffgas ist bekanntlich schwer zu spalten, ohne Edelmetalle zu verwenden, doch die neue Aluminium‑Phosphor‑Einheit schafft genau das. Unter milden Bedingungen reagiert der Komplex mit Wasserstoff auf zwei unterschiedliche Weisen. In einem Pfad addiert sich die H–H‑Bindung simpel über die Aluminium–Phosphor‑Doppelbindung, die so in zwei Einfachbindungen verwandelt wird und bei der jedes Atom ein Wasserstoffatom aufnimmt. Im anderen Fall wird das Wasserstoffmolekül kooperativ von Aluminium und einem benachbarten Stickstoffatom auseinandergezogen, ein Verhalten, das an sogenannte „frustrierte Lewis‑Paare“ erinnert, die Wasserstoff ohne traditionelle Metallkatalysatoren aktivieren. Detaillierte Computersimulationen verfolgten beide Routen und zeigten, dass ihre Energiebarrieren ähnlich sind, was erklärt, warum beide Produkte nebeneinander gebildet werden.
Ein Spektrum kleiner Moleküle auseinandernehmen
Wasserstoff ist nur der Anfang. Das Team prüfte systematisch, wie ihr Aluminium‑Phosphor‑Gerüst mit einer breiten Palette kleiner Moleküle reagiert, darunter Weißphosphor, Isocyanide, Kohlendioxid, Distickstoffmonoxid, Trimethylsilylazid, Selendimere, Silane, Amine, Styrol und einfache Alkine. In vielen dieser Reaktionen wird die ursprüngliche Al=P‑Verbindung vollständig aufgebrochen, wobei die beiden Atome in größeren Käfig‑ oder Ringstrukturen enden, die Fragmente des eingelagerten Moleküls aufnehmen. So wird beispielsweise Weißphosphor (P4) aufgebrochen und in einen Aluminium‑Phosphor‑Käfig umgebaut, während Kohlendioxid zweimal inseriert und ein sechsgliedriger Ring gebildet wird, der Aluminium und Phosphor über zwei neue Kohlenstoff‑Sauerstoff‑Brücken verbindet. Bei Reaktionen mit Silanen und Aminen verhält sich das Molekül hingegen eher wie eine klassische Doppelbindung: Die eingehende Si–H‑ oder N–H‑Einheit addiert sauber über Al=P und demonstriert erneut den „π‑Bindungs“-Charakter dieser ungewöhnlichen Verbindung.
Warum das umgebende Gerüst wichtig ist
Eine der zentralen Lehren der Arbeit ist, dass das voluminöse, stickstoffreiche Gerüst um die Al=P‑Einheit nicht bloß ein Stützgerüst ist; es lenkt, wie und wo Reaktionen stattfinden. Im Vergleich mit früheren, kürzerlebigen Aluminium‑Phosphor‑Systemen zeigen die Autoren, dass kleine Änderungen in den stützenden Liganden das Gleichgewicht zwischen verschiedenen Pfaden umkippen können, etwa zwischen einfacher Addition über die Doppelbindung und aufwändigeren Bindungsaufspaltungen und Ringbildungen. Anspruchsvolle Analysen der Elektronenverteilung offenbarten eine starke Polarisation der Al=P‑Bindung und hoben hervor, wie benachbarte Stickstoffatome mit Aluminium kooperieren können, besonders bei der Wasserstoffaktivierung. Sterische Hinderung — die räumliche Verdrängung großer Gruppen — schiebt eingehende Moleküle ebenfalls zu dem einen oder anderen reaktiven Ort.
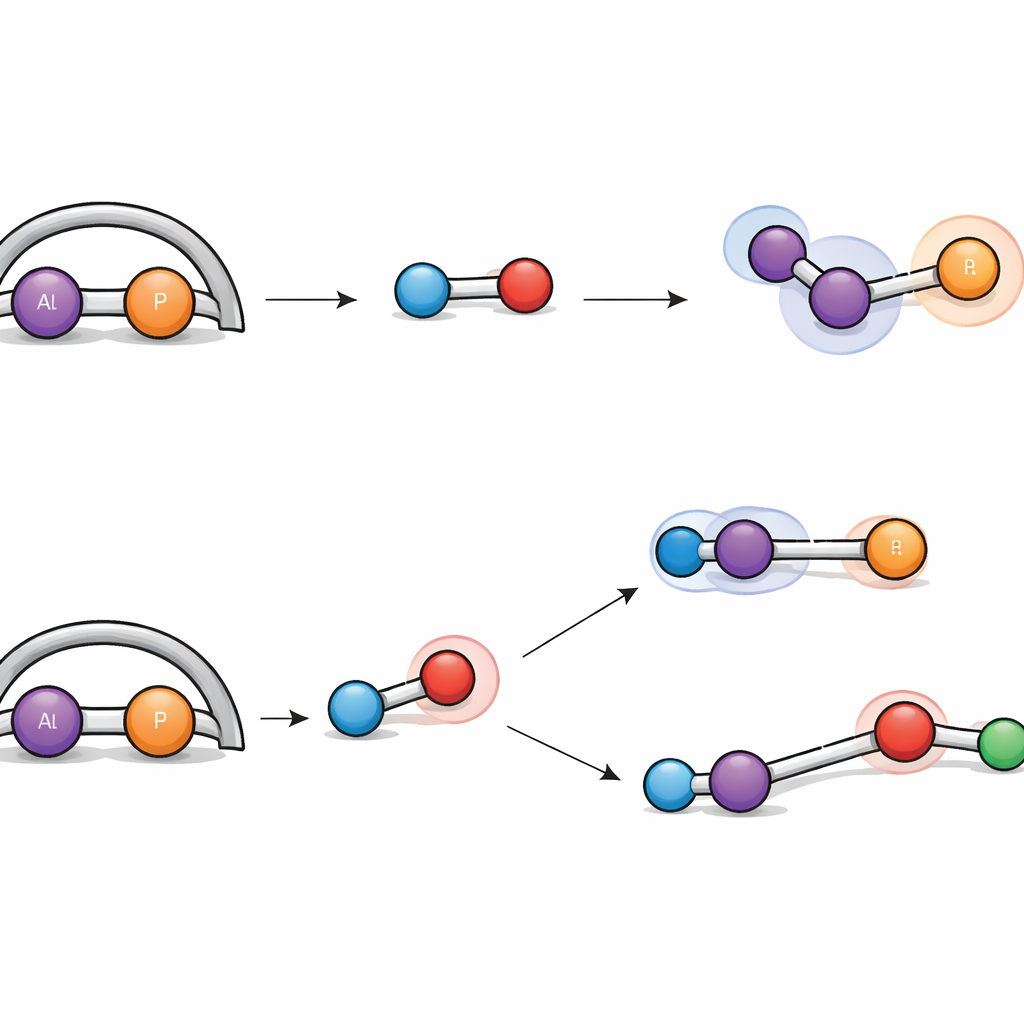
Was das für die zukünftige Chemie bedeutet
Für Nicht‑Spezialisten mag das Buchstabensalat an Reagenzien in dieser Studie fern wirken, doch die zugrundeliegende Botschaft ist klar: Durch gezieltes Abstimmen von Bindungen und Form um Hauptgruppenelemente können Chemiker bewegliche Werkzeuge bauen, die mit traditionellen Metallkatalysatoren konkurrieren oder sie ergänzen. Dieser isolierbare Aluminium‑Phosphor‑Komplex überlebt nicht nur in einer Flasche, sondern bearbeitet auch unter milden Bedingungen eine breite Palette hartnäckiger kleiner Moleküle, spaltet Wasserstoff, rekonstruiert Weißphosphor und bindet Kohlendioxid. Die Arbeit zeigt, dass subtile Änderungen am „Griff“ eines Moleküls seine Reaktivität tiefgreifend umleiten können und bietet eine Blaupause für die Gestaltung künftiger Katalysatoren, die einfache, stabile Moleküle präzise und effizient in wertvollere Produkte überführen.
Zitation: Cha, Y., Yang, Z., Zhuang, X. et al. An isolable phosphaalumene(3) capable of small molecule activation via unique modes of reactivity. Nat Commun 17, 2390 (2026). https://doi.org/10.1038/s41467-026-69118-4
Schlüsselwörter: Aktivierung kleiner Moleküle, Hauptgruppenchmie, Aluminium‑Phosphor-Doppelbindung, frustrierte Lewis‑Paare, Mechanismen der Bindungsaktivierung