Clear Sky Science · de
Hemmungsmechanismus der pilzlichen β−1,3-Glucan-Synthasen durch triterpenoide Antimykotika
Warum das Stoppen von Pilzinfektionen wichtig ist
Pilzinfektionen fordern still mehr als eine Million Menschenleben pro Jahr und bedrohen weltweit Ernten und Ökosysteme. Ärztinnen und Ärzte haben nur eine begrenzte Auswahl an Antimykotika, und einige gefährliche Pilze entwickeln Wege, diesen zu entkommen. Diese Studie enthüllt auf molekularer Ebene, wie eine neue Klasse von Antimykotika ein Schlüsselenzym, das Pilze zum Aufbau ihrer schützenden Zellwand benötigen, anbindet und außer Kraft setzt. Dieses Verständnis liefert eine Roadmap zur Entwicklung besserer Wirkstoffe, die resistente Pilze überlisten können.
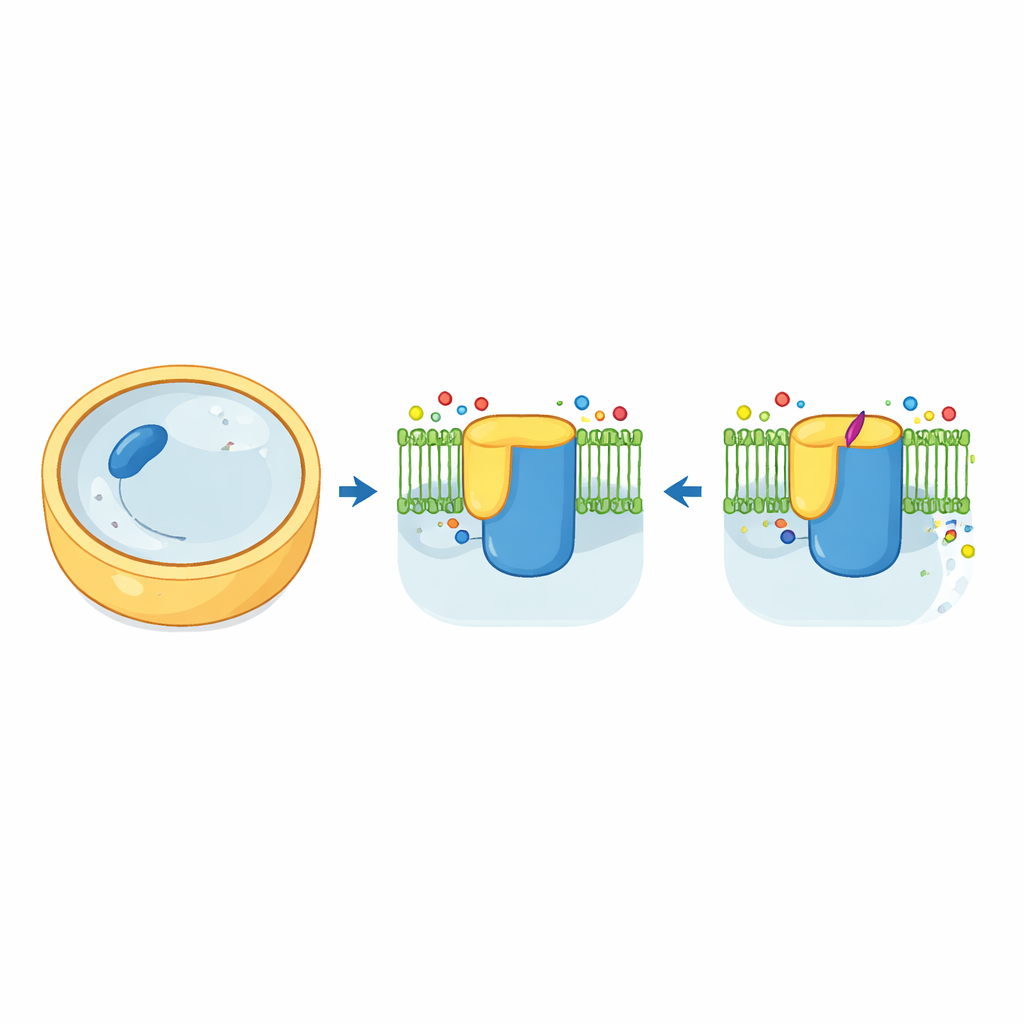
Der „Ziegelmacher“ der pilzlichen Zellwand
Pilzzellen sind von einer widerstandsfähigen Wand umgeben, die größtenteils aus einem zuckerbasierten Polymer namens β-1,3-Glucan besteht. Das Enzym, das dieses Polymer herstellt und nach außen transportiert — die β-1,3-Glucan-Synthase — wirkt wie eine Kombination aus Ziegelmacher und Förderband. In der Bäckerhefe besteht diese Maschine aus zwei sehr ähnlichen Versionen, Fks1 und Fks2, die jeweils in der Zellmembran verankert sind und von einem kleinen Helferprotein namens Rho1 reguliert werden. Mithilfe der Kryo-Elektronenmikroskopie gewannen die Autorinnen und Autoren hochaufgelöste dreidimensionale Aufnahmen von sowohl Fks1 als auch Fks2 in ihrer natürlichen Form. Die Strukturen zeigen eine große zytosolische „Werkbank“, die an ein Geflecht membraneinspannender Helices anschließt, mit einer zentralen Höhlung, die vermutlich als Tunnel dient, durch den die wachsende Glucankette die Zelle verlässt.
Wie ein Naturstoffmedikament das Enzym ergreift
Klinisch bedeutsame triterpenoide Wirkstoffe, darunter das orale Medikament Ibrexafungerp, stammen von einer natürlichen Verbindung namens Enfumafungin. Bislang war unbekannt, wo genau auf der Glucan-Synthase diese Wirkstoffe binden. Die Forschenden lösten Strukturen von Fks1 und Fks2 gebunden an Enfumafungin. Überraschenderweise verkeilt sich das Medikament nicht im aktiven Zentrum, in dem Zuckerbausteine verknüpft werden. Stattdessen liegt es an der Außenseite einer einzelnen Membranhelix, TM5, eingebettet in der Membran etwa drei Nanometer vom katalytischen Zentrum und in der Nähe des wahrscheinlichen Glucan-Austrittskanals. Wichtige Aminosäuren in diesem Bereich umschließen den hydrophoben Kern des Wirkstoffs und berühren seinen sauren Schwanz, während sein Zuckeranhang kaum Kontakt zum Protein hat — was erklärt, warum Chemikerinnen und Chemiker diesen Teil modifizieren konnten, ohne die Wirksamkeit zu verlieren.
Wirkstoffe, die eine bewegliche Maschine einfrieren
Auf den ersten Blick erscheint die Gesamtgestalt des Enzyms mit und ohne Enfumafungin nahezu unverändert. Der entscheidende Unterschied liegt in der Organisation der umgebenden Lipide und in der Flexibilität bestimmter Helices. Wenn das Medikament bindet, dreht sich eine nahegelegene aromatische Seitenkette, um Enfumafungin festzuklemmen, und stabilisiert zusammen mit einer weiteren Aminosäure ein geordnetes Lipid neben dem Wirkstoff. Zusätzlich ordnen sich sterolähnliche Lipide um eine Reihe horizontaler Helices, die mithelfen, den Weg für den Glucanexport zu definieren. Diese Lipide wirken wie Keile und Stützen und verriegeln die Helices sowie den Kanalzugang in einer bestimmten „basalen“ Anordnung. Genetische Tests zeigen, dass Veränderungen vieler Kontaktstellen für das Medikament oder diese Sterole die Wirkstoffbindung schwächen oder die Enzymfunktion zerstören; Mutationen an diesen Stellen entsprechen bekannten Resistenzmutationen in humanen und pflanzlichen Krankheitserregern.
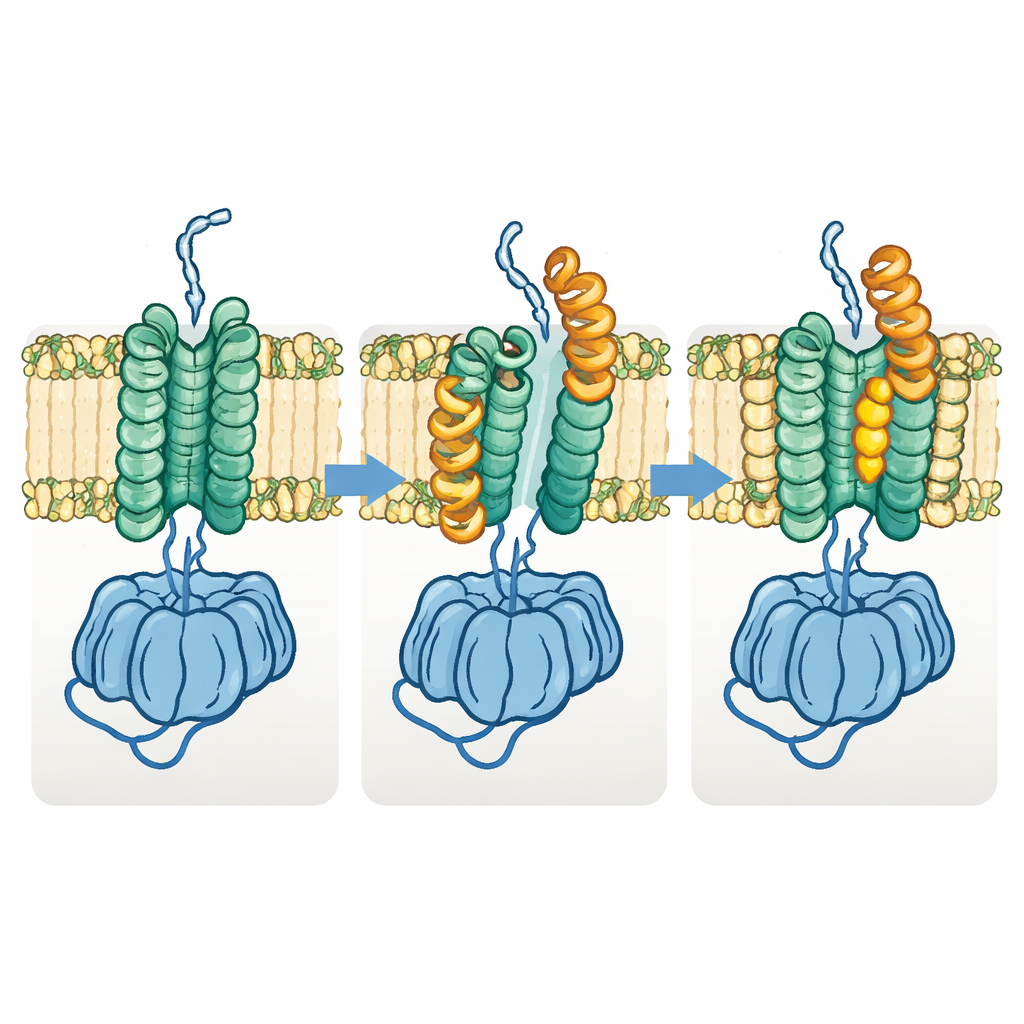
Eine notwendige Formänderung für den Polymertransport
Das Team entdeckte außerdem eine ausgeprägte „offene“ Form von Fks1. In diesem Zustand verschiebt sich eine Hälfte der Membranregion seitlich und Schlüsselfoldhelixstrukturen schwingen nach außen, sodass der Raum zwischen den beiden Membrangebündeln aufgeklappt und der scheinbare Glucantunnel verbreitert wird. Der Vergleich zahlreicher Strukturen legt nahe, dass das Enzym während des normalen Betriebs zwischen dem basalen und dem offenen Zustand zyklisch wechselt: Der basale Zustand bereitet die Polymerbildung vor und initiiert sie, während der offene Zustand der wachsenden Kette erlaubt, lateral durch die Membran nach außen zu wandern. Als die Autorinnen und Autoren Disulfidbrücken einbauten, die das Enzym dauerhaft in einem der beiden Zustände verriegeln sollten, verloren beide Varianten weitgehend ihre Aktivität — ein Befund, der die Notwendigkeit dieser Formänderung für die Funktion stützt.
Was das für zukünftige Antimykotika bedeutet
Indem die Studie zeigt, dass Enfumafungin und verwandte Wirkstoffe nicht das katalytische Zentrum blockieren, sondern die lokale Membranumgebung umgestalten und die Glucan-Synthase im basalen Zustand einfrieren, offenbart sie einen unkonventionellen Wirkmechanismus. Sie demonstriert außerdem, dass Fks1 und Fks2 nahezu identische Strukturen und Wirkstoffantworten teilen, was erklärt, warum beide bei der Bekämpfung von Resistenz berücksichtigt werden müssen. Darüber hinaus macht die Arbeit deutlich, wie kleine Moleküle „schwer ansprechbare“ Membranproteine kontrollieren können, indem sie flache Oberflächen binden und Lipide rekrutieren — ein konzeptioneller Leitfaden für die Entwicklung der nächsten Generation von Antimykotika, die auch gegen sich entwickelnde Pilzresistenzen wirksam bleiben.
Zitation: You, ZL., Sun, L., Wang, LX. et al. Inhibition mechanism of the fungal β−1,3-glucan synthases by triterpenoid antifungal drugs. Nat Commun 17, 2347 (2026). https://doi.org/10.1038/s41467-026-69114-8
Schlüsselwörter: Antimykotika, pilzliche Zellwand, Glucan-Synthase, Arzneimittelresistenz, Kryo-Elektronenmikroskopie