Clear Sky Science · de
Cryo-EM-Strukturen von Zwischenstufen der Portal‑Hals‑Assemblierung des Bakteriophagen T4 zeigen einen Mechanismus zur Zurückhaltung des viralen Genoms
Wie ein Virus seine DNA unter Druck hält
Der Bakteriophage T4 ist ein Virus, das E. coli infiziert und seine DNA so dicht in seinen Kopf verpackt, dass der Innendruck fünf- bis siebenfach höher sein kann als in einer Champagnerflasche. Trotzdem tritt die DNA nicht aus, während das Virus den Rest seines Aufbaus fertigstellt. Diese Studie zeigt auf molekularer Ebene, wie T4 dieses Problem mit einem winzigen Doppelverschluss löst, der wie eine Luftschleuse für sein genetisches Material wirkt.
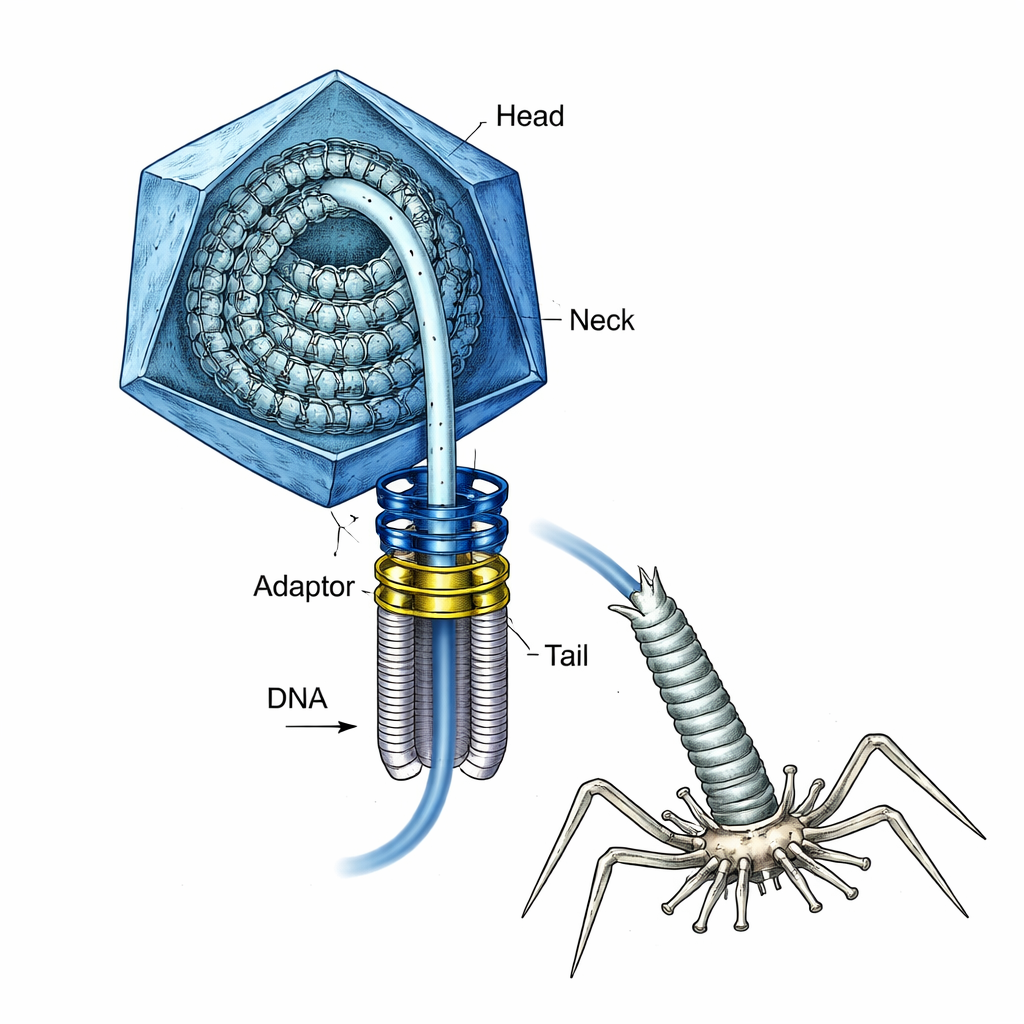
Das Virus mit einer geladenen Feder im Inneren
T4 ist seit langem ein Arbeitspferd der Molekularbiologie und dient außerdem als Modell für den Bau künftiger Impfstoffe und Gentherapie‑Werkzeuge. Während der Assemblierung baut das Virus zunächst eine leere Proteinhülle, den Kopf, und an einer Ecke einen ringförmigen „Portal“-Komplex. Ein kräftiger molekularer Motor zieht dann die DNA durch dieses Portal in den Kopf, bis dieser „voll“ ist. Zu diesem Zeitpunkt muss der Motor sich lösen, ein Hals und ein Schwanz müssen angebracht werden und später muss die DNA in eine Bakterienzelle injiziert werden — alles ohne dass die unter Druck stehende DNA vorzeitig herausspritzt. Wie das Virus diese stark gespannte DNA während dieser Übergänge sicher zurückhielt, war bislang nicht gut verstanden.
Den Hals im Labor wiederaufbauen
Die Forscher rekonstruierten Schlüsselteile von T4 in Bakterien und vermischten sie unter kontrollierten Bedingungen, um zu beobachten, wie der Hals — die Verbindung zwischen Kopf und Schwanz — sich zusammensetzt. Zwei virale Proteine, bezeichnet als gp13 und gp14, wurden separat hergestellt. Für sich genommen lagen sie als Einzelbausteine vor, doch zusammen setzten sie sich zu gestapelten Ringen zusammen, die einen zentralen Tunnel für den DNA‑Durchgang bilden. Überraschenderweise tauchte in diesen Präparationen ein drittes Protein auf: Hfq, ein bekanntes bakterielles Protein, das normalerweise die RNA‑ und Genregulation in E. coli unterstützt. Massenspektrometrie bestätigte, dass Hfq spezifisch an gp14 bindet, was nahelegt, dass das Virus dieses Wirtsprotein als Teil seines Halses ausleiht.
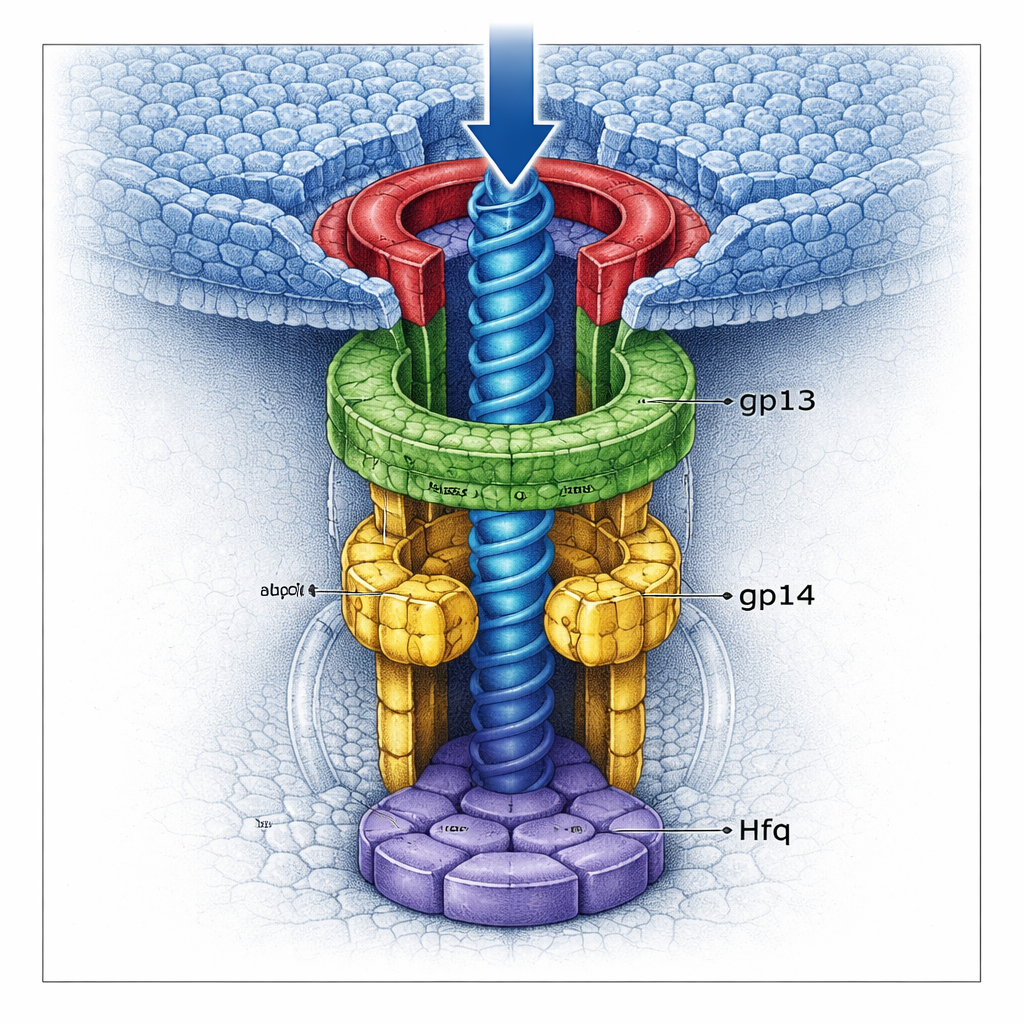
Ein Doppelverschluss, der das Genom verriegelt
Mit hochauflösender Kryo‑Elektronenmikroskopie visualisierte das Team mehrere Zustände des Halskomplexes in nahezu atomarer Detailgenauigkeit. Sie fanden, dass gp13 einen breiten Ring bildet, der sich an das Portal anpasst, während gp14 darunter als Hexamer sitzt und einen engeren Kanal ausbildet. Entscheidend trägt jedes gp14‑Untereinheit eine lange Schleife bei, die in die Mitte des Tunnels schwingt. Zusammen formen sechs solcher „Stopper‑Schleifen“ ein dichtes Tor, das das letzte DNA‑Segment auffangen kann, wenn es versucht, den Kopf zu verlassen. Unterhalb von gp14 setzt sich das gekaperte Hfq‑Protein zu einem eigenen Hexamer zusammen und verschließt den unteren Kanal wie eine zweite Tür. In Anwesenheit von Hfq ist die gp13–gp14‑Struktur vollständiger und starrer, und die kombinierten Verschlüsse verengen den Tunnel noch stärker, wodurch ein DNA‑Leck wesentlich unwahrscheinlicher wird.
Timing, Fehlersicherung und ein ausgeliehener Helfer
Die Studie zeigt außerdem, dass dieses System mehr als ein statischer Pfropf ist; es ist eine sorgfältig choreografierte Abfolge von Formänderungen. Sobald der Kopf voll ist, drückt der Innendruck das Portal in eine neue Konformation, die Bindungsstellen für gp13 freilegt. Ein vorgefertigter gp13–gp14–Hfq‑Hals dockt dann an das Portal an. Gp13 biegt sich, schwingt nach oben und verriegelt sowohl am Portal als auch an der Außenschale, wodurch der Hals fest in den Kopf eingewoben wird. Während dieser Phase halten die gp14‑Stopper‑Schleifen und der Hfq‑Pfropfen die DNA an Ort und Stelle. Hfq erfüllt eine zweite Rolle als Qualitätskontrolleur: Indem es Schlüsseloberflächen an gp14 besetzt, verhindert es, dass gp14 in der falschen Position an das Portal bindet, was zu einer Fehlassemblierung des Halses führen würde. Erst wenn der vorgebaute Schwanz eintrifft, bildet ein Schwanzspitzenprotein, gp15, eine noch stärkere Bindung an gp14, verdrängt Hfq und öffnet den Weg für die kontrollierte Freisetzung der DNA in den Schwanz.
Warum das über ein einzelnes Virus hinaus wichtig ist
Einfach gesagt verwendet T4 ein zweifaches Türschloss, um eine starke DNA‑„Feder“ zurückzuhalten, während es den Rest des Virus fertigstellt. Die erste Tür wird aus seinem eigenen Halsprotein gp14 gebaut, die zweite Tür entlehnt es vorübergehend vom Wirtsprotein Hfq, das das Virus später wieder verwirft. Dieser Doppelverschluss stellt sicher, dass nahezu keine DNA verloren geht und dass das fertige Virus infektiös bleibt. Weil viele große Viren ihre Genome unter ähnlichen extremen Drücken verpacken und verwandte Architekturen teilen, deutet diese Arbeit darauf hin, dass vergleichbare Verschlusssysteme und sogar vorübergehendes Kapern von Wirtsproteinen weit verbreitet sein könnten. Das Verständnis dieser Mechanismen könnte die Entwicklung sichererer viraler Vektoren in der Medizin leiten und neue Ansätze aufzeigen, schädliche Viren durch gezieltes Stören ihrer Genom‑„Schlösser“ zu blockieren.
Zitation: Han, L., Mao, Q., Zhu, J. et al. Cryo-EM structures of bacteriophage T4 portal-neck assembly intermediates reveal a viral genome retention mechanism. Nat Commun 17, 1964 (2026). https://doi.org/10.1038/s41467-026-69107-7
Schlüsselwörter: Bakteriophage T4, virale Assemblierung, Cryo‑Elektronenmikroskopie, Genomverpackung, Wirt–Virus‑Interaktion