Clear Sky Science · de
Strukturelle Grundlage des Pausierens während der Transkriptionsinitiation bei Mycobacterium tuberculosis
Wie die Schalter eines Keims ins Stocken geraten können
Mycobacterium tuberculosis, das Bakterium, das Tuberkulose verursacht, muss Gene ständig an- und ausschalten, um in der harten Umgebung des Körpers zu überleben. Die in diesem Artikel beschriebene Arbeit gewährt Einblick in einen der frühesten Schritte dieser genetischen Kontrolle und fängt eine flüchtige „Pause“ ein, die genau dann auftritt, wenn die Zelle beginnt, DNA in RNA abzulesen. Das Verständnis dieser Pause hilft zu erklären, wie das Mikroben entscheidet, ob ein Gen vollständig eingeschaltet oder der Versuch abgebrochen wird — und könnte schließlich neue Schwachstellen für Antibiotika aufdecken.
Die Botschaft aus DNA starten
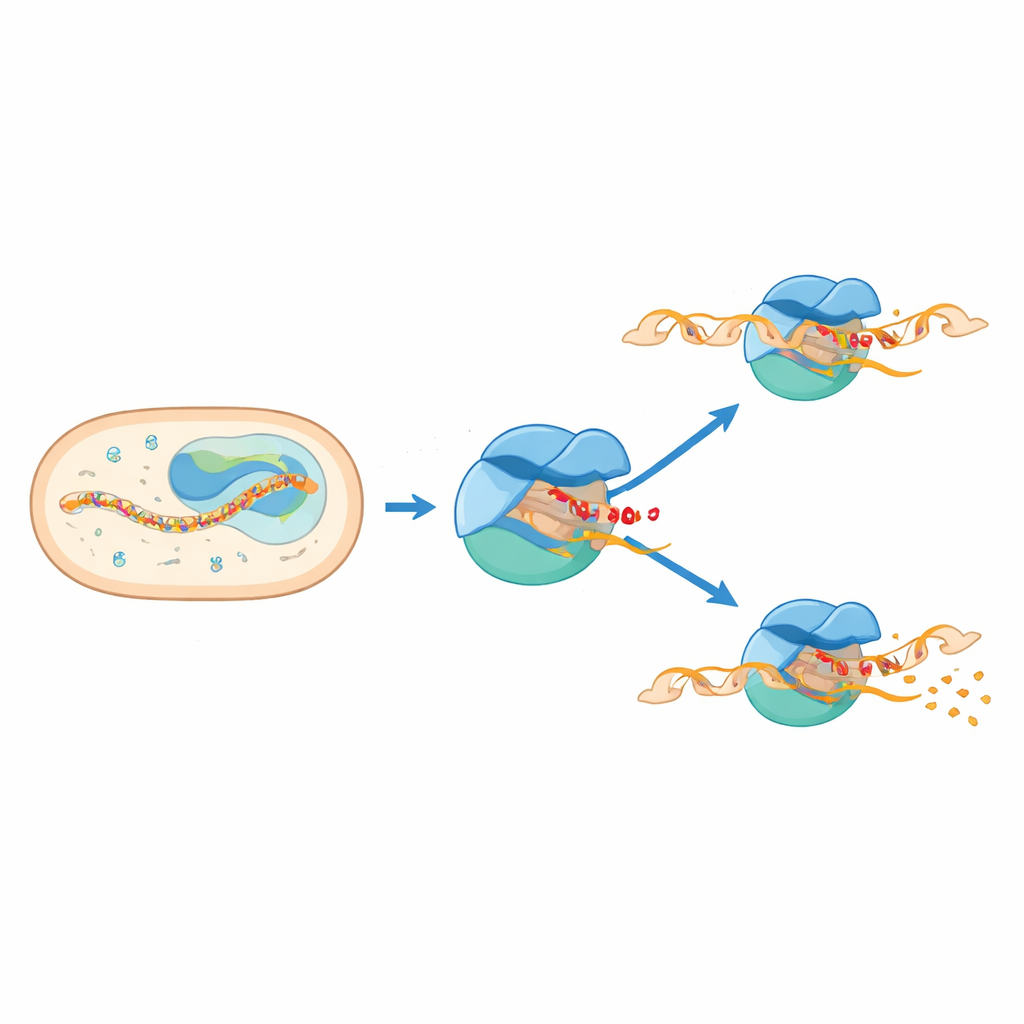
Bei Bakterien bewegt sich eine große Proteinanordnung, die RNA-Polymerase, entlang der DNA, um RNA herzustellen, den ersten Schritt zur Proteinsynthese. Zum Start verbindet sie sich mit Helferproteinen, den Sigma-Faktoren, die sie zu spezifischen Startstellen auf der DNA leiten und helfen, eine kleine „Blase“ in der Doppelhelix zu öffnen. Für Mycobacterium tuberculosis ist ein solcher Helfer, Sigma E genannt, besonders wichtig, wenn das Bakterium unter Stress außerhalb seiner inneren Zellmembran steht. Ein weiterer Faktor, CarD, trägt dazu bei, die offene DNA-Blase zu stabilisieren. Gemeinsam bilden diese Komponenten einen Initiationskomplex, der die ersten Bausteine der RNA herstellt, bevor er entweder die Herstellung einer vollständigen RNA zusichert oder den Versuch aufgibt und kurze RNA-Fragmente freisetzt.
Eine verborgene Pause bei sechs oder sieben Nukleotiden Länge
Frühere biochemische und Einzelmolekülstudien deuteten darauf hin, dass die RNA-Polymerase oft sehr früh pausiert, wenn der neu entstehende RNA-Strang nur sechs oder sieben Bausteine lang ist. Diese Pausen sind jedoch extrem kurz und schwer direkt zu beobachten, weshalb bisher keine hochauflösenden Strukturen vorlagen. In dieser Studie nutzten die Autoren Kryo-Elektronenmikroskopie, um mehrere Zustände der Initiationsmaschinerie von M. tuberculosis einzufrieren und zu visualisieren. Sie konstruierten DNA–RNA-Gerüste, die den Komplex einfrieren, wenn die RNA sechs oder sieben Einheiten lang ist, und lösten Strukturen für drei Hauptzustände: zwei „reguläre“ Initiationskomplexe und einen deutlich pausierten Initiationskomplex.
Wenn zwei Teile der Maschine zusammenstoßen
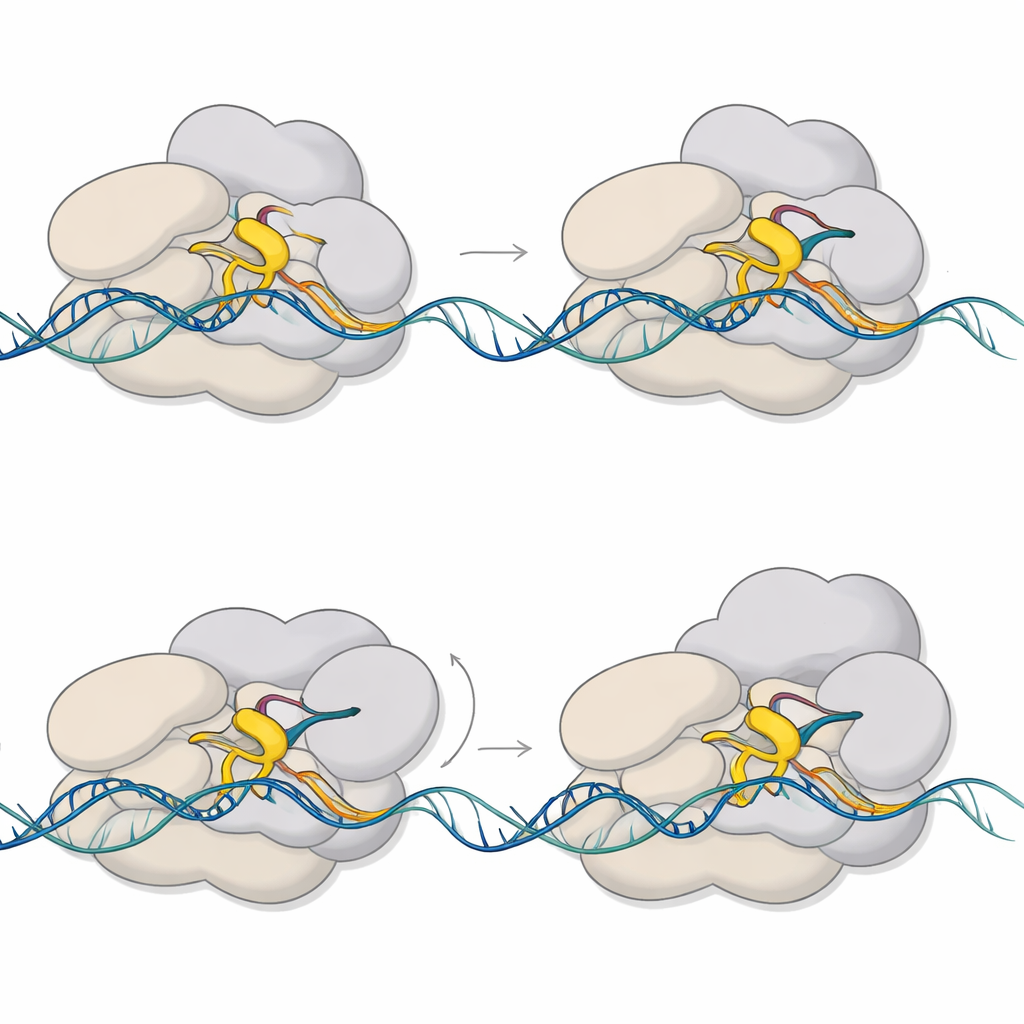
Die Strukturen zeigen, dass die Pause entsteht, wenn zwei Teile der Maschinerie versuchen, denselben Raum zu besetzen. Ein flexibler Abschnitt von Sigma E, bekannt als Region 3.2, ragt in den Kanal hinein, durch den die wachsende RNA passieren muss, um das Enzym zu verlassen. Wenn die RNA auf sechs oder sieben Einheiten anwächst, kollidiert ihre vordere Spitze mit dieser hervortretenden Schleife. Dieser Zusammenstoß erzwingt eine Schwenkbewegung eines großen Moduls innerhalb der RNA-Polymerase und verformt ein zentrales Strukturelement, die Brückenhelix. Gleichzeitig wird die DNA stromaufwärts der aktiven Stelle nach innen gezogen und teilweise entwunden, was eine „eingeschnürte“ und geknickte Blase erzeugt. Diese gekoppelten Bewegungen verriegeln den Komplex in einem pausierten, halb vorgerückten Zustand, der mechanische Spannung speichert.
Ein formwandelnder Helfer stabilisiert die Blase
CarD, der Zusatzfaktor, spielt sich als vielseitiger heraus als bislang angenommen. Im nicht-pausierten Initiationskomplex klemmt CarD in die Minor-Groove eines DNA-Strangs am Rand der Blase und hilft so, die Blase offen zu halten, damit die RNA-Polymerase mit der Synthese beginnen kann. Im pausierten Komplex verschiebt sich CarD und umfasst stattdessen den gegenüberliegenden, nicht als Vorlage dienenden DNA-Strang; zusammen mit Sigma E klemmt es die eingeschnürte Blase enger ein. Biochemische Tests zeigen, dass CarD die Sigma-E-abhängige Transkription verstärkt und beeinflusst, wie viele RNA-Moleküle sich im Stadium von sechs bis sieben Einheiten ansammeln. Diese Befunde deuten darauf hin, dass CarD sowohl den initial offenen Zustand stabilisiert als auch dem pausierten Komplex hilft, ein vorzeitiges Zusammenfallen zu vermeiden.
Eine Kontrollstation zwischen Scheitern und Verpflichtung
Durch den Vergleich hochauflösender Strukturen, die auf teilweise vorgöffneter DNA gebildet wurden, mit niedrig aufgelösten Strukturen, die auf vollständig gepasster DNA zusammengesetzt sind, zeigen die Autoren, dass die gleichen grundlegenden pausierten Formen auch unter natürlicheren Bedingungen auftreten. Sie schlagen vor, dass die Kollision zwischen der wachsenden RNA und der Sigma-3.2-Schleife eine energiegeladene Kontrollstation bei sechs bis sieben RNA-Einheiten schafft. Aus diesem gespannten Zustand kann der Komplex zwei Hauptwege einschlagen: Er kann die kurze RNA freigeben und zurücksetzen — ein abbruchartiger Versuch — oder er kann die gespeicherte Spannung nutzen, um sich vom Promotor zu befreien und in eine stabile, langlebige RNA-Produktion überzugehen. Das Umpositionieren von CarD und das Nachlassen des Haltegriffs des Sigma-Faktors über die stromaufwärts gelegene DNA scheinen diese Entscheidung zu steuern.
Warum das für Tuberkulose wichtig ist
Für eine interessierte Leserschaft lautet die Kernaussage: Das Tuberkulosebakterium schaltet Gene nicht einfach wie ein Licht an. Stattdessen zögert es bei einer winzigen RNA-Länge und nutzt eine kurze mechanische Pause als Entscheidungspunkt zwischen Abbruch und der Verpflichtung zu einer vollständigen Genaktivierung. Diese Arbeit fängt diese Pause in atomarer Detailgenauigkeit ein und zeigt, wie eine kleine bewegliche Schleife, ein schwenkender Kern und eine umgestaltete DNA-Blase zusammen eine steuerbare Kontrollstation bilden. Da Sigma E und CarD zentral dafür sind, wie M. tuberculosis auf Stress reagiert, könnten diese Erkenntnisse Forschern langfristig helfen, Wirkstoffe zu entwerfen, die diesen frühen Schritt blockieren und damit die Anpassungs- und Überlebensfähigkeit des Bakteriums schwächen.
Zitation: Zheng, L., Xu, K. Structural basis of pausing during transcription initiation in mycobacterium tuberculosis. Nat Commun 17, 2197 (2026). https://doi.org/10.1038/s41467-026-69104-w
Schlüsselwörter: Transkriptionsinitiation, RNA-Polymerase-Pausierung, Mycobacterium tuberculosis, Sigma-Faktoren, Cryo-EM