Clear Sky Science · de
Akute Peritonitis-induzierte adipöse CD127+ ILC1s exprimieren PD-L1 und mildern Entzündungen bei Mäusen
Warum Bauchfett helfen kann, tödliche Infektionen zu bekämpfen
Wenn Bakterien aus einem eingerissenen Darm in die Bauchhöhle gelangen, kann der Körper in einen lebensbedrohlichen Zustand namens Sepsis abgleiten. Diese Studie zeigt einen unerwarteten Verbündeten in diesem Kampf: eine spezielle Gruppe von Immunzellen, die im Bauchfett verborgen sind, früh in die Infektion einwandern und als eingebauter Bremsmechanismus gegen außer Kontrolle geratene Entzündungen wirken. Das Verständnis, wie diese Zellen funktionieren, könnte neue Behandlungsansätze inspirieren, die gefährliche Infektionen beruhigen, ohne das Immunsystem komplett auszuschalten.
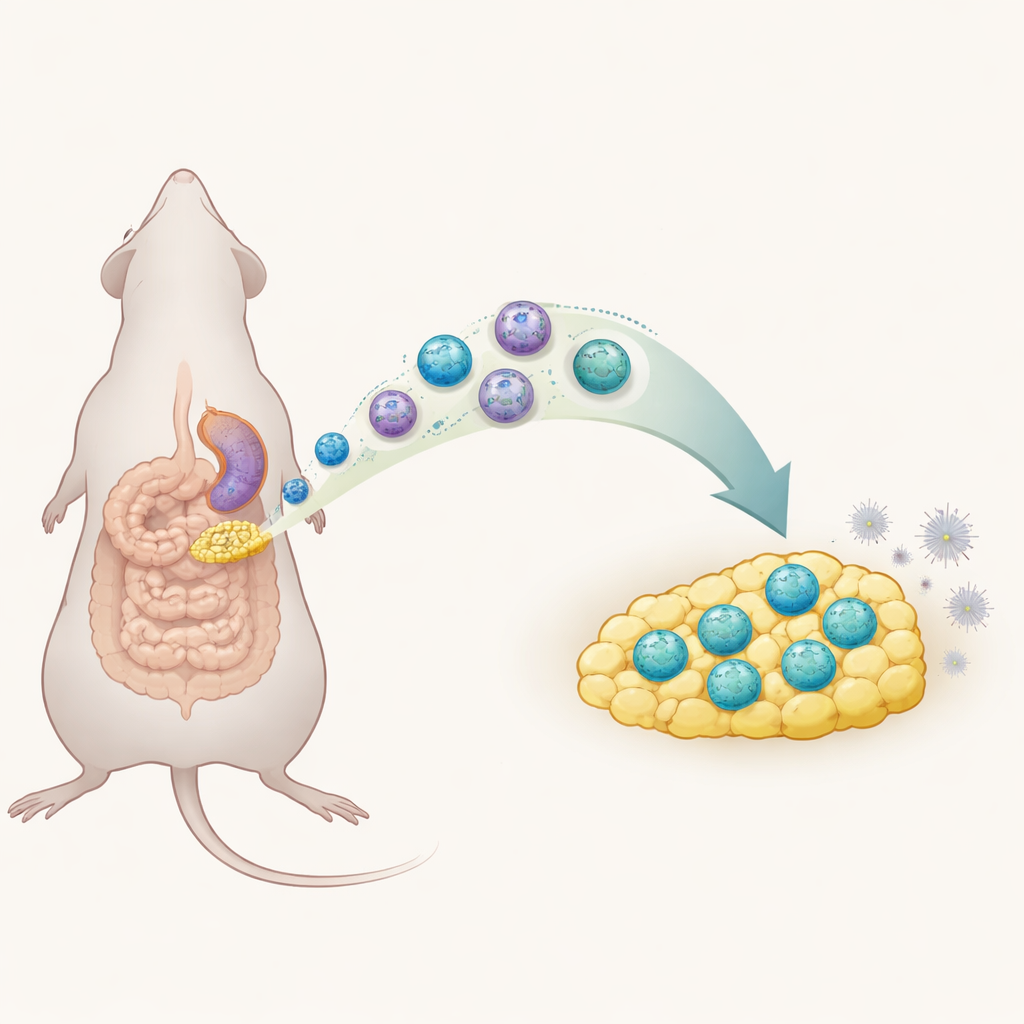
Ein gefährliches Leck im Bauchraum
Peritonitis tritt auf, wenn die Auskleidung des Bauchraums entzündet ist, meist weil Bakterien aus einem perforierten Darm austreten. Wenn dieser frühe Entzündungssturm nicht kontrolliert wird, können Patientinnen und Patienten eine Sepsis entwickeln, die trotz moderner Behandlung immer noch etwa einen von fünf Betroffenen tötet. Ärztinnen und Ärzte können die Infektion chirurgisch und mit Antibiotika behandeln, doch es gibt wenige Mittel, die körpereigene Immunreaktion vor schädlichem Überschießen zu bewahren. Das Fett, das über dem Darm liegt, das sogenannte mesenteriale Fettgewebe, ist dafür bekannt, zu Schadensherden im Darm hin zu strömen, was darauf hindeutet, dass es eine aktive Rolle in dieser frühen Immunantwort spielt.
Verborgene Wächter im Bauchfett
In den letzten Jahren haben Wissenschaftlerinnen und Wissenschaftler „angeborene lymphoide Zellen“ entdeckt, schnell reagierende Immunwächter, die in vielen Geweben leben. Eine Untergruppe, die Gruppe‑1‑ILCs, hilft normalerweise, starke Entzündungsreaktionen auszulösen. In dieser Mausstudie verwendeten die Forschenden ein standardisiertes chirurgisches Peritonitismodell, um zu untersuchen, wie sich diese Zellen im mesenterialen Fett verhalten. Sie fanden heraus, dass sechs Stunden nach der Verletzung das Fett mit Entzündungssignalen aufleuchtete und ein Anstieg von ILC1‑Zellen stattfand, während andere verwandte Zelltypen kaum verändert waren. Dieses Timing stimmte mit dem Höhepunkt der Erkrankung bei den Tieren überein und legt nahe, dass ILC1s eng mit der frühen Entzündungsphase im Bauch verbunden sind.
Wandernde Zellen, die ihre Natur ändern
Bei tiefergehender Analyse nutzte das Team fortgeschrittene Einzelzellprofile, um die ILC1‑Population in Untergruppen zu unterteilen. Unter normalen Bedingungen fehlte den meisten Bauchfett‑ILC1s ein Molekül namens CD127 auf ihrer Oberfläche. Während der akuten Peritonitis tauchte jedoch eine neue Gruppe von CD127‑positiven ILC1s auf und vermehrte sich. Diese Neuankömmlinge produzierten weniger des stark entzündungsfördernden Signals Interferon‑gamma als ihre CD127‑negativen Verwandten und zeichneten sich damit durch zurückhaltenderes Verhalten aus. Die Forschenden zeigten, dass viele dieser Zellen sich nicht einfach vor Ort teilten: Stattdessen wanderten ILC1s aus der Milz über die Blutbahn in das mesenteriale Fett, teils gelenkt durch ein chemisches „Homing“-Signal namens CXCL10 und dessen Rezeptor CXCR3. Einmal im Fett, änderten sie ihre Oberflächenmarker, gewannen CD127 und nahmen diese ruhigere, eher regulatorische Identität an.
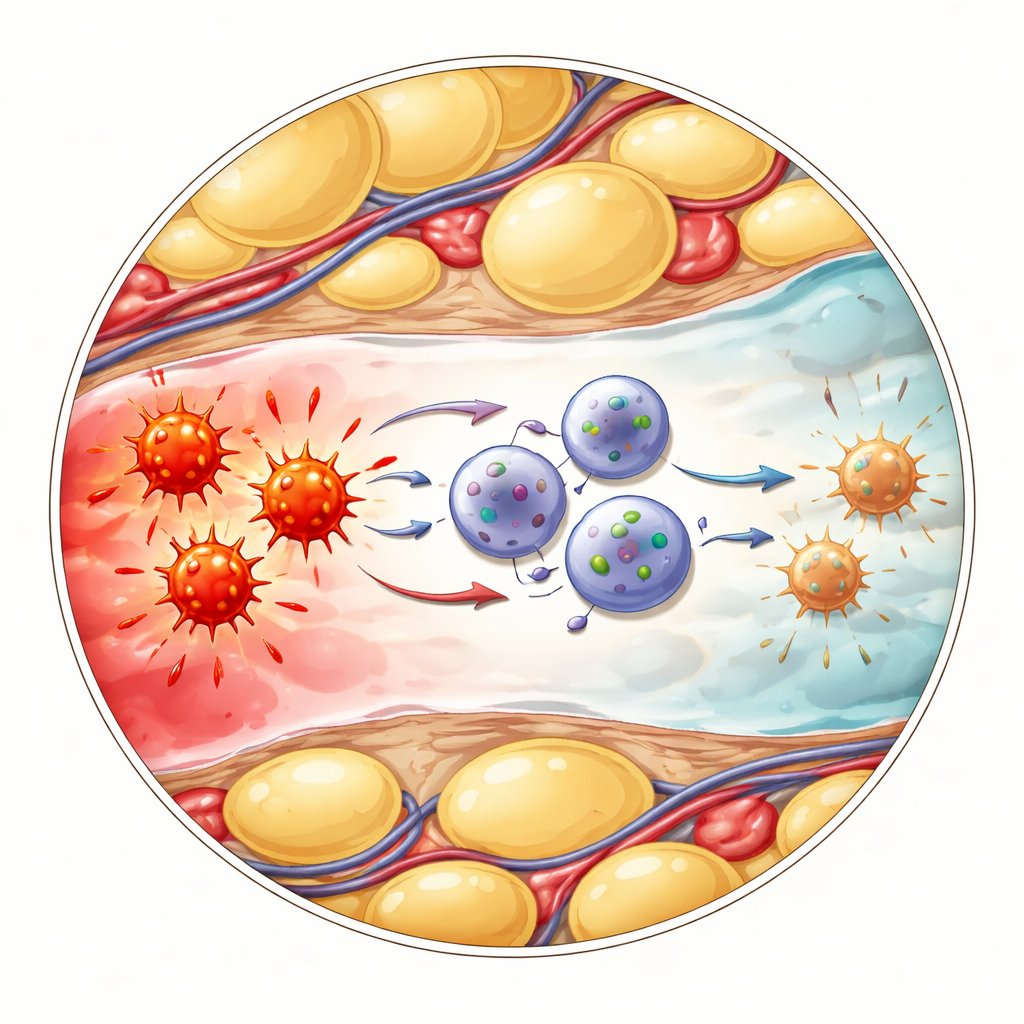
Wie beruhigende Zellen mit feurigen Zellen kommunizieren
Die nächste Frage war, wie diese veränderten ILC1s die Entzündung tatsächlich dämpfen. Die Forschenden konzentrierten sich auf eine andere Immunzellgruppe, die gamma‑delta‑T‑Zellen, die schnell auf Gefahr reagieren und große Mengen des Alarmmoleküls TNF freisetzen können. Einzelzellanalyse deutete darauf hin, dass CD127‑positive ILC1s und gamma‑delta‑T‑Zellen über einen bekannten „Brems“-Weg über die Oberflächenproteine PD‑L1 und PD‑1 interagieren. Im entzündeten Bauchfett steigerten die neu angekommenen ILC1s stark PD‑L1, während benachbarte gamma‑delta‑T‑Zellen hohe PD‑1‑Spiegel zeigten. Als das Team PD‑1 mit Antikörpern blockierte, setzten gamma‑delta‑T‑Zellen mehr TNF frei, was bestätigte, dass dieser Kontakt normalerweise ihre entzündliche Produktion einschränkt. Ebenso litten genetisch veränderte Mäuse, denen ILC1s fehlten, an schwererer Erkrankung, höheren Entzündungsmarkern und mehr TNF aus gamma‑delta‑T‑Zellen — Effekte, die durch direkte Blockade von TNF gemildert werden konnten.
Was das für künftige Therapien bedeutet
Die Autorinnen und Autoren fassen diese Befunde zu einer „Milz‑zu‑Bauchfett“-Achse zusammen: Kurz nachdem Bakterien in die Bauchhöhle gelangt sind, verlassen ILC1s die Milz, wandern ins mesenteriale Fett und verwandeln sich dort in CD127‑ und PD‑L1‑reiche Zellen, die die TNF‑Produktion von gamma‑delta‑T‑Zellen dämpfen. Diese spezialisierten ILC1s schüren die Flammen also nicht, sondern fungieren als lokale Friedenstruppen, verhindern ein Überschießen der Entzündung und helfen möglicherweise, das Fortschreiten einer Peritonitis zur lebensbedrohlichen Sepsis zu stoppen. Langfristig könnten Wirkstoffe, die diesen regulatorischen Kreislauf im Bauchfett stärken oder nachahmen, einen neuen Weg bieten, schwere Infektionen zu behandeln — indem die Immunantwort so abgestimmt wird, dass sie stark genug bleibt, um Erreger zu bekämpfen, aber nicht so stark, dass sie die Patientin oder den Patienten gefährdet.
Zitation: Nagata, R., Akama, Y., Goncalves, P. et al. Acute peritonitis-induced adipose CD127+ ILC1s express PD-L1 and ameliorate inflammation in mice. Nat Commun 17, 2391 (2026). https://doi.org/10.1038/s41467-026-69100-0
Schlüsselwörter: Peritonitis, angeborene lymphoide Zellen, mesenteriales Fettgewebe, Immunregulation, Sepsis