Clear Sky Science · de
Verbesserte Erkennung von Enhancer‑Promoter‑Schleifen durch Normalisierungsmethoden für Chromatin‑Interaktionsdaten
Die verborgenen Schleifen in unserer DNA sichtbar machen
In jeder Zelle falten und schleifen sich lange DNA‑Stränge im dreidimensionalen Raum, wodurch weit auseinanderliegende Bereiche des Genoms in engen Kontakt geraten. Manche dieser Schleifen verbinden physikalisch Schalter, sogenannte Enhancer, mit den Genen, die sie steuern, und beeinflussen so die Entwicklung von Zellen und das Entstehen von Krankheiten wie Krebs. Dieser Artikel stellt eine neue rechnerische Methode vor, Raichu, die diese subtilen regulatorischen Schleifen in genomweiten Experimenten deutlich leichter nachweisbar macht und so ein schärferes Bild davon liefert, wie DNA‑Faltung und Genaktivität zusammenhängen.
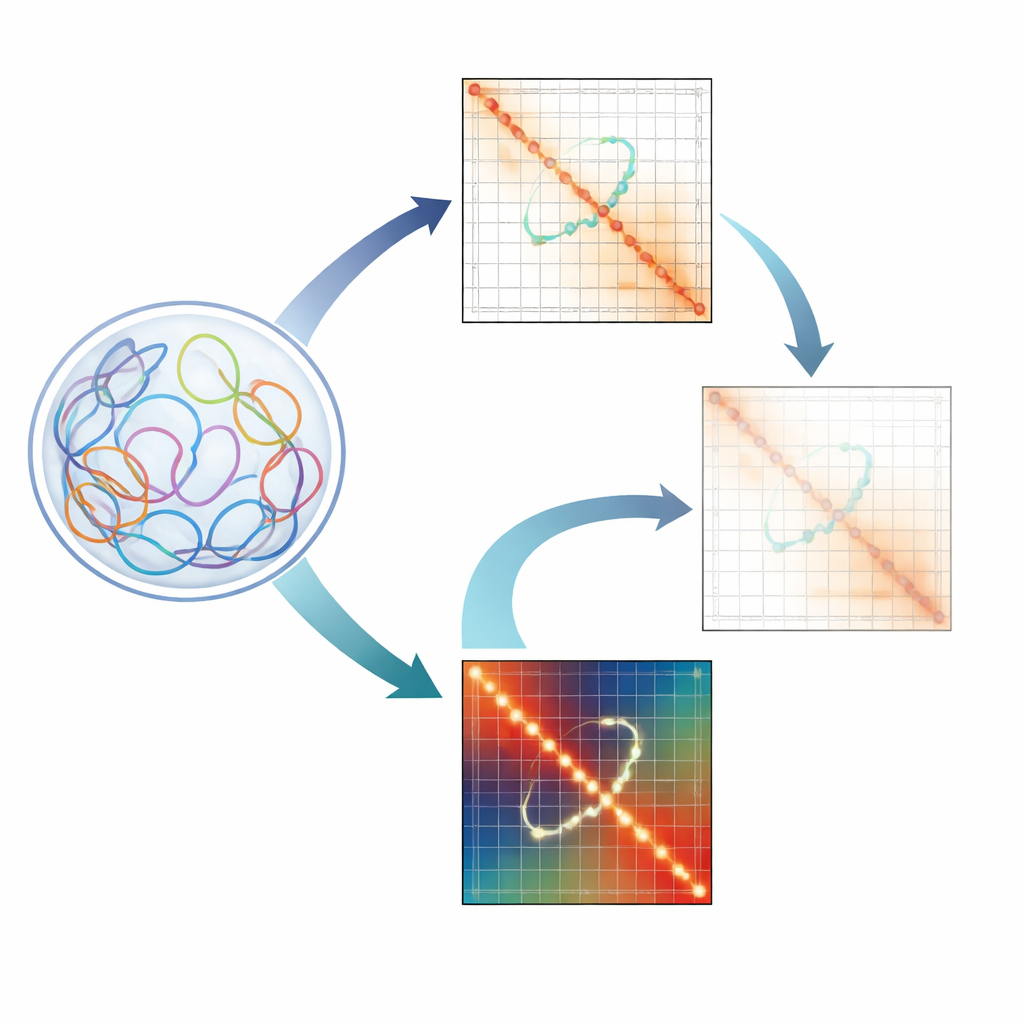
Warum winzige DNA‑Schleifen wichtig sind
Unsere Genome sind nicht wie gerade Buchstabenketten angeordnet. Stattdessen knäueln sie sich zu einer komplexen 3D‑Struktur im Zellkern. In diesem gefalteten Zustand können weit entfernte Genomebereiche aufeinandertreffen und Chromatin‑Schleifen bilden. Manche Schleifen dienen als Gerüst, das ganze Nachbarschaften des Genoms organisiert. Andere sind regulatorische Schleifen, die Promotoren von Genen mit entfernten Enhancern verbinden, die deren Aktivität verstärken. Die Störung solcher regulatorischer Schleifen wurde mit Entwicklungsstörungen und Krebs in Verbindung gebracht, weshalb Forscher daran interessiert sind, sie detailliert zu kartieren.
Die Herausforderung beim Lesen von 3D‑Genomkarten
Techniken wie Hi‑C und verwandte Methoden erfassen Millionen bis Milliarden von DNA‑DNA‑Kontakten und fassen sie in Heatmaps zusammen, wobei jedes Pixel widerspiegelt, wie häufig sich zwei Genomregionen treffen. Diese Karten sind jedoch von technischen Eigenheiten durchzogen: Manche Regionen sind leichter zu erfassen als andere, etwa wegen Sequenzzusammensetzung, wie gut sie sich alignen lassen oder wie sie im Experiment geschnitten werden. Um die Daten zu bereinigen, verwenden Forscher Normalisierungsmethoden wie ICE und KR, die die Karten ausgleichen, sodass jede Region scheinbar gleich gut sichtbar ist. Während diese Werkzeuge große Merkmale wie breite Domänen und starke Struktur‑Schleifen schärfen, zeigen die Autoren, dass sie unbeabsichtigt die schwächeren, aber biologisch wichtigen Enhancer‑Promoter‑Schleifen auswaschen.
Ein neuer Weg, das Signal zu säubern
Raichu verfolgt einen anderen Ansatz zur Bereinigung von Chromatin‑Kontaktdaten. Anstatt jede Genomregion gleich sichtbar erscheinen zu lassen, modelliert es jede Interaktion als Summe von drei Komponenten: einen allgemeinen Abfall der Kontaktfrequenz mit zunehmender chromosomaler Distanz, einen ortsspezifischen Bias und ein verbleibendes Signal, das speziell für diesen Kontakt ist. Mithilfe eines Optimierungsalgorithmus schätzt Raichu das Bias‑Muster, das die beobachteten Daten am besten erklärt, während der allgemeine distanzabhängige Trend fixiert bleibt. Die Kontakte werden dann korrigiert, indem diese Bias‑Werte herausdividiert werden. So bleibt der natürliche globale Abfall der Interaktionen erhalten, während technische Verzerrungen selektiv korrigiert werden, sodass klarere Signale realer, spezifischer DNA‑Kontakte zurückbleiben.
Aufdecken von Tausenden zuvor übersehenen regulatorischen Schleifen
Als die Autoren Raichu auf tief sequenzierte menschliche und Maus‑Datensätze anwendeten, deckte es fast doppelt so viele Chromatin‑Schleifen auf wie Standardmethoden, während nahezu alle zuvor bekannten Schleifen weiterhin wiedergefunden wurden. Die zusätzlichen von Raichu entdeckten Schleifen waren stark angereichert für biochemische Markierungen aktiver Enhancer und Promotoren sowie für die Bindung von Transkriptionsfaktoren, die die Genaktivität steuern. Viele dieser Schleifen wurden unabhängig durch andere 3D‑Genomtechnologien und sogar durch hochauflösende Bildgebung gestützt, was bestätigt, dass sie reale physische Nähe im Zellkern widerspiegeln. Wichtig ist, dass Raichu diesen Vorteil auch behielt, wenn die Daten ausgedünnt wurden, um niedrigere Sequenziertiefen zu simulieren, bei spezialisierten Mapping‑Methoden wie Micro‑C und region capture Micro‑C und sogar beim Zusammenlegen kleiner Zahlen einzelner Zellen.
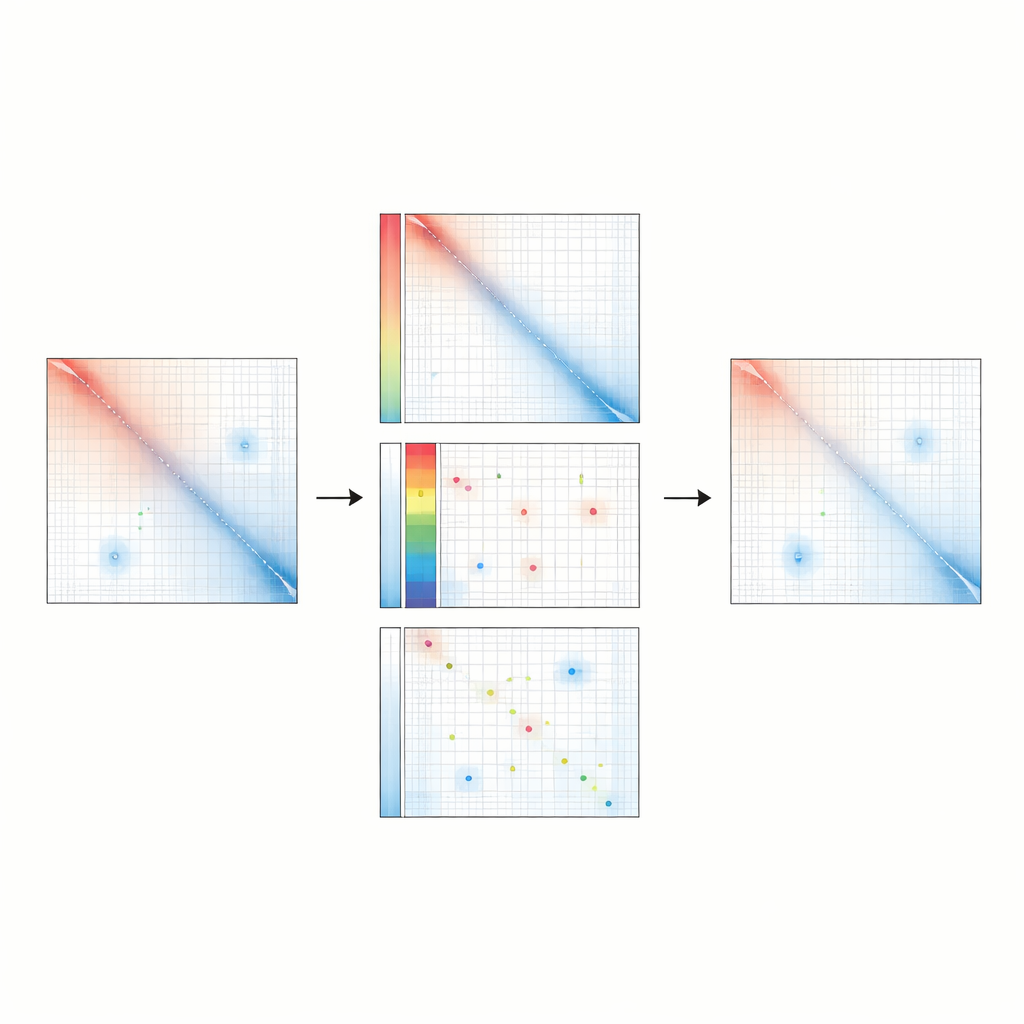
Feine Veränderungen und evolutionäre Muster aufdecken
Weil Raichu besonders empfindlich für regulatorische Schleifen ist, eignet es sich besser, sinnvolle Unterschiede zwischen Bedingungen zu erkennen, die sonst ähnlich erscheinen könnten. In einem gentechnisch veränderten menschlichen Zellmodell mit einer Leukämie‑Risikovarianz entdeckte Raichu neue Schleifen, die nur im Risiko‑Zustand auftauchten, dabei Schlüsselgene mit ihren Enhancern verbanden und mit Verschiebungen in der Genaktivität übereinstimmten. Zwischen Maus‑ und menschlichen neuralen Vorläuferzellen fand Raichu Tausende von Enhancer‑Promoter‑Schleifen, die zwischen den Arten konserviert waren und oft entfernte Enhancer mit Genen verknüpften, die an der Gehirnentwicklung beteiligt sind. Diese Befunde deuten darauf hin, dass viele wichtige regulatorische Kontakte bislang im Verborgenen lagen, verdeckt durch frühere Normalisierungsansätze.
Was das für die zukünftige Genomforschung bedeutet
Für eine nicht‑fachliche Leserschaft lautet die Kernbotschaft, dass die Art und Weise, wie wir große genomische Datensätze verarbeiten, stark beeinflussen kann, welche biologische Signale wir sehen. Indem der Bereinigungsschritt für 3D‑Genomkarten neu gedacht wird, stellt Raichu schwache, aber bedeutende Signale wieder her, die Schalter von Genen mit ihren Zielen verbinden. Das erleichtert das Nachverfolgen, wie DNA‑Faltung die Genaktivität in Gesundheit und Krankheit steuert — von Einzelzellen bis zu ganzen Geweben und zwischen Arten. Wenn immer mehr Studien Raichu einsetzen, können Forscher reichhaltigere Karten der Enhancer‑Promoter‑Kommunikation und ein klareres Bild davon erwarten, wie Veränderungen in der Genomarchitektur zur Entwicklung, zu Krebs und anderen komplexen Erkrankungen beitragen.
Zitation: Wang, X., Shi, D., Xue, F. et al. Boosting the detection of enhancer-promoter loops via normalization methods for chromatin interaction data. Nat Commun 17, 2299 (2026). https://doi.org/10.1038/s41467-026-69082-z
Schlüsselwörter: 3D‑Genom‑Organisation, Enhancer‑Promoter‑Schleifen, Hi‑C‑Datenanalyse, Chromatin‑Normalisierung, Genregulation