Clear Sky Science · de
Tiefes Lernen steuert autonome molekulare Reaktionen mit Einzelbindungsselektivität in tetra-bromierten Porphyrinen auf Au(111)
Maschinen beibringen, Moleküle eine Bindung nach der anderen zu verändern
Chemiker haben lange davon geträumt, Reaktionen mit der Präzision eines Uhrmachers zu steuern und genau eine Bindung in genau einem Molekül auf Befehl zu verändern. Diese Studie zeigt, wie künstliche Intelligenz einen großen Schritt in Richtung dieses Traums machen kann: ein computergesteuertes System, das einzelne Moleküle auf einer Oberfläche findet und eigenständig ausgewählte chemische Bindungen bricht, ohne dass ein Mensch an den Reglern dreht. Eine solche Kontrolle könnte es letztlich erlauben, neue Materialien Atom für Atom „zu schreiben“ und exotische molekulare Strukturen zu erforschen, die mit herkömmlicher Kolben‑und‑Reagenzglas‑Chemie kaum erreichbar sind.
Warum Einzelbindungen wichtig sind
Die meisten chemischen Reaktionen laufen im Bulk ab: unzählige Moleküle kollidieren und ordnen sich nach den allgemeinen Regeln der Thermodynamik und Kinetik neu. Das funktioniert gut für viele Anwendungen, ist aber, als würde man Marmor mit einem Hammer statt mit einem feinen Meißel bearbeiten. Könnten Wissenschaftler eine einzelne Bindung in einem einzelnen Molekül gezielt auswählen und entscheiden, ob sie bleibt oder bricht, ließen sich maßgeschneiderte molekulare Muster für die nächste Generation von Elektronik, Quantenbauelementen und extrem dichter Datenspeicherung herstellen. Rastertunnelmikroskope (STMs) erlauben es Expertinnen und Experten bereits, einzelne Moleküle auf Metalloberflächen mit atomarer Auflösung zu sehen und anzutippen. Bislang beruhten solche Reaktionen aber auf menschlicher Intuition und Geduld, was die Reproduzierbarkeit, Skalierbarkeit und Programmierbarkeit des Verfahrens einschränkt.
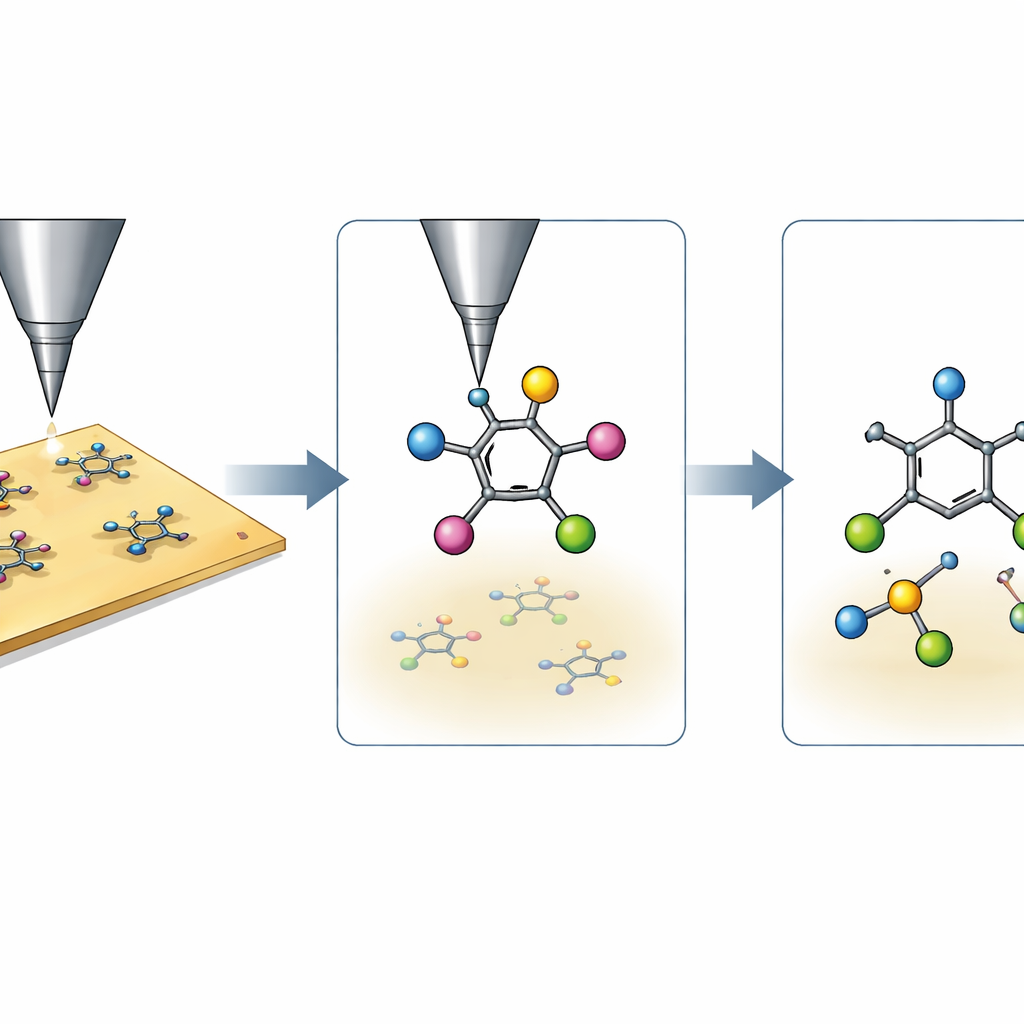
Das Mikroskop in ein selbstfahrendes Labor verwandeln
Die Autorinnen und Autoren verwandeln ein konventionelles STM in eine Art selbstfahrendes Chemielabor, indem sie mehrere Deep‑Learning‑Werkzeuge über dem Instrument schichten. Zuerst durchsucht ein Computer‑Vision‑Modul große Bereiche einer Goldoberfläche, um automatisch isolierte Zielmoleküle zu erkennen und zoomt dann für eine Nahaufnahme heran. Weitere neuronale Netze verfolgen die Kontur jedes Moleküls, bestimmen seine Orientierung und inspizieren vier spezifische Ecken, an denen Bromatome sitzen. Durch die Analyse kleiner Bildausschnitte an diesen Ecken entscheidet das System, ob jedes Brom noch gebunden ist oder bereits in einem früheren Schritt entfernt wurde, und behält so effektiv den „Bindungs‑für‑Bindungs“-Status des Moleküls im Blick, ohne dass ein Mensch die Bilder interpretieren muss.
Ein KI‑Agent, der lernt, Bindungen zu brechen
Sobald das Molekül erkannt und sein aktueller Zustand bekannt ist, wählt ein Verstärkungslernagent die Handlungen aus. Er behandelt jeden Versuch, eine Bindung zu brechen, wie einen Zug in einem komplexen Spiel, wobei die Position der STM‑Spitze, die Spannung und der Strom seine Züge sind und die resultierende molekulare Änderung das Feedback. Das System kodiert die vier Bindungszustände als ein einfaches Vier‑Bit‑Muster und ergänzt einen Code für den gewünschten gesamten Reaktionspfad. Mit einem modernen Algorithmus namens Soft Actor‑Critic lernt der Agent nach und nach, welche Kombinationen aus Spitzenplatzierung und elektrischer Impulsgabe zu einem sauberen Bruch einer einzelnen Kohlenstoff–Brom‑Bindung führen, welche Versuche nichts bewirken und welche das Molekül schädigen oder überreagieren. Es existiert ein enger, sicheres‑und‑effektives Fenster, und in frühen Trainingsphasen scheitern viele Versuche; durch Wiederabspielen und Erweiterung seiner Erfahrungen, einschließlich der Nutzung der vierfachen Symmetrie des Moleküls, konvergiert der Agent zu zuverlässigen Strategien.
Mehrstufige molekulare Wege programmieren
Nach etwa anderthalb Tagen kontinuierlichen Trainings über Hunderte von Reaktionsversuchen kann das System mehrstufige, vorgeplante Reaktionsrouten mit bemerkenswertem Erfolg ausführen. Das Testmolekül, ein tetra‑bromiertes Porphyrin auf einer Goldoberfläche, beginnt mit vier äquivalenten bromhaltigen Armen. Die KI wird angewiesen, verschiedenen schrittweisen Mustern der Bindungsentfernung zu folgen — wie „orthogonal“ oder „Zickzack“ —, von denen jedes durch unterschiedliche Zwischenformen verläuft, bevor es in einem vollständig debromierten Molekül plus vier freien Bromatomen auf der Oberfläche endet. Für jeden Schritt wählt der Agent automatisch, wo die Spitze positioniert werden soll, welche Spannungspulsstärke anzuwenden ist und wie viel Strom zu nutzen ist, überprüft das Ergebnis mit seinem Vision‑System und entscheidet dann über das weitere Vorgehen. Mit der Zeit entdeckt er, dass höhere Spannungen nötig sind, je mehr Brom entfernt wurden, und dass das Platzieren der Spitze direkt über der Zielbindung die Erfolgswahrscheinlichkeit maximiert.
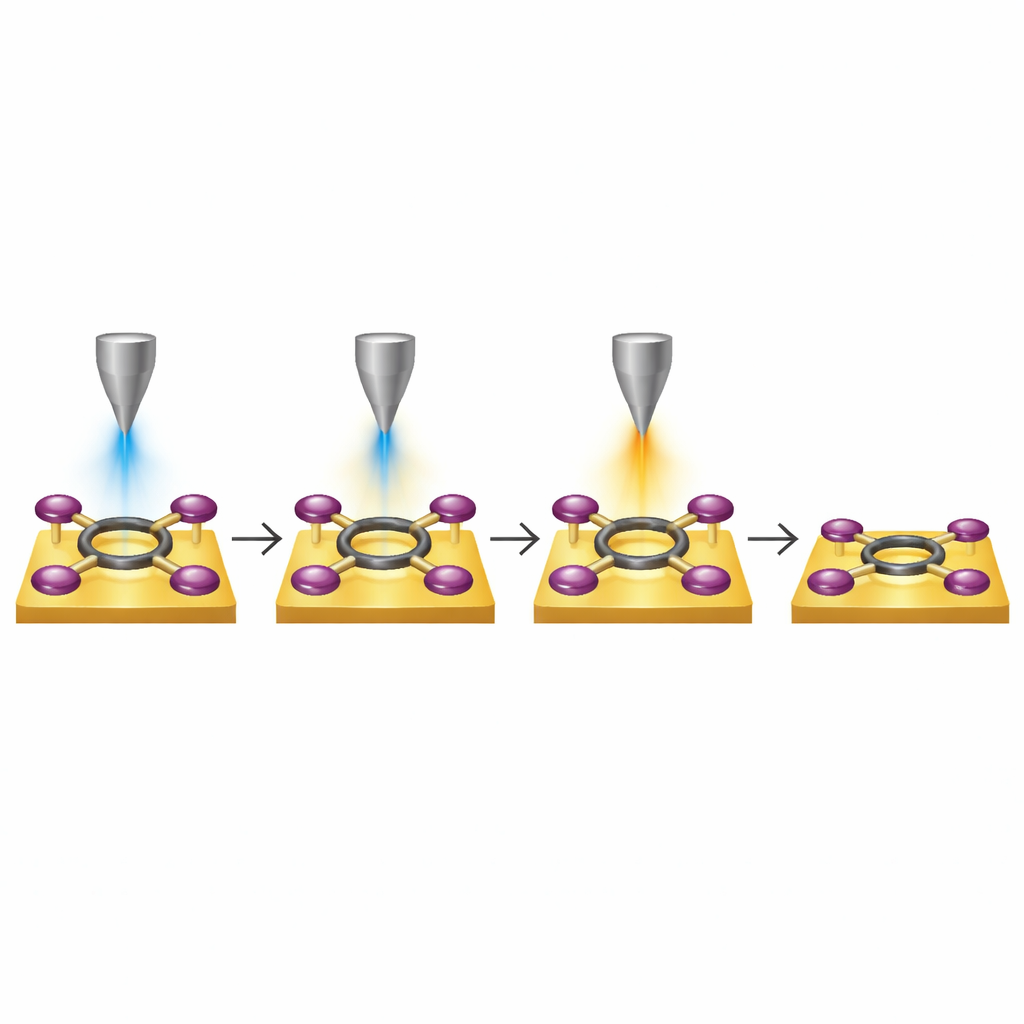
Von Einzelereignissen zur zukünftigen Atom‑für‑Atom‑Fertigung
Die Forschenden zeigen schließlich, dass ihre Plattform das Molekül wiederholt entlang vier unterschiedlicher Reaktionswege leiten kann, während die Selektivität auf Einzelbindungs‑Ebene erhalten bleibt, und erreichen Erfolgsraten, die schrittweise besser werden und in der letzten Bindungsbrechungsstufe nahezu 80 % erreichen. Ebenso wichtig ist, dass sich das System anpasst, wenn sich die mikroskopische Spitze in Form oder Verhalten ändert, und schnell die besten Einstellungen erneut erlernt, statt ins Stocken zu geraten. Für Laien lautet die Kernaussage: Das Mikroskop ist nicht länger nur ein passiver Beobachter, sondern ein aktives, lernendes Werkzeug: Es kann Moleküle finden, entscheiden, welche Bindung zu brechen ist, die passende Kraft anwenden und das Ergebnis selbst verifizieren. Diese Mischung aus präziser Instrumentierung und KI‑Kontrolle weist auf eine Zukunft, in der Wissenschaftler komplexe, atomgenaue Fertigungsaufgaben programmieren und mit Softwareagenten maßgeschneiderte molekulare Strukturen bauen und erkunden können, die von Hand nahezu unmöglich herzustellen wären.
Zitation: Zhu, Z., Huang, Q., Yang, T. et al. Deep learning drives autonomous molecular reactions with single-bond selectivity in tetra-brominated porphyrins on Au(111). Nat Commun 17, 2348 (2026). https://doi.org/10.1038/s41467-026-69080-1
Schlüsselwörter: autonome Chemie, Einzelmolekülreaktionen, Rastertunnelmikroskopie, tiefe verstärkende Lernverfahren, On‑Surface‑Synthese