Clear Sky Science · de
Eine kombinatorische Synthesestrategie zur Entwicklung von Protein-Transportmitteln für Genom-Editierung, die auf die Netzhaut der Maus abzielen
Neue Hoffnung zur Behandlung vererbter Blindheit
Viele Formen vererbter Blindheit beginnen mit einem einzigen fehlerhaften Gen in den lichtempfindlichen Zellen der Augenrückwand. Moderne Gen-Editierwerkzeuge wie CRISPR können theoretisch diese Fehler korrigieren, doch die sichere Zustellung der Editiermaschinerie in die richtigen Zellen war bislang ein großes Hindernis. Diese Studie beschreibt einen neuen Weg, leistungsfähige Gen-Editoren direkt in die Netzhaut von Mäusen zu transportieren, indem speziell konstruierte fettähnliche Partikel verwendet werden, und eröffnet die Aussicht auf einmalige Behandlungen, die bei genetischen Augenerkrankungen das Sehvermögen wiederherstellen könnten.
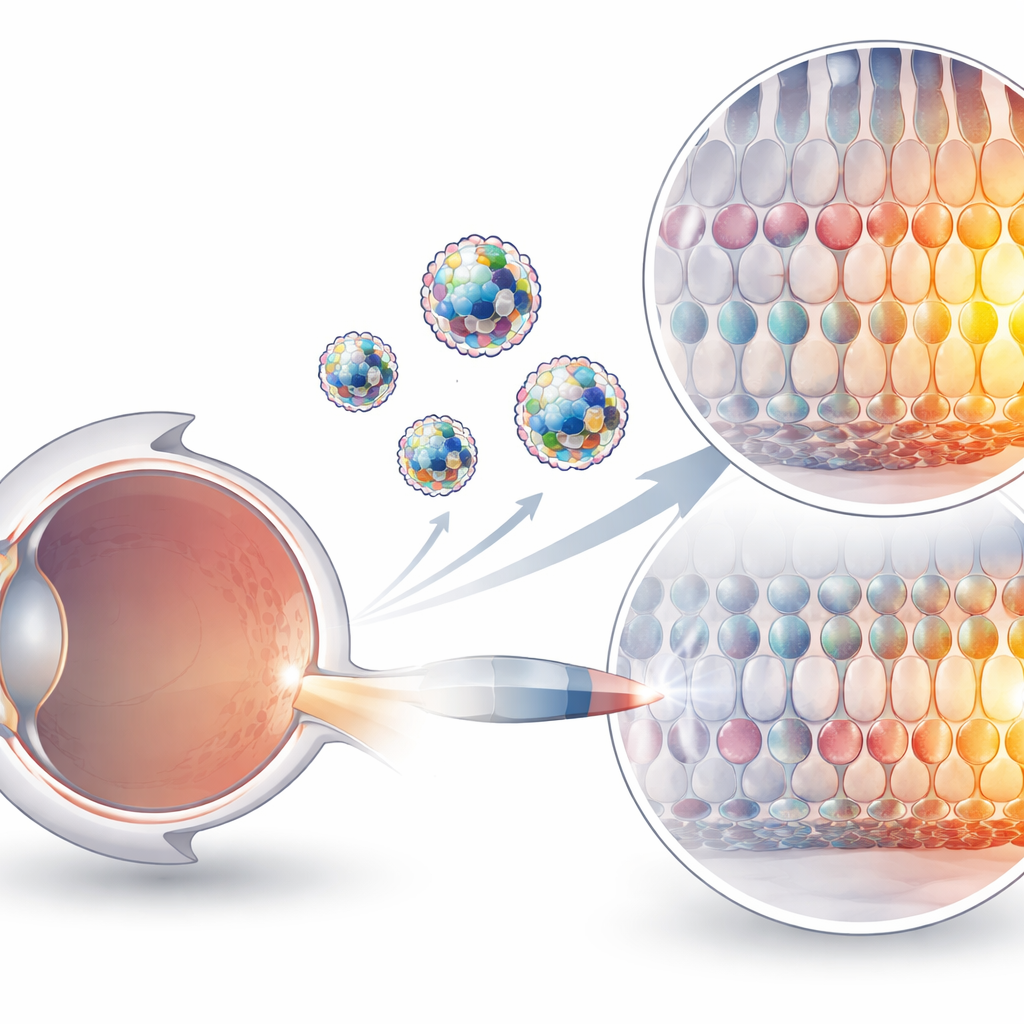
Warum die Lieferung von Gen-Editoren so schwierig ist
CRISPR-basierte Werkzeuge können inzwischen einzelne DNA-Buchstaben verändern, ohne beide Stränge zu schneiden, ein Fortschritt, der sie für die Behandlung genetischer Erkrankungen attraktiv macht. Diese Werkzeuge sind jedoch sperrige Protein–RNA-Komplexe, elektrisch geladen und im Körper empfindlich. Aktuelle Zustellmethoden beruhen größtenteils auf modifizierten Viren oder auf Partikeln, die genetische Baupläne für den Editor transportieren, statt des Editors selbst. Viren können Immunreaktionen auslösen und unterliegen strengen Größenbeschränkungen, während die Lieferung von messenger RNA in der Leber sehr gut funktioniert, in vielen anderen Geweben, einschließlich des Auges, jedoch ineffizient bleibt. Das direkte Injizieren der vorgefertigten Protein–RNA-Komplexe ist konzeptionell sauberer und potenziell sicherer, doch es fehlte an geeigneten Vehikeln, die ihnen helfen, Zellmembranen zu überwinden und ihre Ziele zu erreichen.
Ein farbstoffinspiriertes Shuttle für Proteine
Die Forscher wählten einen unerwarteten Ausgangspunkt: Coomassie Brilliant Blue, ein tiefblauer Farbstoff, der in Biologie-Labors häufig verwendet wird und bereits für bestimmte Augenoperationen zugelassen ist. Dieser Farbstoff bindet sich fest an viele verschiedene Proteine. Das Team verband chemisch Coomassie-»Köpfe« mit fettähnlichen »Schwänzen« und erzeugte so eine Familie neuer Moleküle, die Lipidoide genannt werden. In Wasser neigen diese Lipidoide dazu, Partikel zu bilden, wobei die öligen Teile innen verborgen sind und die Coomassie-Gruppen außen liegen, wo sie Proteine greifen können. Durch Variation der Länge, Verzweigung und Ladung der Schwänze bauten die Wissenschaftler Dutzende von Kandidatenverbindungen, die so entworfen wurden, dass sie einerseits Gen-Editierproteine binden und andererseits mit Zellmembranen interagieren.
Testen der Proteinlieferung in Augen-Zellen
Um herauszufinden, welche Designs tatsächlich funktionierten, verwendete die Gruppe zunächst ein einfaches Testprotein namens Cre-Rekombinase, das in gentechnisch veränderten Zellen und Mäusen einen genetischen Schalter von Grün zu Rot oder umgekehrt umlegt. Mehrere Coomassie-Lipidoide transportierten Cre effizient in kultivierte Zellen und verwandelten große Anteile der Zellen von Grün zu Rot. Nach Injektion unter die Netzhaut von Reportermäusen lösten ausgewählte Verbindungen auffällige Farbwechsel sowohl in der pigmentierten Schicht, die das Sehen unterstützt, als auch in den lichtempfindlichen Photorezeptoren aus, was zeigte, dass die Proteine genau die Zellen erreichten, die bei vielen Erblindungsformen betroffen sind. Diese frühen Experimente zeigten außerdem, dass subtile Änderungen in der Lipidoidstruktur beeinflussen konnten, welche Zelltypen adressiert wurden, was darauf hindeutet, dass zukünftige Versionen für bestimmte Netzhautschichten abgestimmt werden könnten.
Steigerung der Gen-Editierung und Wiederherstellung des Sehens
Anschließend luden die Forscher ihr System mit einem Adenin-Basen-Editor, einer verfeinerten CRISPR-Variante, die die spezifische Einzelbuchstaben-Mutation korrigieren kann, die bei rd12-Mäusen, einem Modell schwerer kindlicher Blindheit, zum Sehverlust führt. Der Editor-Protein–RNA-Komplex drang allein nur schlecht in Zellen ein. Ein Lipidoid mit der Bezeichnung CBB11 verbesserte die Lieferung, neigte jedoch dazu, in Lösung zu verklumpen. Um es zu stabilisieren, betteten die Forscher CBB11 in kleine, gut definierte Liposomen ein—hohle Kugeln aus mehreren Lipidtypen, darunter klinisch verwendete Komponenten aus mRNA-Impfstoffen. In diesen Formulierungen griff CBB11 an der Liposomenoberfläche den Proteinanteil des Editors, während andere Lipide halfen, die RNA-Leitsequenz zu binden, wodurch eine kooperative Hülle entstand, die den gesamten Komplex außen an dem Partikel hielt.
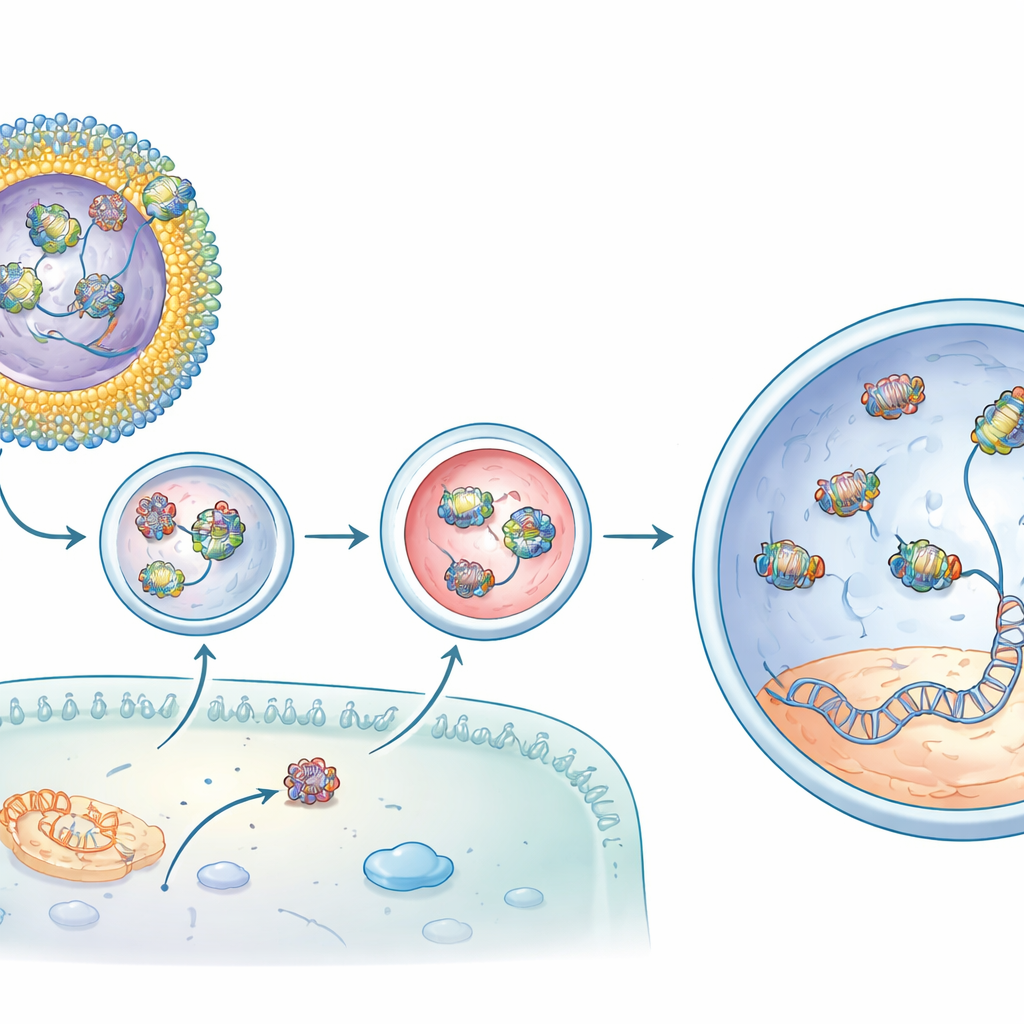
Von molekularer Reparatur zu wiederhergestellten Lichtreaktionen
Als diese CBB11-enthaltenen Liposomen mit dem Baseneditor unter die Netzhaut von rd12-Mäusen injiziert wurden, waren die Ergebnisse eindrucksvoll. Im Vergleich zum allein injizierten Editor steigerte die optimierte Formulierung die gewünschte DNA-Korrektur im Zielgen um deutlich mehr als eine Größenordnung und erzeugte noch höhere Mengen an korrigierter messenger RNA. Chemische Analysen zeigten die Wiederherstellung des lichtempfindlichen retinalen Pigments, das in der Erkrankung fehlt. Am überzeugendsten waren elektrische Aufzeichnungen von den Augen der Tiere, die zeigten, dass ihre Stäbchenzellen einen Großteil ihrer Fähigkeit, auf Dämmerlicht zu reagieren, wiedererlangten—in den besten Fällen bis zu etwa drei Viertel des Signals einer normalen Maus. Off-Target-Veränderungen an anderen Stellen im Genom lagen auf Hintergrundniveau, was darauf hindeutet, dass die Editierung sowohl kraftvoll als auch präzise war.
Was das für künftige Augentherapien bedeuten könnte
Für Nicht-Spezialisten ist die Kernbotschaft, dass die Autoren einen wiederverwendbaren »Shuttlebus« für Gen-Editierproteine gebaut haben, der direkt im lebenden Auge funktioniert. Indem sie sichere, impfstoffähnliche Fettpartikel mit einem proteingriffigen Farbstoff dekorierten, schufen sie ein System, das verschiedene Editoren auf seiner Oberfläche erfassen, in Netzhautzellen liefern, krankheitsverursachende Mutationen korrigieren und nach einer einzigen Behandlung messbar das Sehvermögen von Mäusen wiederherstellen kann. Obwohl weitere Arbeiten nötig sind, um Sicherheit vollständig zu bewerten, das Targeting zu verbessern und die Methode für den Menschen anzupassen, weist diese Plattform auf künftig mögliche einmalige Präzisionsmedikamente für vererbte Netzhauterkrankungen und möglicherweise andere genetische Erkrankungen hin, bei denen lokalisierte, sorgfältige DNA-Reparatur den Unterschied zwischen Blindheit und Sehen ausmachen könnte.
Zitation: Zhang, J., Hołubowicz, R., Smidak, R. et al. A combinatorial synthetic strategy for developing genome-editing protein-delivery agents targeting mouse retina. Nat Commun 17, 2479 (2026). https://doi.org/10.1038/s41467-026-69077-w
Schlüsselwörter: retinale Gentherapie, CRISPR-Basen-Editierung, Liposomen, Proteinlieferung, vererbte Blindheit