Clear Sky Science · de
Einblicke in Struktur und Modulation des menschlichen TWIK-2
Warum dieses winzige Tor in unseren Zellen wichtig ist
Tief im Inneren unserer Zellen steuern mikroskopische Tore aus Proteinen den Fluss geladener Atome und beeinflussen so, wie Nerven feuern, wie sich Blutgefäße verengen und wie unser Immunsystem reagiert. Eines dieser Tore, TWIK-2 genannt, wurde mit einem hohen Blutdruck in der Lunge und schädlicher Entzündung in Verbindung gebracht, doch bislang wussten Forscher nur wenig darüber, wie es aufgebaut ist oder wie man es medikamentös beeinflussen kann. Diese Studie legt die detaillierte Struktur des menschlichen TWIK-2 offen, beschreibt sein elektrisches Verhalten und zeigt Wege auf, wie es für die Entwicklung neuer entzündungshemmender Wirkstoffe gezielt angesteuert werden könnte.
Ein ruhiger Kanal mit großen gesundheitlichen Folgen
TWIK-2 gehört zu einer großen Familie von sogenannten „Leck“-Kaliumkanälen, die durch das Passieren von Kaliumionen über die Zellmembran das Ruhepotenzial der Zellen mitbestimmen. Während andere Familienmitglieder wie TREK- und TASK-Kanäle intensiv untersucht wurden und mit Schmerz und Stimmung in Verbindung stehen, blieb TWIK-2 weitgehend im Dunkeln, weil es schwierig zu messen ist und sich in üblichen Labor‑Systemen schlecht exprimiert. Tier- und Zellstudien verknüpfen TWIK-2 jedoch mit pulmonaler Hypertonie, akutem Lungenversagen, Hörverlust und der Aktivierung eines Immunkomplexes namens NLRP3-Inflammasom, der bei Sepsis und anderen Erkrankungen schädliche Entzündungen antreibt. Das Verständnis von TWIK-2 ist daher sowohl für die Grundlagenbiologie als auch für das Design gezielter Therapien entscheidend.
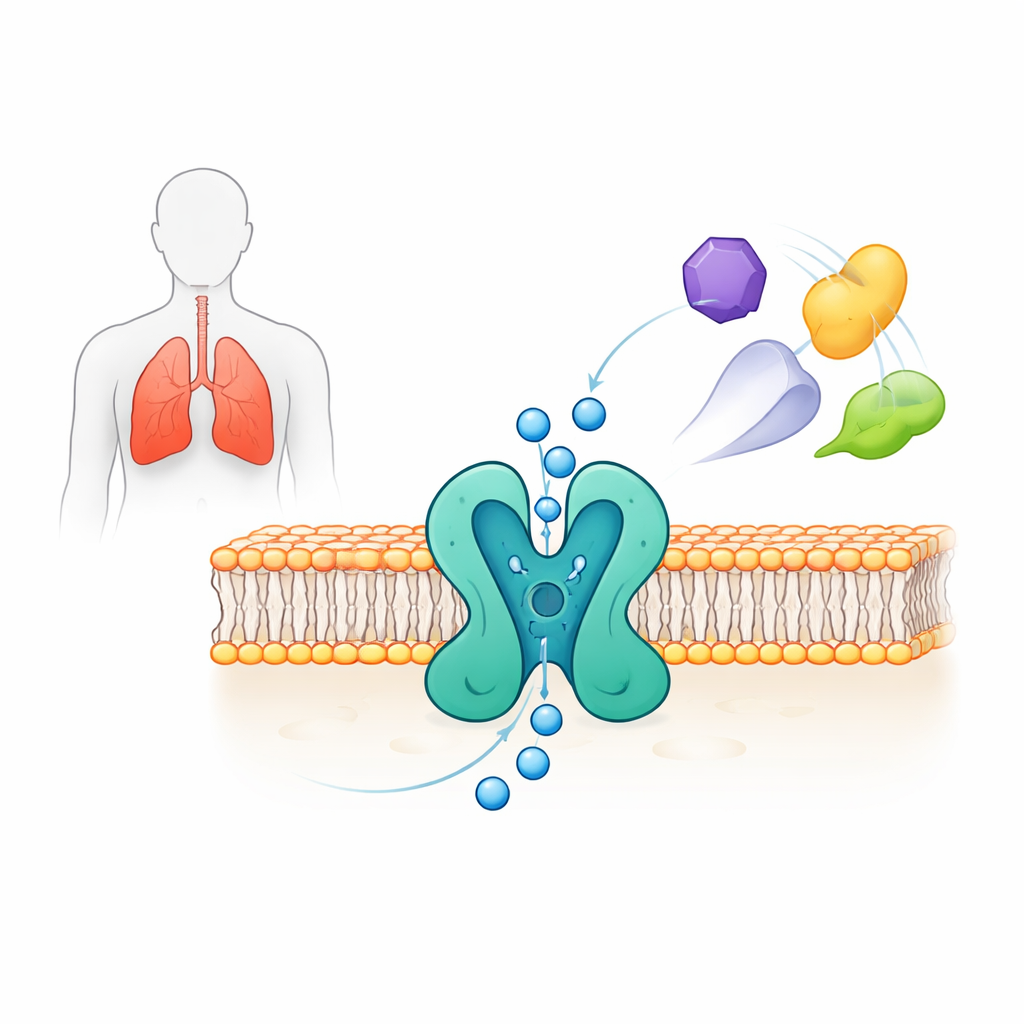
Das Tor auf atomarer Ebene sehen
Die Forschenden exprimierten das vollständige menschliche TWIK-2 in humanen Zelllinien und bestimmten seine dreidimensionale Struktur mittels Einzelpartikel‑Kryo‑Elektronenmikroskopie mit einer Auflösung von etwa 3,7 Angström. Der Kanal bildet eine zweiteilige Anordnung, die zusammen einen zentralen Porus für Kaliumionen erzeugt. Jede Hälfte enthält vier membranüberspannende Segmente und zwei „Poren‑Helices“, die eine enge Region formen, den Selektivitätsfilter, in dem Kalium von anderen Ionen unterschieden wird. Über dem Porus bilden zwei bogenförmige „Kappen“ zwei getrennte Eintrittspfade für Ionen von außen. Die Struktur zeigt außerdem subtile Asymmetrien zwischen den beiden Seiten des Porus, die TWIK-2 eine pseudo‑vierteilige Anordnung verleihen — ein Kennzeichen dieser Kanal‑Familie.
Verborgene Lipide und ein fein abgestimmter Ionenpfad
Entlang des Ionenleitungswegs kartierten die Autor:innen, wie Kaliumionen vom Zellinneren durch eine hydrophobe „Manschette“, den Selektivitätsfilter hinauf und unterhalb der Kappe hindurch nach außen wandern. Die engste Stelle ist immer noch breit genug, dass Kalium in Einzelfile reisen kann. Obwohl das Protein ohne zugesetzte Lipidmoleküle gereinigt wurde, zeigten die Kryo‑EM‑Karten röhrenförmige Dichten in der Nähe des unteren Porusteils und in seitlichen Taschen zwischen den Helices. Diese Stellen repräsentieren wahrscheinlich Lipide oder Detergensschwänze, die bei der Aufreinigung an TWIK-2 haften blieben, und deuten darauf hin, dass natürliche Membranlipide in diesen Rillen Platz nehmen und die Form benachbarter Helices leicht verschieben könnten. Solche Verschiebungen, insbesondere in einer Helix namens M4 und in den Schleifen des Selektivitätsfilters, dürften darüber entscheiden, ob der Kanal offen, geschlossen oder in einem Zwischenzustand ist.
Das Tor mit Mutationen und Blockern erforschen
Um Struktur und Funktion zu verknüpfen, verwendeten die Wissenschaftler:innen ein automatisiertes Patch‑Clamp‑System, um Ströme aus Zellen zu messen, die entweder normales TWIK-2 oder Versionen mit gezielten Aminosäureveränderungen exprimierten. Sie fanden, dass TWIK-2 stark spannungsabhängig ist, aber im Gegensatz zu seinem Verwandten TWIK-1 weitgehend unempfindlich gegenüber Änderungen der äußeren Säurestärke (pH) bleibt. Mutationen an zwei konservierten Threonin‑Resten an der Basis des Selektivitätsfilters ließen den Kanal schneller öffnen und mehr Strom leiten, was darauf hindeutet, dass diese Positionen als Scharniere wirken, die den geschlossenen Zustand stabilisieren. Veränderungen am Ein- und Ausgang des Porus beeinflussten, wie schnell der Kanal an‑ und abschaltete, und zeigten, wie eng der Ionenpfad reguliert ist. Das Team testete dann vier bekannte kleine Moleküle, die verwandte Kanäle modulieren. Zwei davon, ML365 und NPBA, blockierten TWIK-2 stark, während die anderen keine Wirkung zeigten. Durch den Vergleich, wie verschiedene Mutationen die Medikamentenempfindlichkeit veränderten, schließen die Autor:innen, dass diese Verbindungen wahrscheinlich unmittelbar unter dem Selektivitätsfilter und in benachbarten Kavitäten binden und dass unterschiedliche Arzneistoffe über überlappende, aber unterschiedliche Bindungsmodi wirken.
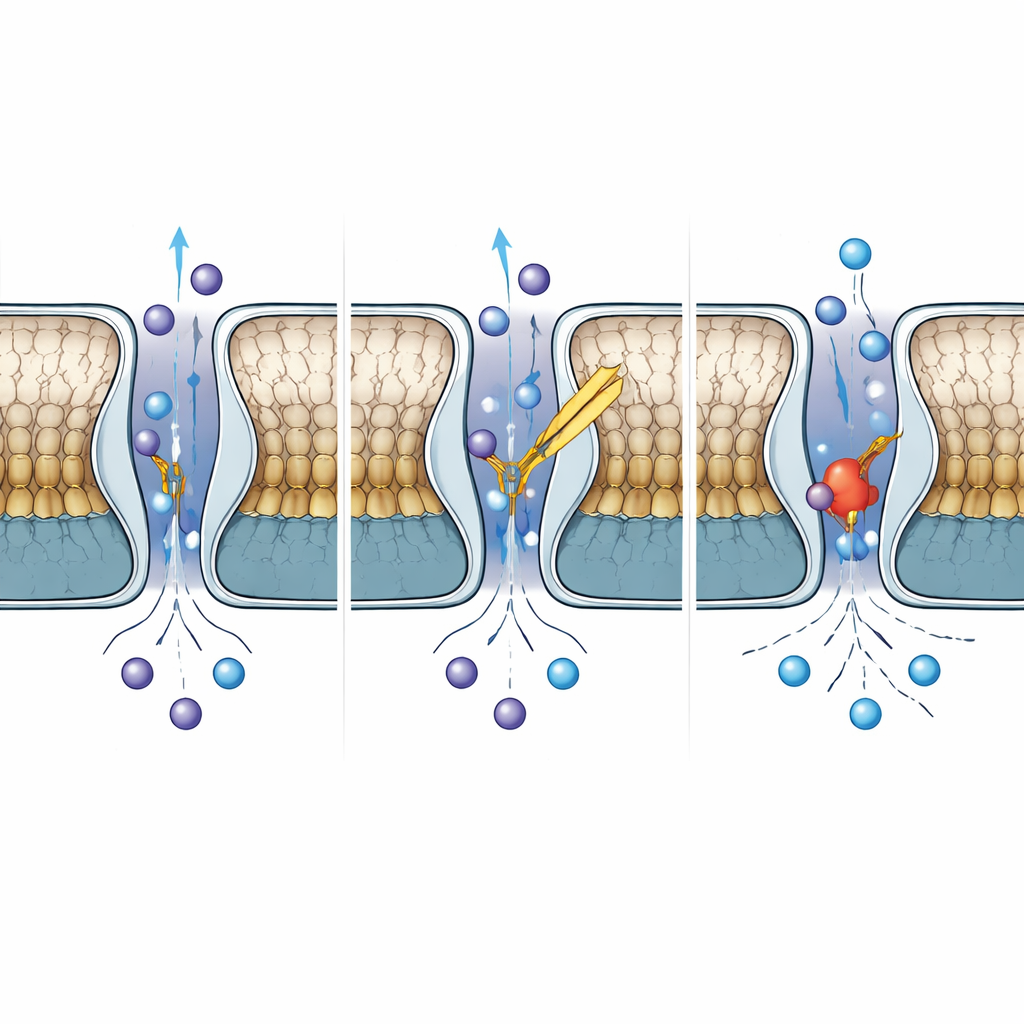
Wodurch sich TWIK-2 von seinen nahen Verwandten unterscheidet
Obwohl TWIK-2 mehr als die Hälfte seiner Sequenz mit TWIK-1 teilt, unterscheiden sich ihre Eigenschaften in wichtigen Punkten. Beim Vergleich von TWIK-2 mit veröffentlichten TWIK-1‑Strukturen bei neutralem und saurem pH stellten die Autor:innen fest, dass die Kappenregion von TWIK-2 der säureinhibierten Form von TWIK-1 ähnelt, während der Selektivitätsfilter weiterhin in einer an den leitenden, offenen Zustand erinnernden Anordnung vorliegt. Ein einzelnes Histidin in TWIK-1, das Protonen wahrnimmt und sich bei niedrigem pH in den Porus schwingt, um den Ionentransport zu blockieren, ist in TWIK-2 durch ein Tyrosin ersetzt. Selbst wenn das Team an dieser Position in TWIK-2 wieder ein Histidin einführte, wurde der Kanal nicht pH‑sensitiv, was zeigt, dass die pH‑Kontrolle in diesen Kanälen auf einem weiter gefassten Netzwerk von Resten und Bewegungen beruht und nicht nur auf einer einzigen „Schalt“-Aminosäure.
Von der Struktur zu zukünftigen Therapien
Insgesamt liefert diese Arbeit das erste hochauflösende Bild des menschlichen TWIK-2 und zeigt, wie spezifische strukturelle Merkmale dessen Ionenfluss, Spannungsantwort und Empfindlichkeit gegenüber kleinen Blockern bestimmen. Die Entdeckung, dass bereits existierende Verbindungen TWIK-2 selektiv hemmen können, kombiniert mit einer robusten automatisierten Screening‑Plattform, eröffnet die Möglichkeit groß angelegter Suchen nach sichereren und wirksameren Wirkstoffen. Da die TWIK-2‑Aktivität in Immunzellen mit entgleister Entzündung, insbesondere in der Lunge, verknüpft ist, könnten solche Medikamente die Grundlage neuer entzündungshemmender Behandlungen bilden, die durch das sanfte „Herunterregeln“ dieses kleinen, aber mächtigen Tors in der Zellmembran wirken.
Zitation: Ma, Q., Hernandez, C.C., Navratna, V. et al. Insights into the structure and modulation of human TWIK-2. Nat Commun 17, 2201 (2026). https://doi.org/10.1038/s41467-026-69072-1
Schlüsselwörter: TWIK-2 Kaliumkanal, zwei-poren-domain K2P-Kanäle, cryo-EM Ionkanalstruktur, Modulatoren von Kaliumkanälen, pulmonale Entzündung