Clear Sky Science · de
Koloniale räumliche Einzelzell-Proteomik und Mausmodelle verknüpfen mitochondriale Dysfunktion mit einem Mangel an dimerischem IgA-sezernierenden Plasmazellen bei Morbus Crohn
Warum Darm-Antikörper bei Morbus Crohn wichtig sind
Morbus Crohn ist vor allem für schmerzhafte Schübe intestinaler Entzündung bekannt, doch lange bevor Symptome aufflammen, können sich subtile Veränderungen in der Art und Weise zeigen, wie das Immunsystem den Darm schützt. Diese Studie stellt eine einfache, aber wichtige Frage: Bilden Menschen mit Morbus Crohn in Remission weiterhin die richtige Art von Antikörpern, um die Darmmikroben in Schach zu halten? Durch die Kombination von Patient:innenproben, hochauflösender Gewebeprofilierung, Stoffwechselanalysen und Mausmodellen decken die Autor:innen eine verborgene Schwäche in der Antikörperschutzschicht des Darms auf, die mit der zellulären Energieproduktion zusammenhängt.
Eine Schutzschicht, die nicht ausreicht
Unser Darm ist auf einen speziellen Antikörper angewiesen, das sekretorische IgA, das in den Schleim an der Darmoberfläche freigesetzt wird. IgA, besonders in seiner „doppelten“ Form als dimeres IgA, überzieht Bakterien und andere Mikroben und hält sie eher an der Oberfläche als tief im Gewebe. In dieser Arbeit untersuchten die Forschenden Kolonbiopsien, Blut und Stuhl von Menschen mit Morbus Crohn in Remission sowie von nicht entzündeten Kontrollen. Im Kolongewebe hatten Crohn-Patient:innen tatsächlich mehr B-Zellen und antikörperproduzierende Zellen sowie höhere Mengen an IgA-bezogenen Genen und Proteinen. Doch bei der Messung von IgA im Stuhl fanden die Forschenden das Gegenteil dessen, was man erwarten könnte: Das sekretorische IgA im Darmlumen war deutlich reduziert. 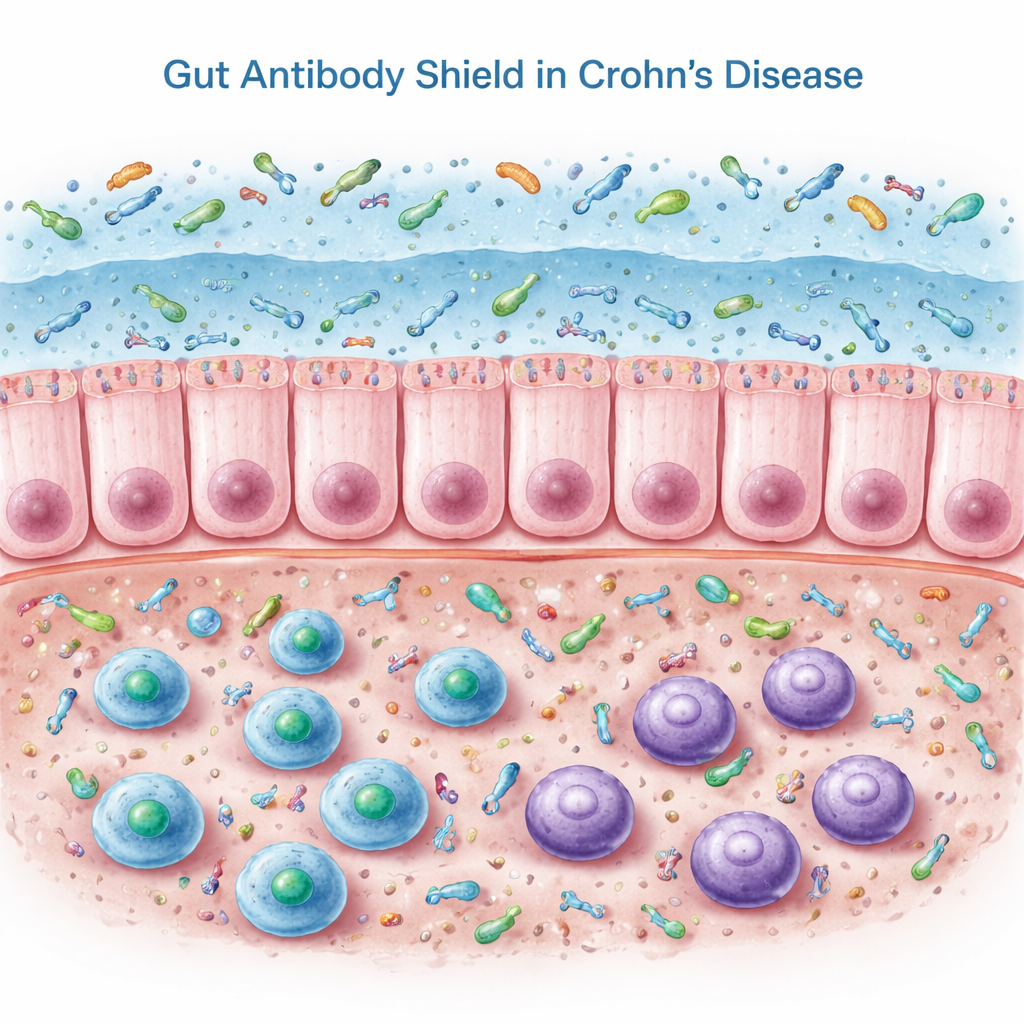
Auf halbem Weg steckengeblieben: antikörperproduzierende Zellen, die nicht vollständig ausreifen
Die Zellen, die IgA sezernieren — Plasmazellen — reifen normalerweise über definierte Stadien von aktiven, kurzlebigen Vorläufern zu langlebigen Spezialisten heran, die große Mengen dimeres IgA produzieren. Mit räumlicher Einzelzell-Proteomik, die viele Proteine auf Einzelzellen innerhalb intakten Gewebes abbildet, konnten die Autor:innen unreife und vollständig ausgereifte Plasmazell-Subsets im Kolon unterscheiden. Bei Crohn-Patient:innen waren frühe Plasmoblasten und unreife Plasmazellen vermehrt, während die am stärksten gereiften Plasmazellen reduziert waren. Biochemische Analysen bestätigten, dass das Verhältnis von dimerem zu monomerem IgA in Crohn-Kolons niedriger war, und jede antikörperproduzierende Zelle sezernierte im Durchschnitt weniger dimeres IgA. Als das Team geschaltete Gedächtnis-B-Zellen aus dem Kolon isolierte und sie in Kultur zur Plasmazell-Differenzierung anregte, konnten Zellen von Crohn-Patient:innen wichtige Reifungsmarker nicht hochregulieren und produzierten weniger Gesamt- und dimeres IgA, obwohl die IgG-Produktion weitgehend normal blieb. Das spricht für eine intrinsische Blockade im Reifungsprogramm, spezifisch für IgA-sezernierende Plasmazellen.
Energiezentralen unter Belastung
Um zu verstehen, was diese Blockade antreibt, wandten sich die Forschenden dem Zellstoffwechsel zu. Sie fanden, dass Plasmazellen im Crohn-Gewebe höhere Mengen an CD38 exprimierten, einem Enzym an der Zelloberfläche, das NAD+ verbraucht — einen zentralen Brennstoff für die mitochondriale Energieproduktion. Gene, die an der mitochondrialen oxidativen Phosphorylierung beteiligt sind — dem Hauptweg, auf dem Zellen ATP aus Nährstoffen erzeugen — waren im Kolongewebe von Crohn-Patient:innen insgesamt herunterreguliert, und Plasma-Metabolitenmuster sprachen für eine Verschiebung weg von effizienter mitochondrialer Atmung. In Ex-vivo-Experimenten verbrauchten aus Crohn-Gewebe stammende Plasmazellen wenig Glukose, setzten weniger Laktat frei und zeigten eine verringerte Expression mitochondrialer Energie-Gene, was auf einen metabolisch „ruhigen“ oder geschwächten Zustand hindeutet. 
Hinweise aus Mausmodellen und der Ernährung
Mausmodelle lieferten zusätzliche Unterstützung. Mäuse mit einer definierten mitochondrialen Mutation, die den ATP-produzierenden Enzymkomplex V beeinträchtigt, hatten weniger ausgereifte Plasmazellen in darmassoziierten lymphatischen Geweben, eine verminderte Expression von Plasmazell-Markern im Kolon und niedrigere Mengen sowohl monomerer als auch dimerer IgA im Kolon. Umgekehrt entwickelten gesunde Mäuse, die eine zuckerfreie, eiweißreiche Diät erhielten — welche die mitochondriale Aktivität im Kolon fördert — mehr IgA-produzierende Zellen und höhere fäkale IgA-Werte. Diese komplementären Experimente verbinden die mitochondriale Leistungsfähigkeit direkt mit der Fähigkeit von Plasmazellen, zu reifen und eine robuste IgA-Barriere im Darm aufrechtzuerhalten.
Was das für Menschen mit Morbus Crohn bedeutet
In der Summe zeichnet die Studie das Bild, dass Morbus Crohn — selbst während klinischer Remission — mit einer Überfülle unreifer B-Linien-Zellen im Kolon und einem Mangel an voll ausgereiften, energieintensiven Plasmazellen verbunden ist, die dimeres IgA in den Schleim sezernieren. Der Darm mag ruhig erscheinen, doch seine Antikörperschutzschicht ist dünner und weniger wirksam. Indem diese Defizienz mit mitochondrialer Dysfunktion verknüpft wird — möglicherweise teils bedingt durch erhöhte CD38-Aktivität — legt die Arbeit nahe, dass Therapien, die auf die Wiederherstellung des zellulären Energiestoffwechsels oder die Feinabstimmung der CD38-Signalgebung abzielen, helfen könnten, die mukosale IgA-Barriere wiederaufzubauen. Für Patient:innen eröffnet das die Perspektive, dass künftige Behandlungen nicht nur Entzündungen bei ihrem Auftreten unterdrücken, sondern auch die vorderste Antikörperabwehr des Darms stärken könnten, um Schübe von vornherein zu verhindern.
Zitation: Raschdorf, A., de Almeida, L.N., Solbach, P. et al. Colonic spatial single-cell proteomics and murine models link mitochondrial dysfunction to dimeric IgA-secreting plasma cell deficiency in Crohn’s disease. Nat Commun 17, 1590 (2026). https://doi.org/10.1038/s41467-026-69069-w
Schlüsselwörter: Morbus Crohn, Darm-Antikörper, IgA, Mitochondrien, intestinales Immunsystem