Clear Sky Science · de
FidlTrack: hochauflösendes, struktur-aware Single-Particle-Tracking löst intrazelluläre Molekülbewegungen in Organellen auf, die APP-Verarbeitung wahrnehmen
Einzelne Moleküle in lebenden Zellen beobachten
Im Inneren jeder Zelle sind unzählige Moleküle ständig in Bewegung, stoßen zusammen, binden sich oder zerfallen. Moderne Mikroskope können einzelne Moleküle nacheinander verfolgen und liefern so die Aussicht auf ein detailliertes Bild der Vorgänge auf kleinster Ebene. Wenn jedoch viele Moleküle schnell in engen, gewundenen Räumen wie dem endoplasmatischen Retikulum oder den Mitochondrien unterwegs sind, werden ihre Bahnen unübersichtlich und leicht fehlinterpretierbar. Diese Studie stellt FidlTrack vor, eine neue Methode, die dieses Durcheinander bereinigt, sodass Forschende dem verfolgen, was sie in Echtzeit an einzelnen Molekülen sehen, mehr vertrauen können.
Warum das Verfolgen winziger Bewegungen so schwierig ist
Single-Particle-Tracking funktioniert, indem derselbe helle Punkt über viele Filmframes hinweg verfolgt wird. Auf relativ flachen Zelloberflächen, wo sich Moleküle langsam bewegen und voneinander getrennt sind, ist das überschaubar. Tief im Zellinneren jedoch diffundieren Moleküle wesentlich schneller und drängen sich in enge, verschlungene Tubuli und Schichten. Zwischen zwei Frames kann sich derselbe Punkt weit bewegt haben, und mehrere identische Punkte können in Reichweite liegen. Traditionelle Software muss „raten“, welcher Punkt im nächsten Frame demselben Molekül entspricht, und diese Zuordnungen können leicht falsch sein. Schlimmer noch: richtige und falsche Pfade können sehr ähnlich aussehen, sodass schwer zu beurteilen ist, welchen Teil der Daten man vertrauen kann.
Experimente so gestalten, dass die Daten ehrlich sind
Die Forschenden bauten zunächst einen realistischen Simulator, der „Ground-Truth“-Filme diffundierender Moleküle erzeugt, bei denen die wahren Pfade bekannt sind. Sie nutzten diese synthetischen Datensätze, um systematisch zu testen, wie zentrale Faktoren die Verfolgbarkeit beeinflussen: wie schnell sich Moleküle bewegen, wie viele in jedem Bild erscheinen, wie oft Bilder aufgenommen werden und wie weit ein Molekül zwischen Frames springen darf. Daraus erstellten sie Karten, die für jede Situation zeigen, welche Einstellungen den Anteil korrekt rekonstruierter Bewegungen maximieren. Diese Karten zeigen: Bei langsam bewegenden Molekülen in moderater Dichte kann Tracking sehr zuverlässig sein, bei schnell bewegenden Molekülen in hoher Dichte steigen die Fehler dagegen rasch an, und mehr Moleküle erhöhen nicht mehr die nützliche Information.
Fragwürdige Schritte erkennen und ausschneiden
Nächstes widmete sich das Team einer subtilen, aber wirkungsvollen Idee: Mehrdeutigkeit. Eine Bewegung ist dann mehrdeutig, wenn mehr als ein möglicher nächster Punkt in Reichweite liegt, sodass der Algorithmus zwischen mehreren plausiblen Verknüpfungen wählen muss. Mithilfe ihrer Simulationen zeigten die Autorinnen und Autoren, dass ein großer Anteil der Tracking-Fehler aus solchen mehrdeutigen Schritten entsteht. Sie definierten einen Ambiguity Score, der zählt, wie oft solche Situationen auftreten, und untersuchten dann, was passiert, wenn nach dem Tracking alle mehrdeutigen Schritte entfernt werden. Dieses Beschneiden opfert einige Daten und verkürzt Pfade, erhöht aber deutlich die Zuverlässigkeit des verbleibenden Materials und verbessert Schätzungen zur Geschwindigkeit der Molekülbewegung. Auf realen Filmen eines Markers im endoplasmatischen Retikulum war die Mehrdeutigkeit in dicht gedrängten Regionen nahe dem Zellkern höher; das Entfernen mehrdeutiger Verknüpfungen säuberte diese Bereiche, ohne einfachere Regionen zu schädigen.
Die Zellarchitektur das Tracking leiten lassen
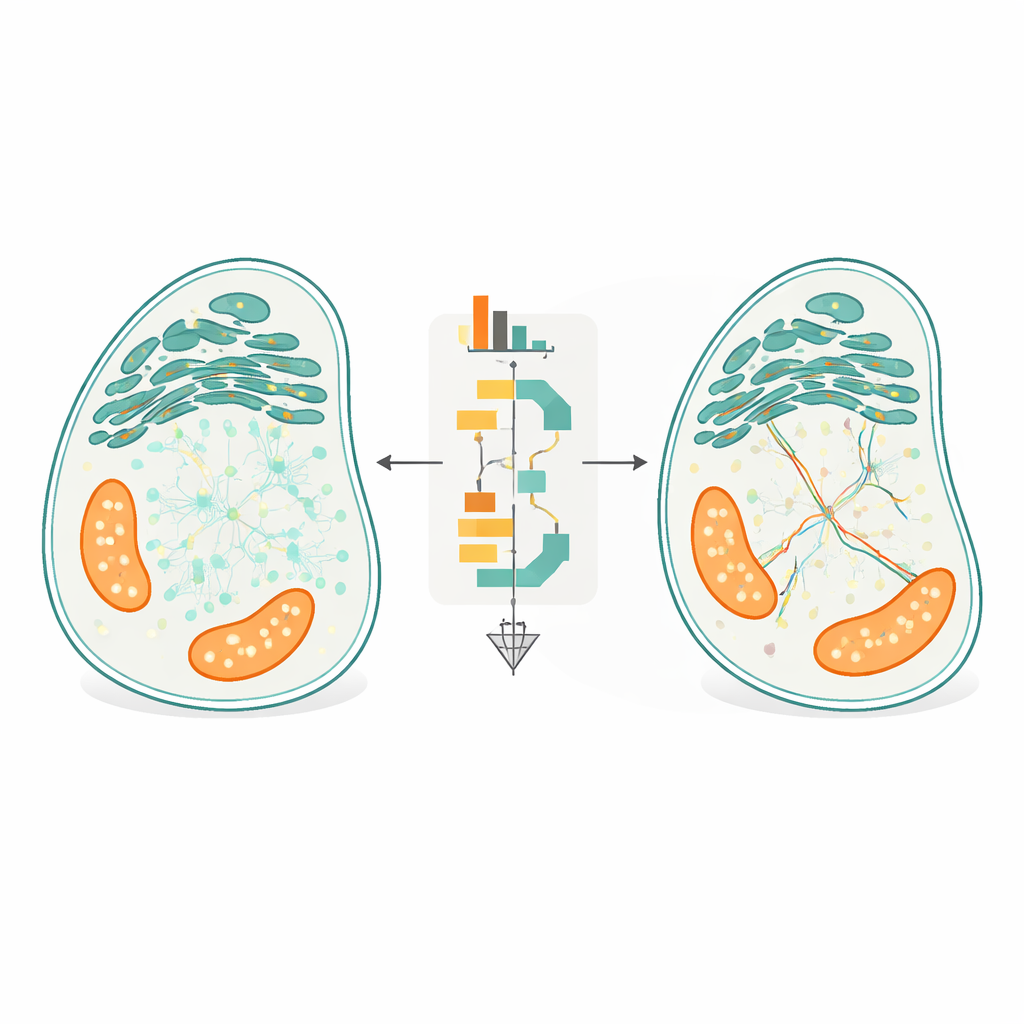
Die zentrale Innovation von FidlTrack ist das „struktur-aware“ Tracking. Anstatt jeden Punkt so zu behandeln, als bewege er sich im leeren Raum, nutzt die Methode Bilder der inneren Zellarchitektur – etwa Konturen des endoplasmatischen Retikulums, der Mitochondrien oder schlanker neuronaler Ausläufer – um einzuschränken, wo sich Moleküle realistisch bewegen können. Das Organellenbild wird in einen Graphen verbundener Pixel umgewandelt, und Distanzen werden entlang dieses Graphen statt als Gerade durch den Raum gemessen. Verbindungen, die erfordern würden, dass ein Molekül über eine Lücke zwischen zwei getrennten Tubuli springt, können so als unmöglich markiert und verworfen werden. In Simulationen eng gepackter Tubuli und in realen Filmen neuronaler Prozesse und Organellen verringerte dieses Strukturwissen mehrdeutige Verknüpfungen um bis zu die Hälfte und erhöhte die Menge vertrauenswürdiger, nicht-mehrdeutiger Bewegungsdaten um ein Mehrfaches.
Verborgenes Zellverhalten und krankheitsrelevante Ereignisse aufdecken
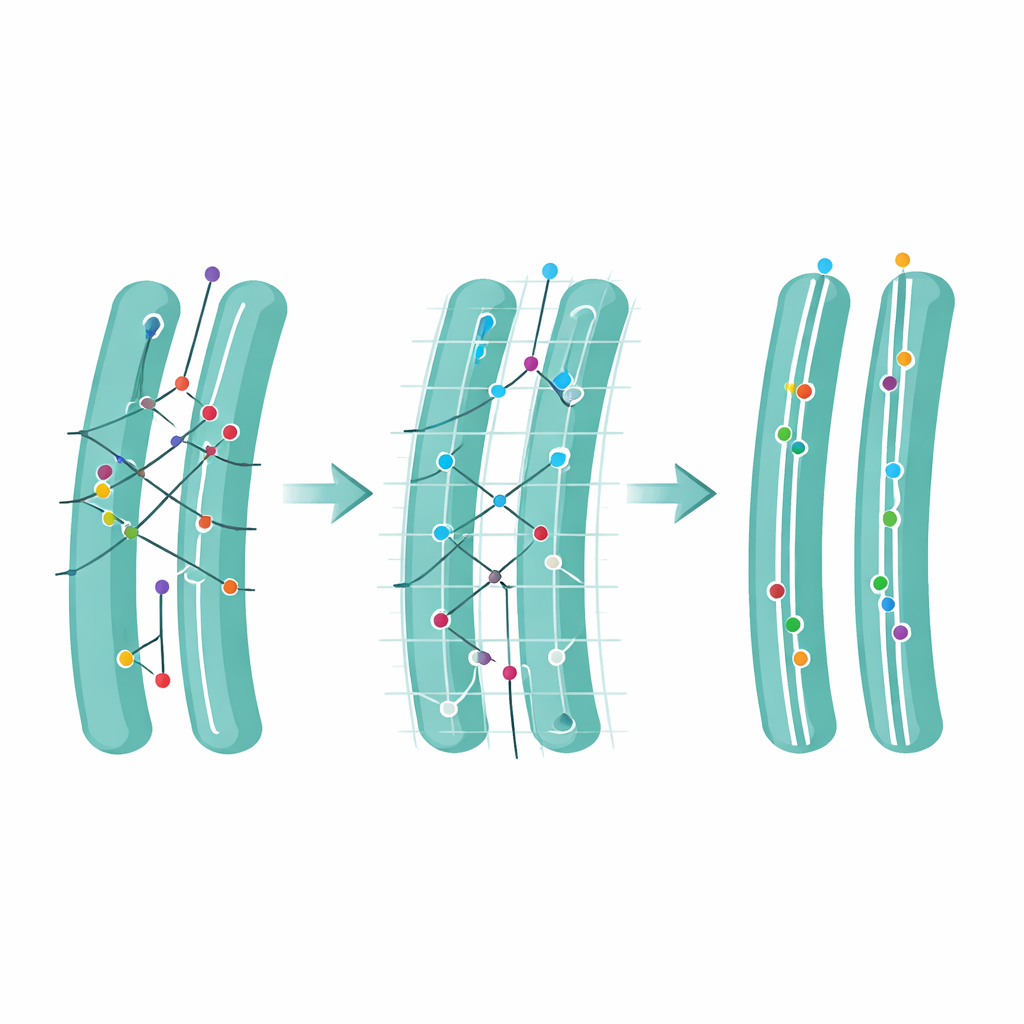
Mit diesen Werkzeugen – optimierten Einstellungen, Ambiguitätsfilterung und Strukturbewusstsein – gingen die Autorinnen und Autoren mehrere biologische Fragestellungen an, die zuvor außerhalb der Reichweite lagen. Im endoplasmatischen Retikulum konnten sie sauber verfolgen, wie Proteine mit Exit-Stellen interagieren, die Fracht zum Golgi-Apparat leiten, und dabei kurze „Vorbeiflüge“ von längeren Verweilzeiten unterscheiden. Sie fingen seltene Momente ein, in denen das Alzheimer-assoziierte Protein APP vom Enzym BACE1 geschnitten wird, sichtbar als plötzlicher Wechsel von langsamer, membrangebundener Bewegung zu schnellerer freier Diffusion. Sie verfolgten zudem gentechnisch veränderte Antikörper-ähnliche Moleküle im ER und schlossen aus Änderungen ihrer Bewegung, wann sie an ihr Ziel gebunden waren und wann sie frei drifteten. In all diesen Fällen lieferte FidlTrack zuverlässigere Trajektorien und schärfte Unterschiede, die beim Standard-Tracking verwischt oder unterschätzt wurden.
Was das für die zukünftige Zellbiologie bedeutet
Für Nicht-Spezialisten ist die Kernbotschaft: Nicht alle Einzelmolekülspuren sind gleichwertig – einige sind vertrauenswürdig, andere irreführend, und bisher war schwer zu unterscheiden, welche welche sind. FidlTrack bietet einen praktischen, Open-Source-Weg, um sowohl die Zuverlässigkeit eines Datensatzes zu messen als auch diese Zuverlässigkeit zu verbessern: durch Anpassung experimenteller Einstellungen, Entfernen mehrdeutiger Schritte und Nutzung der eigenen Zellgeometrie als Leitfaden. So wird es möglich, Moleküle mit größerer Zuversicht durch das komplexe Zellinnere zu verfolgen und seltene oder subtile Ereignisse – von Protein-Sortierung bis hin zu krankheitsrelevanter Verarbeitung –, die zuvor im Rauschen verborgen waren, aufzudecken.
Zitation: Parutto, P., Yuan, Y., Davì, V. et al. FidlTrack: high-fidelity structure-aware single particle tracking resolves intracellular molecular motion in organelles sensing APP processing. Nat Commun 17, 2639 (2026). https://doi.org/10.1038/s41467-026-69067-y
Schlüsselwörter: Single-Particle-Tracking, intrazelluläre Dynamik, Organelle-Struktur, Proteinbewegung, Alzheimer-Krankheit