Clear Sky Science · de
Tenascin C+ Myofibroblasten verschlimmern die neointimale Hyperplasie durch Vermittlung von Nerven-Makrophagen-Interaktionen bei Mäusen
Wenn Blutgefäße falsch heilen
Verfahren, die verstopfte Arterien wieder eröffnen, wie Angioplastie und Bypass-Operationen, retten unzählige Leben. Dennoch hinterlassen sie oft ein verborgenes Problem: Mit der Zeit kann das behandelte Gefäß nach innen vernarben, sich wieder verengen und die Patientinnen und Patienten erneut gefährden. Diese Studie an Mäusen deckt ein unerwartetes Dreiergespräch zwischen Stützzellen, Nerven und Immunzellen in der Gefäßwand auf, das dieses schädliche Überheilen vorantreibt, und identifiziert ein Molekül namens Tenascin C als vielversprechenden Angriffspunkt, um den Kreislauf zu durchbrechen.
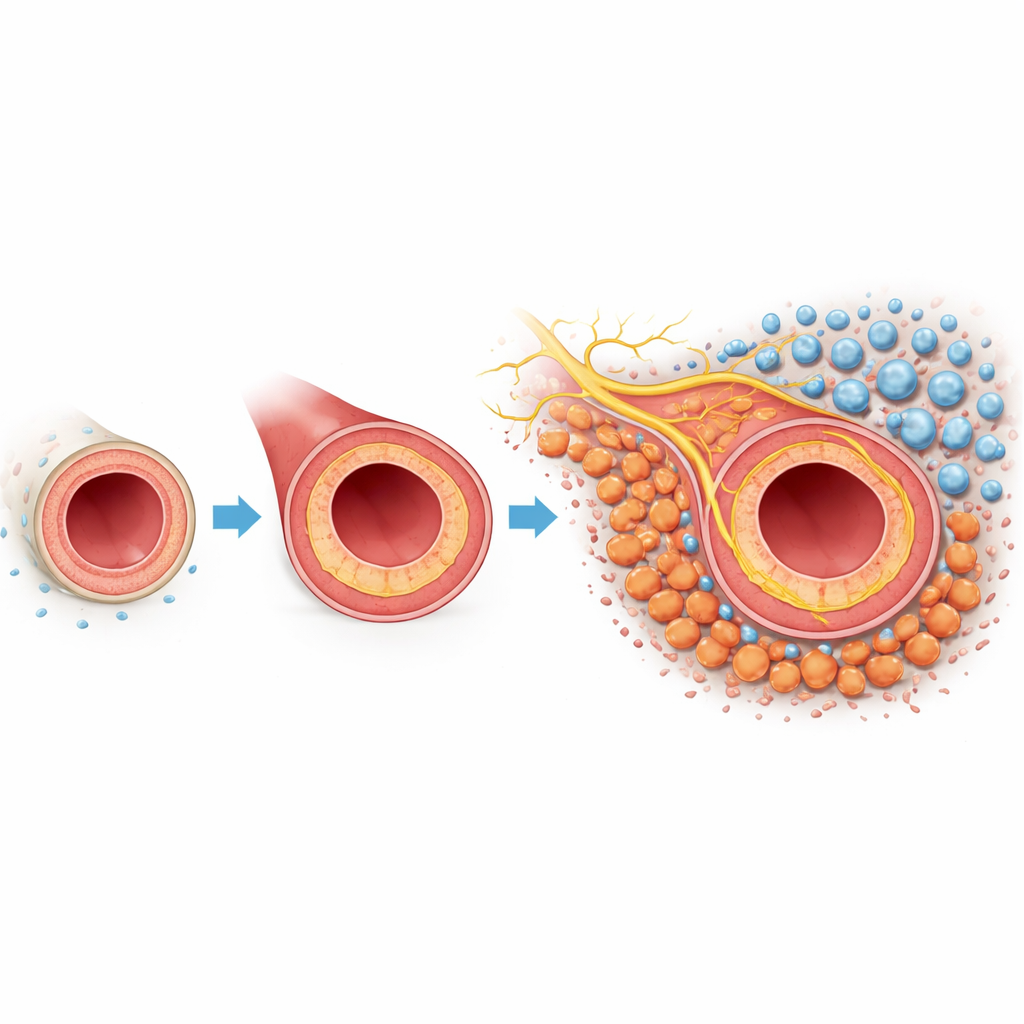
Ein genauerer Blick auf problematische Narbenbildung in Arterien
Wenn eine Arterie verletzt oder während einer Operation manipuliert wird, kann die innere Auskleidung zu aggressiv nachwachsen. Dieses nach innen gerichtete Wachstum, Neointimale Hyperplasie genannt, verdickt die Gefäßwand und verengt den Blutflusskanal. Die äußerste Schicht des Gefäßes, die Adventitia, enthält Fibroblasten – Stützzellen, die normalerweise die Gefäßstruktur erhalten. In diesem Mausmodell, bei dem die Halsschlagader teilweise abgebunden wurde, um eine Verletzung zu simulieren, nutzten die Forschenden Einzelzell-Genprofilierung und räumliche Kartierung, um alle wichtigen Zelltypen zu erfassen. Sie fanden heraus, dass Fibroblasten besonders zahlreich waren und ihr Verhalten nach der Verletzung dramatisch veränderten, was darauf hindeutet, dass diese Zellen zentrale Akteure der Narbenreaktion sein könnten.
Der Aufstieg narbenbildender Tenascin‑C-Zellen
Bei genauerer Untersuchung der Fibroblastenpopulation entdeckte das Team eine eindeutige Untergruppe, die erst nach der Verletzung auftrat. Diese Zellen trugen Merkmale von Myofibroblasten – hohe Mengen des kontraktilen Proteins α-glatte Muskel-Aktin und einen weiteren Marker namens Periostin – was darauf hinweist, dass sie in einen narbenbildenden Modus übergingen. Entscheidend war, dass diese Untergruppe auch große Mengen Tenascin C produzierte, ein Matrixprotein, das in gesunden erwachsenen Geweben normalerweise selten ist, bei Krankheit und Gewebereparatur jedoch reichlich vorkommt. Laborversuche zeigten, dass die Exposition normaler adventitieller Fibroblasten gegenüber Transforming Growth Factor Beta oder zusätzlichem Tenascin C sie dazu brachte, zu diesen Tenascin‑C-positiven Myofibroblasten zu werden. Die Zellen schütteten dann noch mehr Tenascin C aus und erzeugten so eine sich selbst verstärkende Schleife über ein spezifisches Oberflächenrezeptorpaar, Integrin αvβ1, die die narbenbildende Population kontinuierlich vergrößerte.
Nerven und Immunzellen ziehen in die Nachbarschaft
Die Geschichte endete nicht mit der Narbenbildung. Mit 3D-Ganzpräparat-Imaging und räumlicher Transkriptomik beobachteten die Forschenden, dass die Tenascin‑C‑reichen Myofibroblasten nahe sprossenden Nervenfasern und sogenannten Makrophagen in der äußeren Gefäßwand gruppiert waren. Verletzte Arterien zeigten dichte, verfilzte Sensornerven und mehr synapsenähnliche Strukturen als normal, sowohl bei Mäusen als auch in menschlichen Arterienproben mit neointimaler Hyperplasie. Makrophagen in diesen Regionen wiesen ein entzündliches Profil auf und produzierten Moleküle wie IL‑1β und TGF‑β1, die die Narbenbildung weiter anheizen können. Zusammen zeichneten die Daten ein Bild einer umorganisierten Mikroumgebung, in der narbenbildende Zellen, Nerven und Makrophagen physisch miteinander verflochten sind und sich gegenseitig beeinflussen.
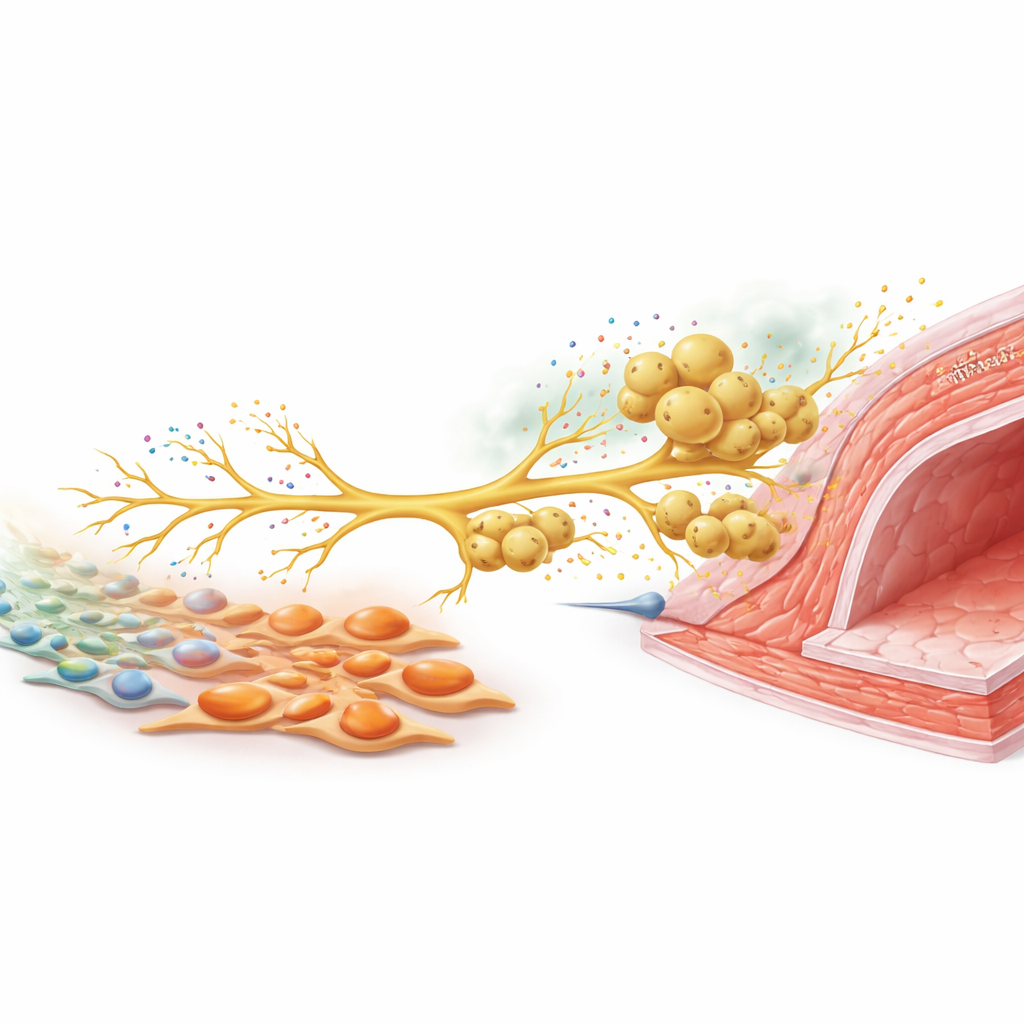
Ein Nervensignal, das weitere Verteidiger herbeiruft
Um zu verstehen, wie diese Zelltypen kommunizieren, konzentrierte sich das Team auf Sensornerven, die schädliche Reize wahrnehmen. In Zellkultur förderten Tenascin‑C‑reiche Myofibroblasten das Auswachsen von Nervenfasern aus Dorsalwurzelganglienneuronen. Bei verletzten Mäusen steigerten diese sensorischen Neuronen die Produktion von CCL2, einem chemischen Signal, das gut dafür bekannt ist, Makrophagen anzuziehen. Wenn Neuronen und Makrophagen gemeinsam kultiviert wurden, wanderten Makrophagen entlang wachsender Nervenfasern, ähnlich wie sie in vivo um Arterien beobachtet wurden. Das Stummschalten von CCL2 in Neuronen reduzierte die Makrophagenrekrutierung stark. Im Tiermodell führten eine Dämpfung der sensorischen Nervenaktivität mittels eines Giftes oder das selektive Löschen von Tenascin C nur in Fibroblasten jeweils zu geringerer Nervendichte, niedrigeren CCL2‑Werten, verringerter Makrophagenansammlung und letztlich zu einer geringeren Verdickung der Gefäßwand. Die Kombination beider Interventionen brachte keinen zusätzlichen Nutzen, was darauf hindeutet, dass sie entlang desselben Pfades wirken.
Warum dieser neue Weg wichtig ist
Insgesamt zeigen die Ergebnisse einen Teufelskreis: Eine Verletzung veranlasst Fibroblasten dazu, zu Tenascin‑C-produzierenden Myofibroblasten zu werden; diese Zellen verändern die Matrix und stimulieren Sensornerven; aktivierte Nerven setzen CCL2 frei, das Makrophagen anzieht; und Makrophagen sezernieren entzündliche und fibrotische Faktoren, die die Narbenbildung verschlimmern und die Arterie verengen. Indem Tenascin C und seine nachgeschaltete Nerven–Makrophagen‑Achse als zentrale Treiber dieses Kreislaufs identifiziert werden, legt die Arbeit nahe, dass Therapien, die dieses Molekül oder seine Signalpartner angreifen, dazu beitragen könnten, reparierte Arterien länger offen zu halten und Patientinnen und Patienten nach kardiovaskulären Eingriffen dauerhafteren Schutz zu bieten.
Zitation: Tong, X., Shi, G., Fang, Z. et al. Tenascin C+ myofibroblasts exacerbate vascular neointimal hyperplasia by propagation of nerve-macrophage interactions in mice. Nat Commun 17, 2199 (2026). https://doi.org/10.1038/s41467-026-69062-3
Schlüsselwörter: neointimale Hyperplasie, Tenascin C, vaskuläres Remodeling, Sensornerven, Makrophagenentzündung