Clear Sky Science · de
Paclitaxel fördert die Ausbreitung TREM2+ Makrophagen und erklärt damit seine geringere Wirksamkeit im Vergleich zu Nab‑paclitaxel
Warum diese Studie wichtig ist
Viele Frauen mit Brustkrebs erhalten Chemotherapeutika aus der Gruppe der Taxane, am häufigsten Paclitaxel oder eine neuere Variante, die an winzige Albuminpartikel gekoppelt ist und als Nab‑paclitaxel bekannt ist. Ärztinnen und Ärzte vermuteten schon länger, dass das neuere Präparat oft bessere Ergebnisse liefert, doch die Gründe dafür waren unklar. Diese Studie wertet sowohl Patientendaten als auch Tierexperimente aus und zeigt, dass herkömmliches Paclitaxel unbeabsichtigt die Metastasierung in die Lunge fördern kann, indem es die Immunzellen des Körpers umformt, und sie weist auf einen Weg hin, diesen schädlichen Nebeneffekt zu blockieren.
Zwei ähnliche Medikamente, zwei unterschiedliche Ergebnisse
Die Forschenden verglichen zunächst die reale Wirksamkeit von Paclitaxel und Nab‑paclitaxel bei mehreren tausend Frauen mit Brustkrebs. Durch die Zusammenführung von Ergebnissen aus 17 klinischen Studien mit 6.486 Patientinnen fanden sie, dass Nab‑paclitaxel höhere Tumorverkleinerungsraten und öfter ein vollständiges Verschwinden des Krebses in Brust und benachbarten Lymphknoten vor einer Operation erzielte. Dieser Vorteil zeigte sich besonders deutlich bei Patientinnen, die nach früheren Therapieversagen behandelt wurden. Da beide Medikamente in ähnlichen Dosen verabreicht werden und auf ähnlichem Wege auf teilende Krebszellen zielen, deutet das Ergebnis darauf hin, dass Unterschiede jenseits der direkten Tumorzellabtötung eine Rolle spielen müssen.
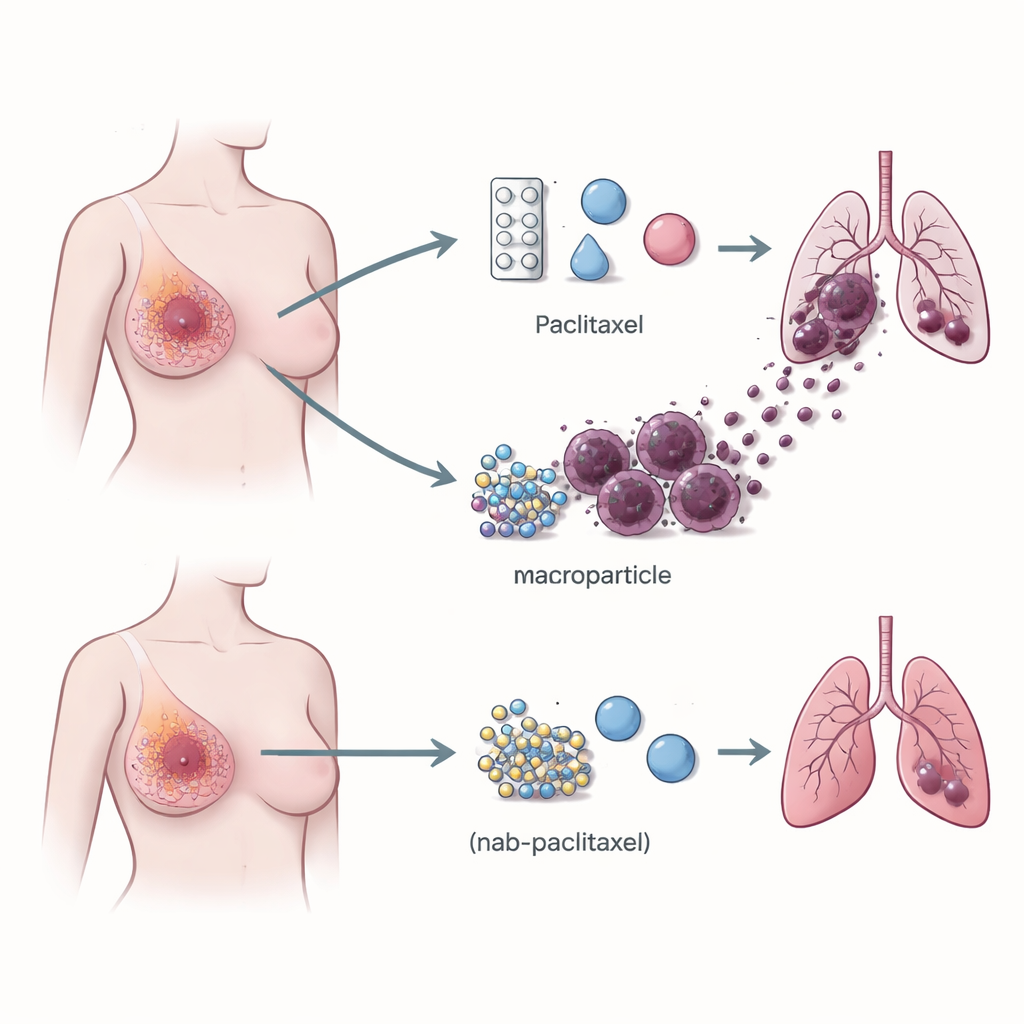
Immunzellen, die der Krebsverbreitung helfen
Der Blick richtete sich auf die Immunumgebung des Tumors – das Gemisch aus weißen Blutkörperchen, die den Krebs bekämpfen oder, überraschend oft, sein Wachstum unterstützen können. Mittels Einzelzell‑RNA‑Sequenzierung, die die Genaktivität tausender einzelner Zellen erfasst, verglich das Team Tumoren von Patientinnen, die mit Paclitaxel gegenüber Nab‑paclitaxel behandelt wurden. Sie fanden, dass in Paclitaxel‑behandelten Tumoren deutlich mehr Makrophagen vorkamen, die einen Rezeptor namens TREM2 auf ihrer Oberfläche tragen. Diese TREM2‑positiven Makrophagen sammelten sich vermehrt an den Tumorrändern und waren bei Patientinnen, die später Lungenmetastasen entwickelten, deutlich zahlreicher als bei solchen, deren Krebs lokal blieb. Dieses Muster bestätigte sich in größeren Patientengruppen und in Mausmodellen und stellte eine starke Verbindung zwischen diesem Makrophagentyp und dem Risiko der Krebsverbreitung her.
Wenn die Behandlung Tumoren verkleinert, aber die Ausbreitung fördert
Bei Mäusen mit Brusttumoren tat Paclitaxel das Erwartete: Es verlangsamte oder verkleinerte die Primärtumoren. Gleichzeitig erhöhte es jedoch die Anzahl von Krebsabsiedlungen in der Lunge und verstärkte das Vorkommen TREM2‑positiver Makrophagen im Tumor und im Blutkreislauf. Nab‑paclitaxel dagegen verringerte die Tumorgröße, ohne Lungenmetastasen zu fördern oder diese Makrophagen zu vergrößern, obwohl es die Primärtumoren ebenso effektiv verkleinerte. Wurde das TREM2‑Gen bei Mäusen entfernt oder TREM2 mittels antisense Oligonukleotiden (kurze DNA‑Stücke, die spezifische Gene stilllegen) reduziert, behielt Paclitaxel seine Fähigkeit zur Tumorverkleinerung, verlor aber weitgehend seine Fähigkeit, die Lungenmetastasierung zu fördern. Das zeigt, dass TREM2‑tragende Makrophagen nicht nur Beobachter sind; sie sind notwendige Partner bei der durch Paclitaxel ausgelösten Metastasierung.
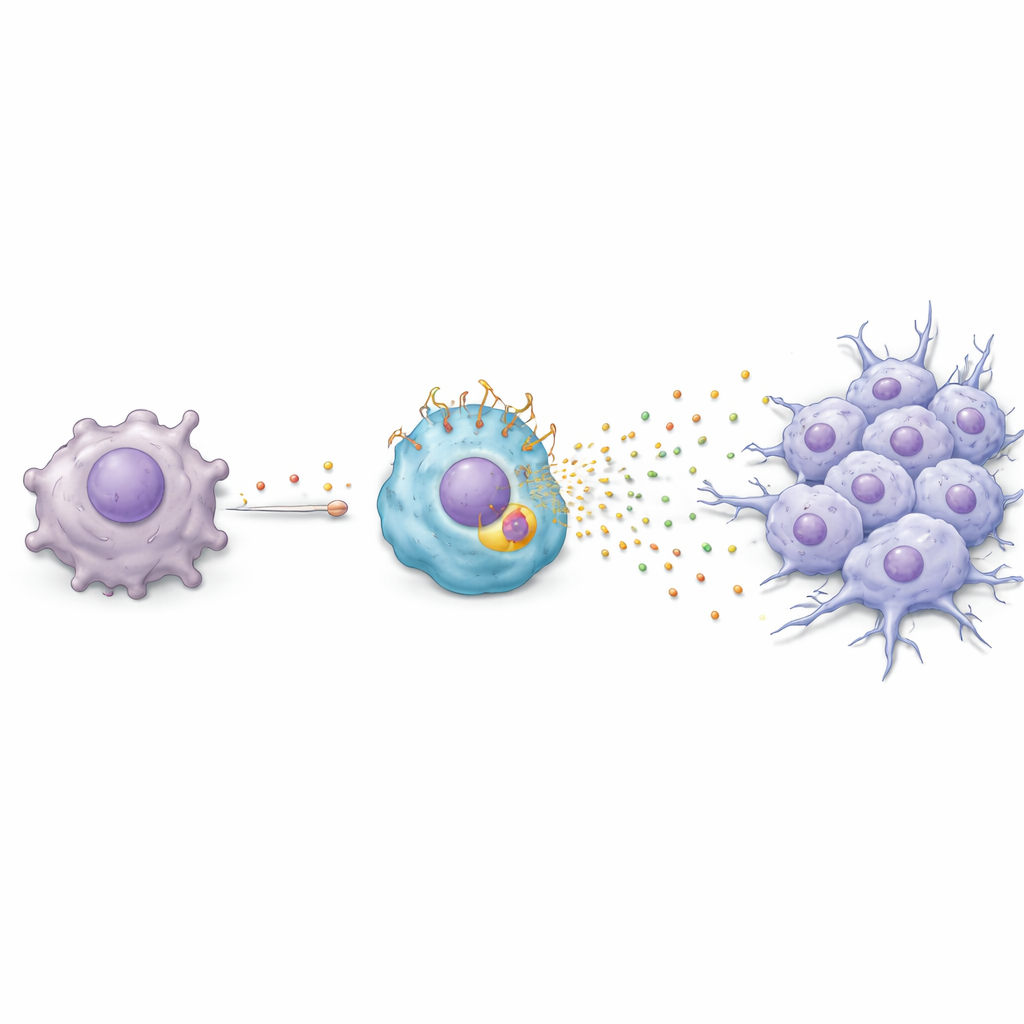
Eine chemische Kaskade vom Tumor zur Immunzelle
Die Forschenden untersuchten anschließend, wie Paclitaxel Makrophagen in diesen schädlichen TREM2‑reichen Zustand versetzt. Sie entdeckten eine Kaskade: Paclitaxel veranlasst Krebszellen, ein Stressantwort‑Gen namens ATF3 hochzufahren, was wiederum die Produktion eines Wachstumsfaktors namens FGF2 steigert. Die Krebszellen geben FGF2 in ihre Umgebung ab, wo es auf benachbarte Makrophagen wirkt. Dort aktiviert FGF2 einen weiteren Regulator, EGR1, der die TREM2‑Expression erhöht. Sobald TREM2 hoch ist, beginnen Makrophagen, ein Gemisch aus Proteinen – darunter Serpin E1, HGF, CCL3 und CXCL2 – freizusetzen, das Krebszellen in eine beweglichere, invasivere Form treibt, die als epithelial‑mesenchymale Transition bekannt ist. In Zellkulturen und in Mäusen machte dieser chemische Austausch Tumorzellen wanderfreudiger und invasiver, typische Schritte auf dem Weg zur Metastasierung.
Aus dem zweischneidigen Schwert ein sichereres Werkzeug machen
Aus allgemein verständlicher Sicht ist die Kernbotschaft: Paclitaxel kann wie ein zweischneidiges Schwert wirken — während es Tumoren angreift, instruiert es gleichzeitig bestimmte Immunzellen, dem Krebs zu helfen, in entfernte Organe zu entkommen. Nab‑paclitaxel scheint diesen speziellen Immunfehlalarm zu vermeiden. Ermutigend ist, dass das Blockieren von TREM2 — oder Teilen der FGF2–EGR1–TREM2‑Signalachse — in Tiermodellen die tumorverkleinernden Vorteile von Paclitaxel von seinen metastasenfördernden Risiken trennen kann. Wenn ähnliche Strategien beim Menschen sicher und wirksam sind, könnten Ärztinnen und Ärzte ein bekanntes, breit verfügbares Chemotherapeutikum weiter einsetzen und gleichzeitig dessen Neigung zur Förderung der Krebsverbreitung eindämmen, was langfristig zu besseren Ergebnissen für Patientinnen und Patienten führen könnte.
Zitation: Xing, Y., Zhong, R., Li, Q. et al. Paclitaxel drives TREM2+ macrophage expansion underlying its inferior therapeutic efficacy compared to Nab-paclitaxel. Nat Commun 17, 2272 (2026). https://doi.org/10.1038/s41467-026-69060-5
Schlüsselwörter: Brustkrebs, Paclitaxel, Tumormikroumgebung, Makrophagen, Metastasen