Clear Sky Science · de
Zuverlässige Umnutzung des Antikörper‑Interaktoms innerhalb der Zelle
Antikörper in winzige Werkzeuge innerhalb unserer Zellen verwandeln
Antikörper sind als präzise Waffen im Blutkreislauf bekannt, die Viren und andere Bedrohungen gezielt erkennen. In vielen Krankheiten — darunter Alzheimer, Parkinson und einige Krebsarten — findet das Geschehen jedoch größtenteils innerhalb der Zellen statt, wo konventionelle Antikörper selten hinkommen oder nicht gut funktionieren. Diese Studie zeigt, wie sich bestehende Antikörper systematisch in kleinere „Intrakörper“ umbauen lassen, die zuverlässig in lebenden menschlichen Zellen funktionieren. Das eröffnet neue Möglichkeiten für Diagnostik, Forschungsmittel und potenziell künftige Therapien, die direkt im Zentrum krankheitsrelevanter Prozesse wirken.
Warum herkömmliche Antikörper in Zellen Probleme haben
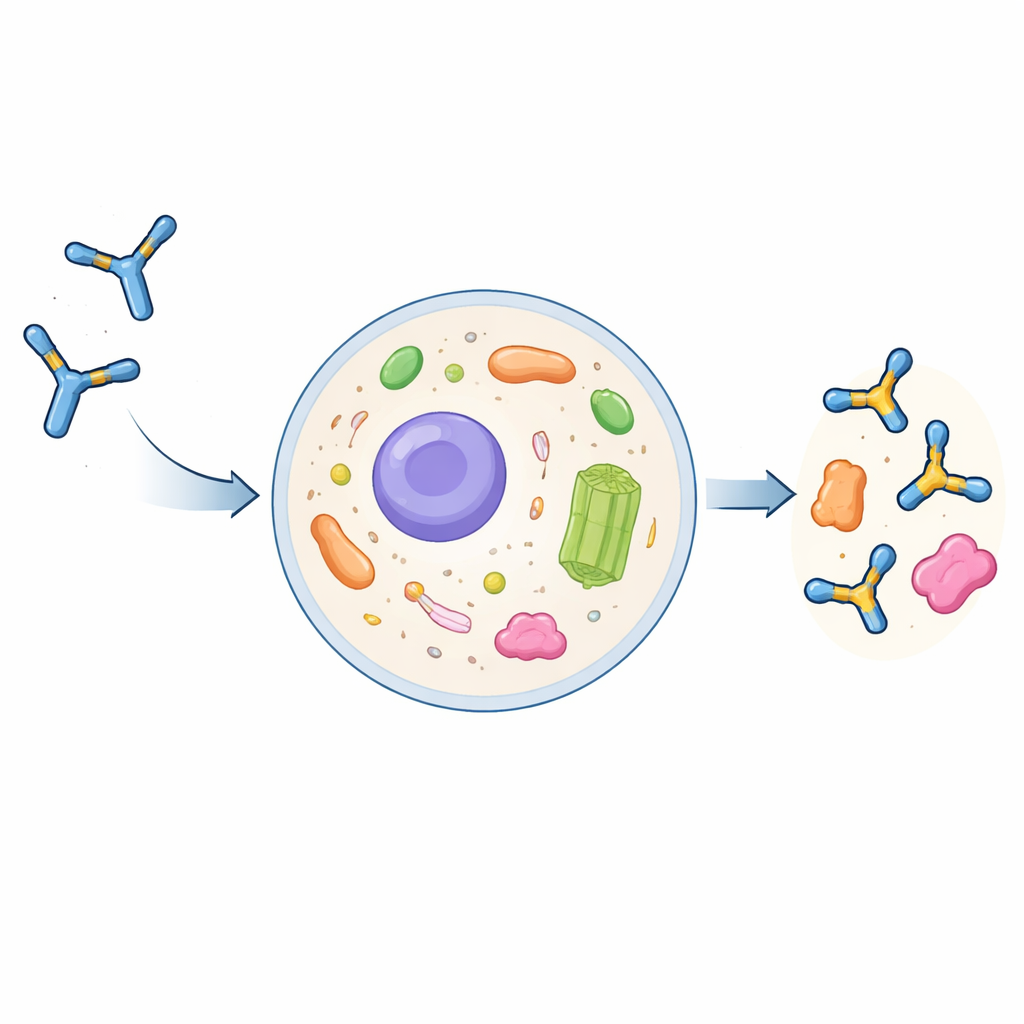
Vollständige Antikörper sind große, Y‑förmige Proteine, die sich evolutionär auf den Einsatz außerhalb von Zellen spezialisiert haben. Sie werden im sekretorischen Weg einer Zelle assembliert und chemisch modifiziert und dann in den Blutkreislauf freigesetzt. Wenn Zellen sie wieder aufnehmen, landen sie meist in Abbaukompartimenten statt im flüssigen Inneren der Zelle, dem Zytoplasma. Wissenschaftler können Antikörper auf die erkennungsrelevanten Teile kürzen — die sogenannten single‑chain variable fragments (scFvs) — und diese als Intrakörper innerhalb der Zelle exprimieren. Diese Intrakörper neigen jedoch dazu, zu verklumpen, unlöslich zu werden und ihre Bindungsfähigkeit zu verlieren. Bislang gab es keine allgemeine, verlässliche Anleitung, um einen konventionellen Antikörper in einen gut funktionierenden Intrakörper zu verwandeln.
Die Gestaltungsregeln für lösliche Intrakörper finden
Die Forscher begannen damit, zu messen, wie gut sich 45 verschiedene Intrakörper in menschlichen Zellen gelöst hielten. Sie verglichen systematisch zahlreiche Proteineigenschaften — etwa Gesamt‑Hydrophobizität, vorhergesagte Strukturqualität und die Eigenschaften der Bindungsschleifen — um herauszufinden, welche Merkmale am besten erklären, ob ein Intrakörper löslich bleibt. Ein einfacher Faktor stach hervor: die Gesamtladung bei annähernd physiologischem pH. Intrakörper mit einer stark negativen Nettoladung blieben deutlich eher löslich, während solche mit neutraler oder positiver Ladung zur Aggregation neigten. Andere aufwendigere Prädiktoren, einschließlich Strukturvertrauenswerte aus dem AlphaFold‑System, korrelierten nicht mit der Löslichkeit. Daraus bauten die Autoren ein praktisches, ladebasiertes Modell, das abschätzen kann, welcher Anteil eines Intrakörpers in der löslichen Fraktion eines Zellextrakts zu finden ist.
Linker und Domänen für besseres Verhalten neu designen
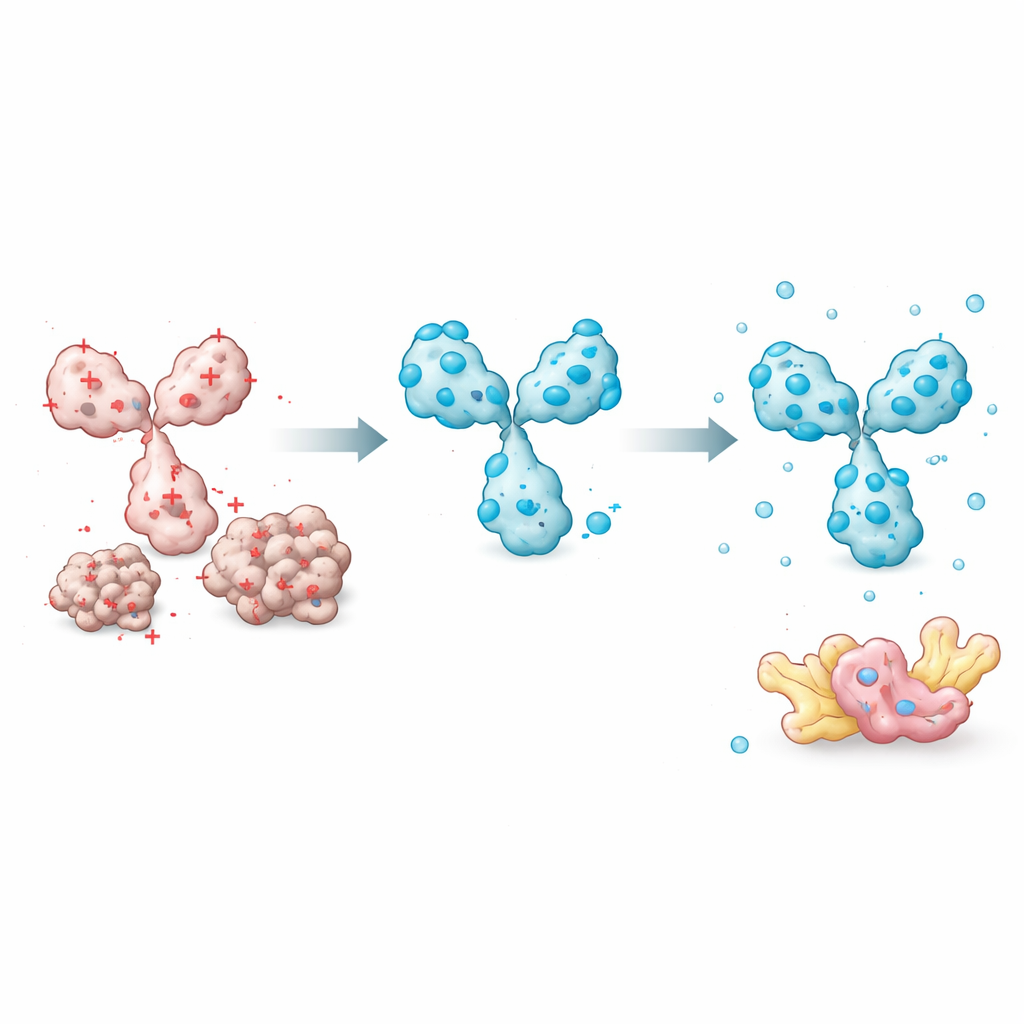
Mit dieser Erkenntnis konzentrierte sich das Team auf Merkmale, die sich leicht anpassen lassen, ohne die Zielerkennung zu stören. Ein Schlüsselelement ist der kurze Peptid‑„Linker“, der die beiden variablen Domänen verbindet. Die meisten bestehenden Designs verwenden neutrale Linker, die die Ladung nicht verändern. Durch den Austausch an diesen Positionen gegen negativ geladene Aminosäuren konnten die Forscher die Gesamtladung des Intrakörpers senken und die Löslichkeit drastisch verbessern, während die Zielbindung erhalten blieb. Sie entdeckten außerdem, dass die Reihenfolge der variablen Domänen (ob der schwere oder der leichte Teil zuerst kommt) und bestimmte Rahmenpositionen außerhalb der Bindungsschleifen beeinflussen, wie leicht das Protein faltet und gelöst bleibt. Eine Domänenanordnung zu wählen, die empfindlichere Bereiche schützt, und gezielt platzierte Ladungs‑Tauschaktionen zu introduzieren, steigerte die Leistungsfähigkeit weiter.
Künstliche Intelligenz nutzen, um Intrakörper in großem Maßstab zu bauen
Um über individuelles Ausprobieren hinauszukommen, kombinierten die Autoren ihre einfachen Ladungsregeln mit fortgeschrittener Proteindesign‑Software auf Basis tiefer neuronaler Netze. Ausgehend von bekannten Antikörper‑Rückgraten verwendeten sie einen „inverse folding“‑Ansatz, um neue Sequenzen vorzuschlagen, die die gewünschte Form annehmen, aber Oberflächeneigenschaften — insbesondere Ladungsmuster — aufweisen, die Stabilität und Löslichkeit begünstigen. Änderungen an den entscheidenden Bindungsschleifen wurden eingeschränkt, um die Erkennung zu bewahren, während der Algorithmus die umliegenden Oberflächen neu gestalten durfte. Tests zeigten, dass viele dieser KI‑gelenkten Intrakörper nicht nur hoch löslich, sondern auch thermisch stabiler waren als von Menschen entworfene Varianten und dabei die Fähigkeit behielten, krankheitsrelevante Ziele wie fehlgefaltetes SOD1, p53, α‑Synuclein und andere mit Neurodegeneration assoziierte Proteine zu binden.
Eine Bibliothek zellinnerer Proteinfänger aufbauen
Indem sie diese Regeln und Werkzeuge großflächig anwendeten, formatierten die Forscher rechnerisch 672 Antikörper in Intrakörper um, von denen vorhergesagt wurde, dass sie in Zellen gut funktionieren. Diese konstruierten Moleküle decken mehr als 60 verschiedene intrazelluläre Ziele ab, darunter Proteine, die an Alzheimer, Parkinson und Huntington beteiligt sind, sowie krebsbezogene Faktoren und posttranslationale Modifikationen wie Phosphorylierung und Acetylierung. In Versuchen zogen ausgewählte Intrakörper spezifische krankheitsverknüpfte Proteinformen an — etwa mutiertes SOD1 oder bestimmte Konformationen von α‑Synuclein — während sie die normalen Varianten ignorierten. Alle Sequenzen wurden offen zugänglich gemacht, und die Autoren stellen ein Web‑Tool zur Verfügung, mit dem andere die Löslichkeit von Intrakörpern aus der Sequenz mithilfe desselben ladebasierten Modells abschätzen können.
Was das für zukünftige Medikamente und Forschung bedeutet
Praktisch gesehen verwandelt diese Arbeit die umfangreiche, bereits vorhandene Sammlung von Antikörpern — viele davon schon klinisch untersucht — in ein Toolkit, das sich zuverlässig für den Einsatz innerhalb von Zellen anpassen lässt. Durch die Befolgung einer einfachen Reihe von Gestaltungsregeln können Forschende nun Intrakörper erstellen, die mit hoher Wahrscheinlichkeit beim ersten Versuch funktionieren, was Zeit und Kosten spart. Für Laien lautet die Kernbotschaft: Wissenschaftler haben eine einfache Methode gefunden, unsere besten Proteinerkenner so „umzuprogrammieren“, dass sie im überfüllten Inneren lebender Zellen funktionieren, wo viele Krankheiten beginnen. Dies könnte die Entwicklung neuer Möglichkeiten beschleunigen, krankheitsauslösende oder -begleitende fehlgefaltete Proteine zu verfolgen, zu untersuchen und schließlich zu behandeln.
Zitation: O’Shea, C.M., Shahzad, R., Aghasoleimani, K. et al. Reliable repurposing of the antibody interactome inside the cell. Nat Commun 17, 2222 (2026). https://doi.org/10.1038/s41467-026-69057-0
Schlüsselwörter: Intrakörper, Antikörper‑Engineering, Proteinlöslichkeit, neurodegenerative Erkrankung, Künstliche Intelligenz in der Biologie