Clear Sky Science · de
Regulierung von Grenzflächenwasser für Sauerstoffübertragung an benzyliche C(sp3)–H-Bindungen über Ni-aktivierte Wolfram‑Sauerstoff‑Kovalenz
Aus Wasser und Öl nützliche Chemikalien machen
Chemiker suchen seit langem nach saubereren Wegen, einfache ölbasierte Moleküle in wertvollere Bausteine für Kunststoffe, Arzneimittel und Alltagsprodukte zu verwandeln. Diese Studie zeigt, wie das feine „Abstimmen“ der dünnen Wasserschicht, die eine Elektrode berührt, gewöhnlichem Wasser erlaubt, Sauerstoff an hartnäckige Kohlenwasserstoffe abzugeben — wodurch Abfall und Energieverbrauch reduziert werden.
Warum Sauerstoff aus Wasser wichtig ist
Viele industrielle Chemikalien entstehen, indem Sauerstoff an Kohlenwasserstoffe gebunden wird — Moleküle, die überwiegend aus Kohlenstoff und Wasserstoff bestehen. Heute bedeutet das oft den Einsatz starker Oxidationsmittel und hoher Temperaturen, was großen Energieaufwand und klimawirksame Emissionen zur Folge hat. Wasser ist eine günstige, sichere und reichlich verfügbare Sauerstoffquelle, aber es direkt dazu zu bringen, diesen Sauerstoff an robuste C–H‑Bindungen abzugeben, erfordert üblicherweise sehr hohe Spannungen. Unter diesen harten Bedingungen geht ein großer Teil der elektrischen Energie dafür verloren, Wasser in Sauerstoffgas zu spalten, anstatt nützliche Produkte zu erzeugen.
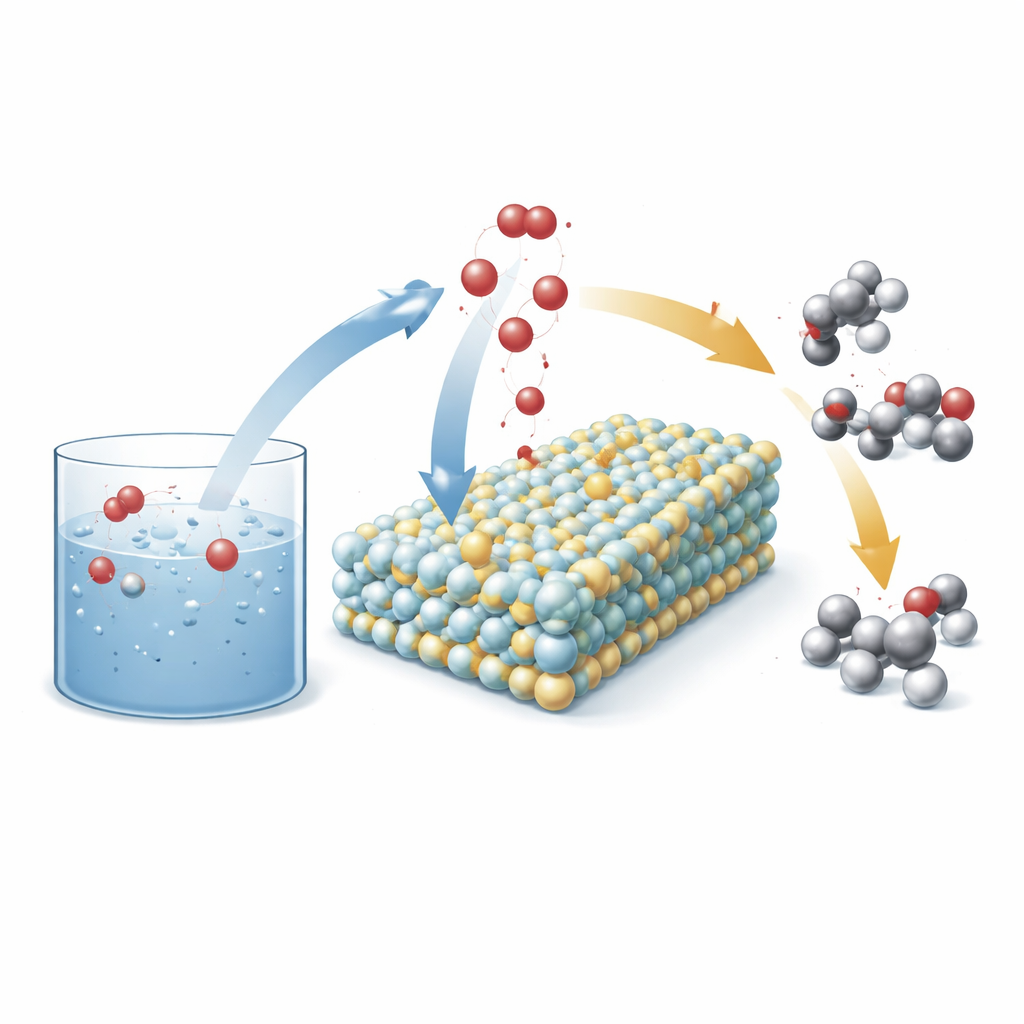
Eine clevere Elektrode, die Wasser umordnet
Die Forschenden entwickelten eine neue Art von Anode (die positive Elektrode in einer elektrochemischen Zelle) aus winzigen Wolframcarbid‑Partikeln, die sich während des Betriebs in ein amorphes Wolfram‑Sauerstoff‑Material umwandeln. In dieses Gerüst werden einzelne Nickelatome eingebracht. Unter Reaktionsbedingungen wandert Sauerstoff aus dem Wasser in das Feststoffgerüst und formt eine nickelaktivierte Wolframoxid‑Oberfläche mit vielen exponierten reaktiven Stellen. Diese neu entstandene Oberfläche dient dann als Plattform, auf der Wasser- und Kohlenwasserstoffmoleküle in kontrollierter Weise zusammentreffen und Sauerstoff austauschen — zugunsten wertvoller Produkte wie Alkohole und Ketone statt überoxidierter Säuren und anderer Nebenprodukte.
Die Wasser‑Hülle an der Oberfläche lockern
Eine zentrale Entdeckung ist, dass Nickelatome die Packungsweise der Wassermoleküle an der Elektrode subtil stören. Normalerweise bildet Wasser an einer geladenen Oberfläche ein dichtes Netz aus Wasserstoffbrücken, ähnlich einem engen Geflecht, das Bewegungen verlangsamt. Computersimulationen und empfindliche Infrarotmessungen zeigen, dass sich dieses Netzwerk in nickeldotierten Bereichen lockert — mit weniger Wasserstoffbrücken und mehr „freien“ Wassermolekülen. Dadurch entstehen Kanäle, durch die Wasser leichter zu den reaktiven Wolfram‑Sauerstoff‑Stellen diffundieren kann. Infolgedessen können sauerstoffhaltige Fragmente aus dem Wasser die Oberfläche schneller und häufiger erreichen und die Reaktion speisen, anstatt als Sauerstoffgas zu entweichen.
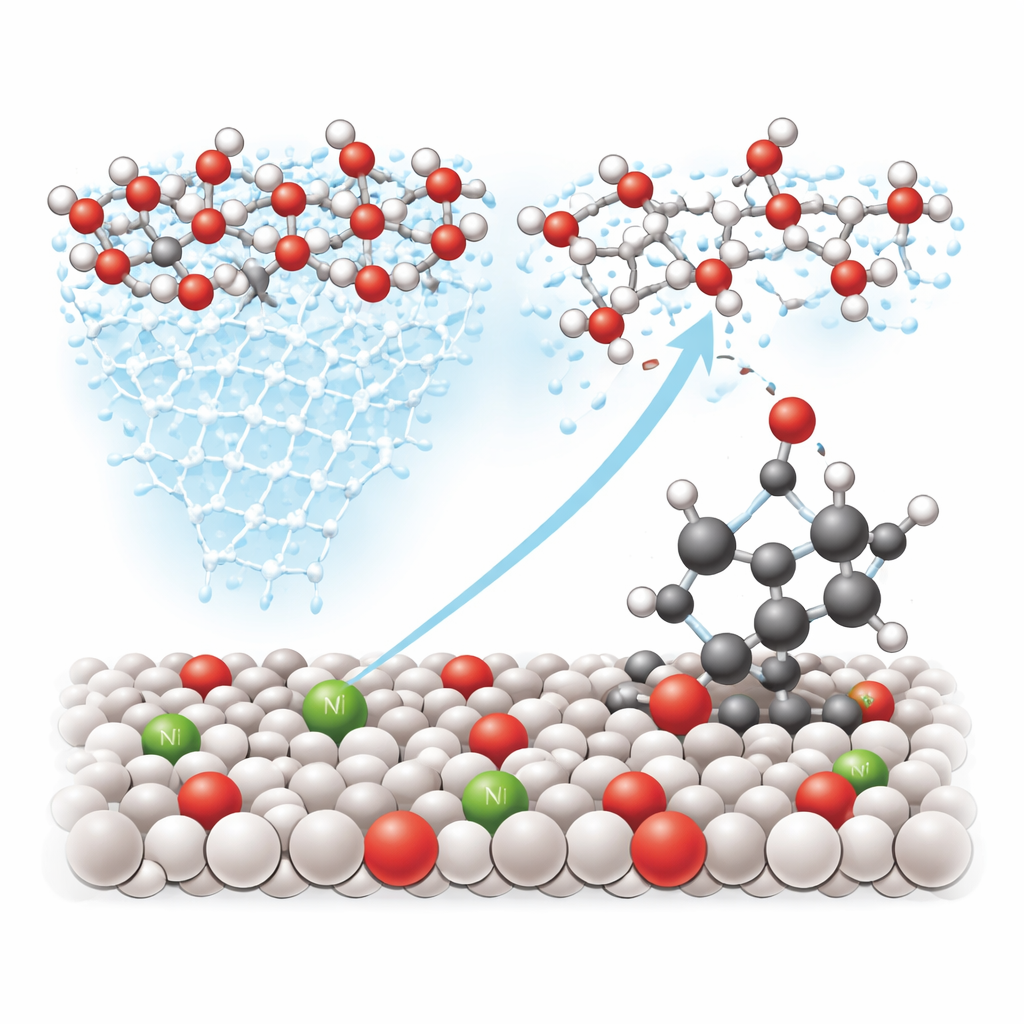
Sauerstoff zu den richtigen Bindungen lenken
Über die verbesserte „Verkehrsführung“ an der Oberfläche hinaus stimmt Nickel auch die elektronische Struktur benachbarter Wolframatome so ab, dass bestimmte Stellen besonders gut darin sind, Wasser zu binden und zu aktivieren. Die Experimente mit Isotopen — speziellen Versionen von Sauerstoff und Wasserstoff, die verfolgt werden können — zeigen, dass der aktive Sauerstoff aus frisch gespaltenem Wasser stammt und nicht aus dem Volumen des Oxids selbst. Spektroskopische „Momentaufnahmen“ erfassen eine kurzlebige Brücke zwischen Wolfram, Sauerstoff und dem benzylichem Kohlenstoff an Molekülen wie Ethylbenzol. Theoretische Rechnungen bestätigen, dass es auf der nickelmodifizierten Oberfläche leichter ist, dass ein Sauerstoffatom diese C–H‑Stelle angreift, als dem üblichen Wasser‑Spaltungsweg zu folgen, der Sauerstoffgas erzeugt — wodurch die Reaktion effektiv in Richtung nützlicher oxygenierter Produkte gelenkt wird.
Effizient, selektiv und langlebig
In Tests wandelt die nickelaktivierte Elektrode eine Reihe benzylicher C–H‑Bindungen in Alkohole und Ketone um, mit Faraday‑Wirkungsgraden — dem Anteil der elektrischen Ladung, der in die gewünschte Chemie fließt — typischerweise über 50 % und in optimierten Fällen über 56 %. Das System läuft über viele Zyklen, ohne an Aktivität zu verlieren, und erhält dabei seine Nickel‑Wolfram‑Struktur. Da es Wasser als einzige Sauerstoffquelle nutzt und zusätzliche chemische Oxidationsmittel vermeidet, bietet es eine wettbewerbsfähige Energieeffizienz und geringere Materialkosten im Vergleich zu anderen fortgeschrittenen Methoden. Auch wenn der aktuelle Anwendungsbereich auf benzyliche Stellen fokussiert ist, deutet das zugrundeliegende Prinzip — atomare Zusätze zu verwenden, um Grenzflächenwasser umzustrukturieren und Reaktionspfade umzuleiten — auf ein breiteres Instrumentarium für grünere, elektrisch getriebene Oxidationen ansonsten träger C–H‑Bindungen hin.
Was das für sauberere Chemie bedeutet
Diese Arbeit zeigt, dass kleine Änderungen auf atomarer Ebene überproportionale Auswirkungen darauf haben können, wie Wasser an einer Elektrode reagiert und wo sein Sauerstoff landet. Indem Nickelatome sowohl die Struktur des Grenzflächenwassers lockern als auch reaktive Stellen feinjustieren, verwandeln die Autorinnen und Autoren Wasser in einen effizienten Sauerstoffspender für schwer aktivierbare Kohlenstoff‑Wasserstoff‑Bindungen und unterdrücken zugleich die unerwünschte Bildung von Sauerstoffgas. Langfristig könnten solche Strategien dazu beitragen, die Oxidationschemie in der chemischen Industrie neu zu gestalten — energieeffizienter und klimafreundlicher durch Einsatz von Strom und Wasser statt harter Oxidantien und fossiler Ausgangsstoffe.
Zitation: Leng, BL., Lin, X., Dong, HY. et al. Regulating interfacial water for oxygen transfer to benzylic C(sp3)–H bonds via Ni-activated tungsten-oxygen covalency. Nat Commun 17, 2355 (2026). https://doi.org/10.1038/s41467-026-69054-3
Schlüsselwörter: Elektrokatalyse, Wasseroxidation, Benzyliche C–H‑Aktivierung, nickeldotiertes Wolframoxid, grüne Chemie