Clear Sky Science · de
Mosaikartige partielle epidermale Reprogrammierung gestaltet Nachbarzellen und Nischen um, um Hauthomöostase und Reparatur zu verfeinern
Der Haut beim Selbstheilen helfen
Wer schon einmal mit einer langsam heilenden Schnittwunde oder einer hartnäckigen Narbe zu tun hatte, wünscht sich oft, die Haut könnte sich schneller und sauberer reparieren. Diese Studie untersucht einen Weg, einige Hautzellen behutsam „zurückzusetzen“, sodass das gesamte Gewebe besser zur Heilung befähigt wird. Indem eine kleine Teilmenge von Zellen kurzzeitig in einen flexibleren, jüngeren Zustand gedrängt wird, zeigen die Autorinnen und Autoren, dass sich die Maus-Haut so vorbereiten lässt, dass Wunden schneller schließen und kleinere, weichere Narben entstehen—ohne die Zellen in gefährliche, tumorähnliche Zustände zu verwandeln.
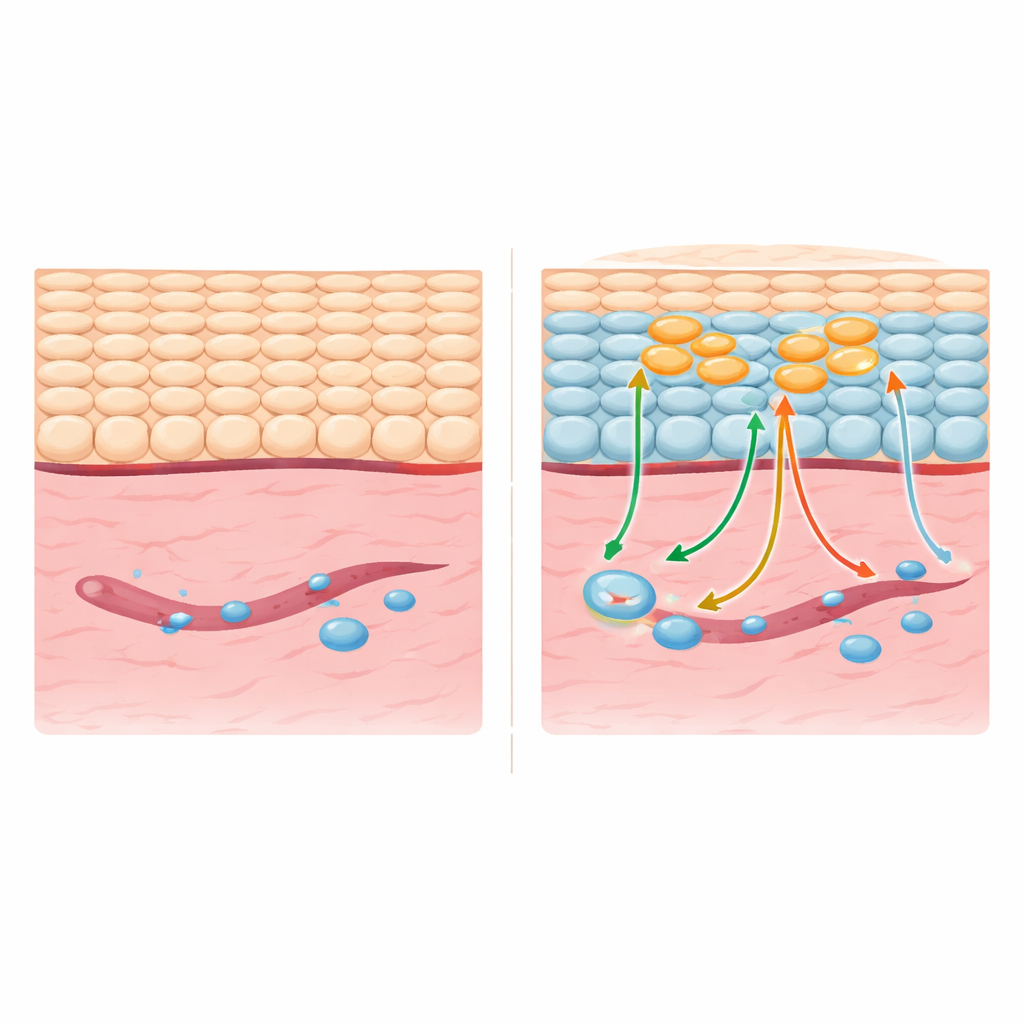
Die Zell‑Uhr sanft zurückdrehen
Die Forschenden konzentrierten sich auf die äußerste Hautschicht, das Epidermis, die kontinuierlich von erwachsenen Stammzellen erneuert wird. Anstatt zu versuchen, jede Zelle umzuprogrammieren, konstruierten sie Mäuse so, dass nur verstreute epidermale Zellen kurzzeitig vier bekannte „Reprogrammierungs“-Proteine (häufig Yamanaka‑Faktoren genannt) anschalteten. Dieser kurze Impuls löschte nicht die Identität der Zellen und machte sie nicht vollständig stammzellartig; sie exprimierten keine Schlüsselmarker der Pluripotenz und bildeten keine Tumoren. Stattdessen kehrten sowohl die reprogrammierten Zellen als auch einige ihrer Nachbarn teilweise von ihrem normalen Weg vom stammzellähnlichen zum voll ausdifferenzierten Zustand um und erhielten Merkmale jüngerer, flexiblerer Epidermiszellen zurück, während sie in der Hautlinie blieben.
Wellenartige Effekte in benachbarten Zellen
Mithilfe von Einzelzell-RNA-Sequenzierung zeigte das Team, dass diese mosaikartige partielle Reprogrammierung nicht nur die Zielzellen veränderte, sondern auch benachbarte Zellen, die niemals die Reprogrammierungsfaktoren exprimierten. Viele epidermale Zellen traten in einen Zustand ein, der eng an Zellen erinnerte, wie man sie nach einer tatsächlichen Verletzung findet: Markern aktiver, wandernder Keratinozyten wurden eingeschaltet, und Gene, die an Stress‑, Hypoxie‑ und Entzündungssensorik beteiligt sind, waren erhöht. Wichtig war, dass nur die direkt reprogrammierten Zellen einen Anstieg der Zellteilung zeigten, während die Nachbarn einen auf Reparatur eingestellten Zustand annahmen, ohne übermäßige Proliferation. Dieses Gleichgewicht ließ sich auf unterschiedliche Signalwege zurückführen: Reprogrammierte Zellen aktivierten einen wachstumsfördernden PI3K‑Signalweg, der wiederum EGFR‑Signale und sekretierte Faktoren verstärkte, die „Heilungssignale“ an umliegende Zellen weitergaben, während andere Signale die WNT‑Aktivität in den Nachbarn dämpften, um unkontrolliertes Wachstum zu verhindern.
Einbeziehung des Immunsystems und der Blutgefäße
Das Reparaturprogramm der Haut umfasst mehr als nur Epidermiszellen, und die partielle Reprogrammierung gestaltete auch diese „Nischen“ um. Die veränderte Epidermis produzierte Chemokine, die bestimmte T‑Zellen anlockten und aktivierten, von denen bekannt ist, dass sie die Wundverschließung unterstützen. Ein Signalweg, angetrieben vom Chemokin CCL20 und seinem Rezeptor CCR6, zog RORγt‑positive T‑Zellen an, die typischerweise an Wundrändern auftreten und die Re‑epithelialisierung fördern. Gleichzeitig wurde ein zentraler Stresssensor, HIF‑1α, in der Epidermis aktiviert und beeinflusste das Muster des Neubaus von Blutgefäßen in der darunterliegenden Dermis. Dies führte dazu, dass Gefäße näher an den ursprünglichen Wundrändern entstanden und mit der Zeit das vaskuläre Wachstum so organisierten, dass es mit qualitativ besserer Reparatur und nicht mit dichter, fibröser Narbenbildung assoziiert war.
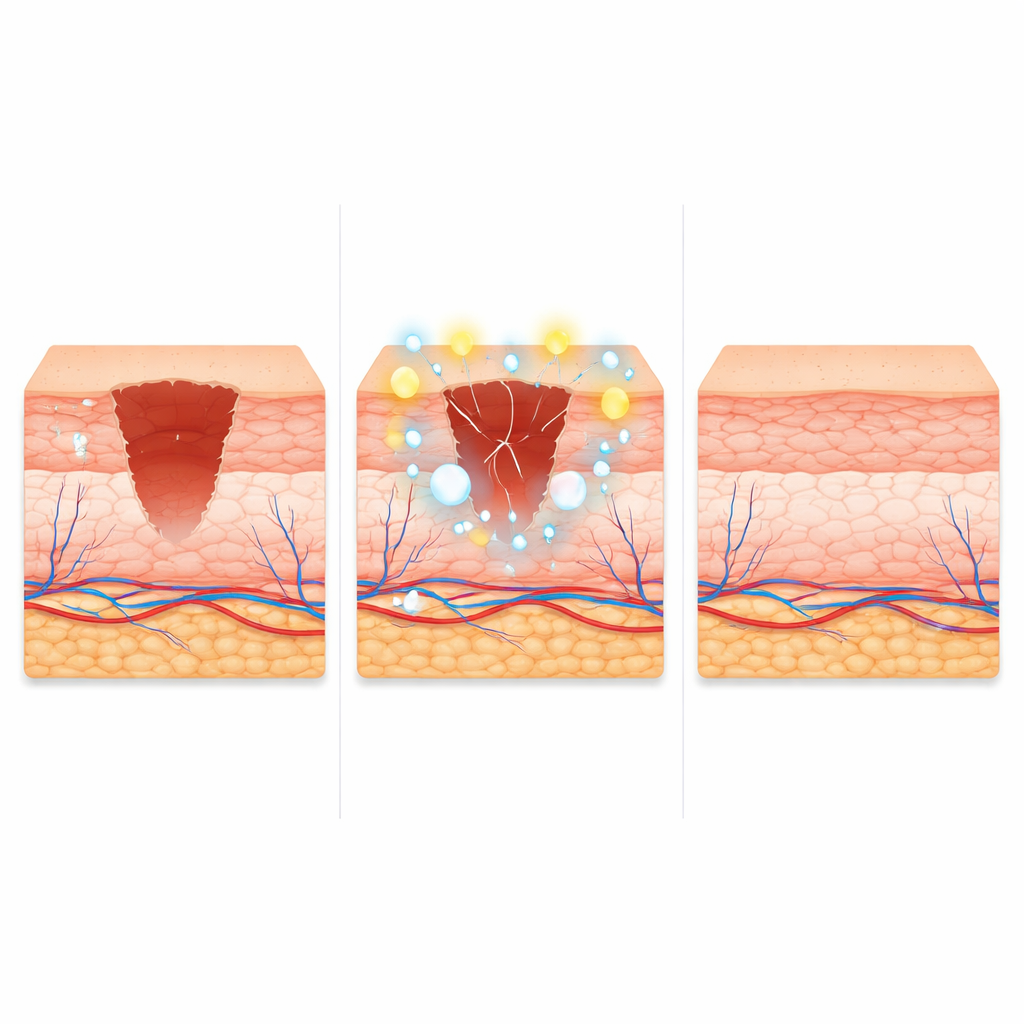
Bessere Heilung und weniger Narbenbildung in gesunder und diabetischer Haut
Als die Forschenden bei diesen Mäusen Vollschichtwunden anlegten und gleichzeitig kurzzeitig partielle Reprogrammierung induzierten, schloss die Haut schneller. Die wandernde Epidermiskante rückte weiter vor, die Barriere erholte sich früher, und die resultierenden Narben waren dünner, mit Kollagenfasern, die dem unverletzten Hautbild näherkamen und einem geringeren Anteil unreifen Kollagens. Eine vorübergehende Blockade von HIF‑1α hob einen Großteil dieses Nutzens auf und unterstrich seine zentrale Rolle. Bemerkenswerterweise verbesserte dieselbe Strategie auch die Heilung bei diabetischen Mäusen, die normalerweise schlecht heilen: Wunden schlossen schneller, proliferative Defekte in Epidermiszellen wurden behoben und das Gefäßwachstum im Wundbett erholte sich teilweise. Wenn die Reprogrammierung jedoch über das kurze Fenster hinaus verlängert wurde, entwickelten sich entzündliche Veränderungen und Verdickungen der Haut, was die Notwendigkeit einer strikten Kontrolle von Dosis und Timing hervorhebt.
Was das für zukünftige Therapien bedeuten könnte
Insgesamt zeigt die Arbeit, dass ein leichtes und temporäres „Auflockern“ einer Teilmenge von Hautzellen ihre Kommunikation mit Nachbarn und Stütz‑/Nischenzellen umprogrammieren kann und so das gesamte Gewebe in einen koordinierten, reparaturfördernden Zustand schiebt. Indem nützliche partielle Reprogrammierung von gefährlicher vollständiger Reprogrammierung getrennt wird und mosaikartige statt globale Veränderungen genutzt werden, weist die Studie auf künftige Behandlungsansätze hin, die eines Tages das Wundverschlussverhalten beschleunigen und Narbenbildung reduzieren könnten—selbst bei Menschen mit Erkrankungen wie Diabetes—indem sie sicher die regenerativen Fähigkeiten der Haut stärkt.
Zitation: Kwak, M., Choi, E., Jo, Y. et al. Mosaic partial epidermal reprogramming remodels neighbors and niches to refine skin homeostasis and repair. Nat Commun 17, 2191 (2026). https://doi.org/10.1038/s41467-026-69047-2
Schlüsselwörter: Hautregeneration, Wundheilung, zelluläre Reprogrammierung, Stammzellnischen, Narbenreduktion