Clear Sky Science · de
Das an die bakterielle RNA-Polymerase gebundene Protein CarD koppelt Promotoraktivität an DNA-Supercoiling
Wie Bakterien ihre Gene an Auf und Ab des Lebens anpassen
Innerhalb jeder bakteriellen Zelle wird die DNA ständig verdreht, wieder entdreht und gelesen. Diese Arbeit untersucht, wie ein kleines Hilfsprotein namens CarD zusammen mit der physikalischen Verwindung der DNA wirkt, um essentielle Gene hoch- oder herunterzuregeln. Das Verständnis dieser Partnerschaft zeigt, wie Bakterien ihre grundlegenden „Hausarbeits“-Aktivitäten—wie den Aufbau von Ribosomen und die Proteinsynthese—an veränderte Bedingungen anpassen, etwa bei schnellem Wachstum oder Stress.
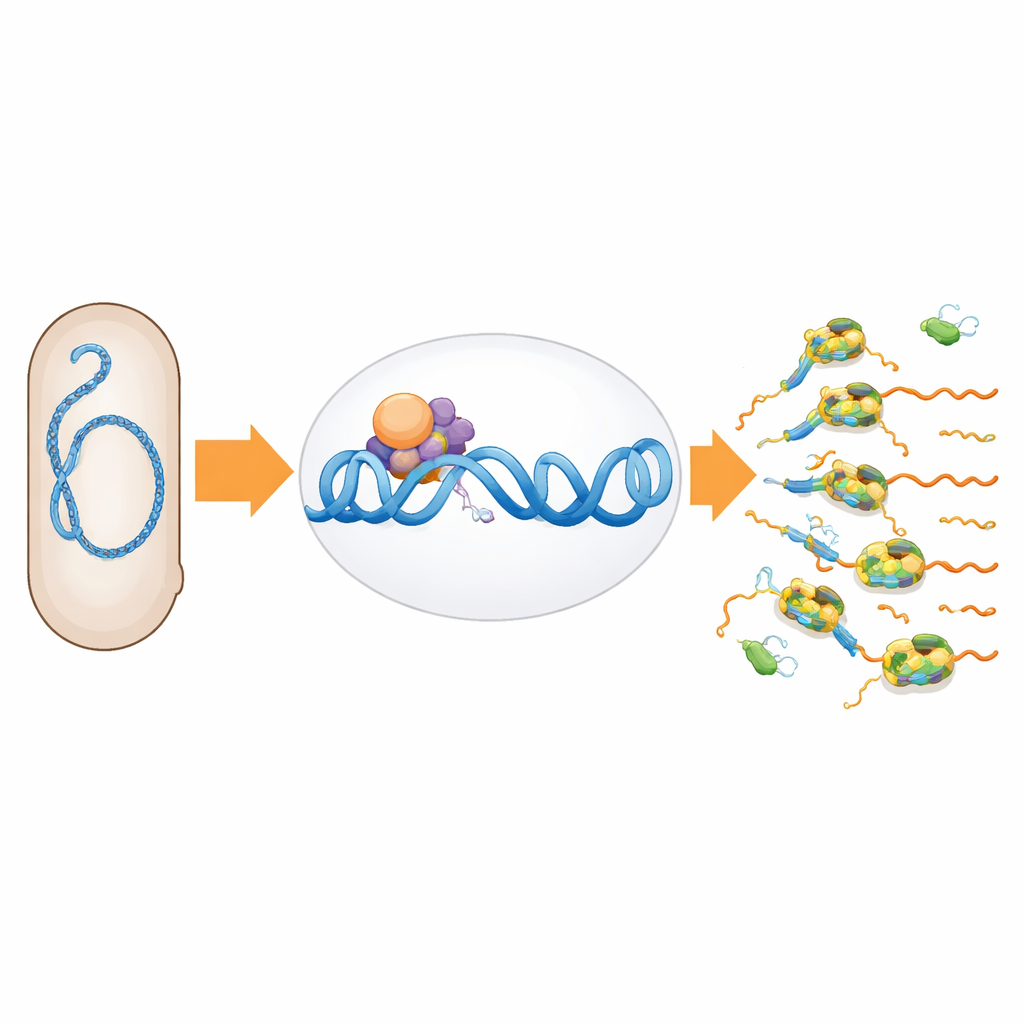
Die Herausforderung, DNA zu öffnen
Um ein Gen abzulesen, muss ein bakterielles Enzym, die RNA-Polymerase, zunächst einen kurzen Abschnitt der DNA-Doppelhelix an einer Kontrollregion, dem Promotor, aufbrechen. Viele Bakterien verwenden an diesen Promotoren ein standardisiertes DNA-Muster, das das Auftrennen relativ leicht macht. Rhodobacter sphaeroides, ein photosynthetisches Bakterium, ist ungewöhnlich: Mehr als die Hälfte seiner Promotoren fehlen an einer entscheidenden Position eine wichtige DNA-Base. Für sich genommen würde dieser Mangel das Öffnen der DNA deutlich erschweren, dennoch treiben diese Promotoren weiterhin eine starke Expression lebenswichtiger Gene an, darunter solche für die Proteinfabriken der Zelle.
Ein Helferprotein ersetzt defekte Schalter
Die Autoren zeigen, dass Rhodobacter dieses Problem mit dem Protein CarD löst, das sich neben der RNA-Polymerase an Promotoren bindet. CarD drückt wie ein Keil in die DNA und hilft so, die beiden Stränge zu trennen, damit die Transkription beginnen kann. Durch Kartierung von Tausenden Transkriptionsstartpunkten und der Bindungsorte von CarD und RNA-Polymerase im Genom fanden die Forscher heraus, dass CarD eng mit Promotoren verknüpft ist, die das defekte DNA-Muster tragen. Diese fehlerhaften Schalter rekrutieren damit effektiv CarD als eingebauten Stabilisator, wodurch Gene trotz schwächerer Sequenzen eingeschaltet werden können.
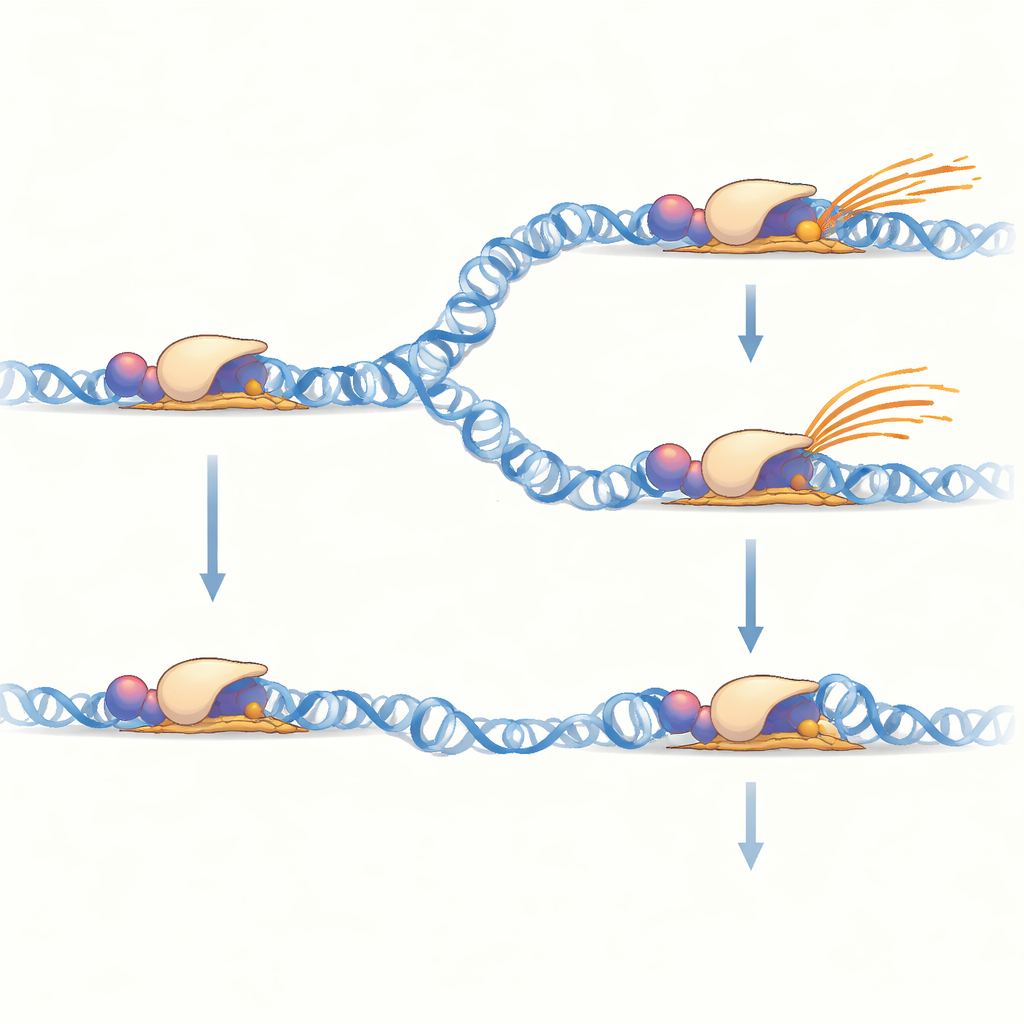
Verdrehte DNA als zweiter Regelknopf
DNA in Zellen ist keine entspannte gerade Leiter; sie ist oft über- oder unterverdreht, eine Eigenschaft, die als Supercoiling bezeichnet wird. Unterverdrehte (negativ supercoiled) DNA lässt sich leichter öffnen, während entspannte DNA dem Aufwickeln widersteht. Mit einer Methode, die unterdrehte DNA-Abschnitte markiert, erstellten die Autoren eine genomweite Karte des Supercoilings und entdeckten, dass CarD-gebundene Promotoren sich in besonders unterverdrehten Regionen befinden. Behandelten sie Zellen mit einem Wirkstoff, der die DNA entspannt, indem er ein Enzym blockiert, das normalerweise negative Verwindungen hinzufügt, verloren diese CarD-gebundenen Promotoren sowohl CarD als auch die RNA-Polymerase, und die benachbarten Gene wurden größtenteils herunterreguliert. Das zeigte, dass CarD’s Fähigkeit, die DNAöffnung zu unterstützen, stark vom geeigneten Verdrehungszustand der umgebenden DNA abhängt.
Promotoren rekonstruieren und ihre Reaktion beobachten
Um Ursache und Wirkung direkter zu testen, rekonstruierte das Team Schlüsselpromotoren auf zirkulären DNA-Molekülen und veränderte systematisch sowohl die DNA-Sequenz als auch deren Verdrehung in Reaktionen im Reagenzglas. Für einen wichtigen Ribosompromotor, der normalerweise CarD benötigt, stellten sie fest, dass CarD nur dann die Aktivität steigern konnte, wenn die DNA ausreichend unterverdreht war. Reparierten die Forscher die fehlende Base im Promotor, konnte CarD selbst auf entspannter DNA aktivieren, und starkes Supercoiling wurde weniger kritisch. Umgekehrt konnte beim Promotor, der das carD-Gen selbst kontrolliert, CarD in Kombination mit starker negativer Verwindung die geöffnete DNA überstabilisieren und die Transkription unterdrücken, während das gleiche Protein auf entspannter DNA eine aktivierende Rolle einnahm. Durch den Bau hybrider Promotoren, die Teile aus diesen verschiedenen Schaltern kombinierten, zeigten die Autoren, dass subtile Sequenzmerkmale und die DNA-Form CarD’s Wirkung eher in Richtung Aktivierung oder Repression kippen können.
Wachstum, Stress und zentrale Zellarbeit verknüpfen
Untersuchten die Autoren, welche Gene sowohl von CarD als auch von negativem DNA-Supercoiling abhängen, fanden sie viele, die an grundlegenden Prozessen beteiligt sind, etwa beim Aufbau von Ribosomen und Transfer-RNAs—Teile der Maschinerie, die schnelles Wachstum antreibt. In langsam wachsenden oder gestressten Zellen wird die globale DNA entspannter, und CarD bindet an diesen Stellen weniger stark, wodurch die Expression dieser energieintensiven Gene sinkt. Auf diese Weise wirken CarD und DNA-Supercoiling gemeinsam als mechanischer Sensor, der die grundlegende Genexpression an den physikalischen und Umweltzustand der Zelle koppelt.
Warum das für das Verständnis von Bakterien wichtig ist
Für Laien zeigt diese Studie, dass Bakterien sich nicht allein auf genetische „Software“ (DNA-Sequenzen) verlassen, um ihr Verhalten zu steuern; sie nutzen auch die physikalische „Hardware“ der DNA-Verdrehung sowie Hilfsproteine wie CarD, um feinzujustieren, welche Gene aktiv sind. In Rhodobacter sphaeroides sind viele Promotoren absichtlich schwach ausgelegt und werden dann von CarD gerettet—aber nur, wenn die DNA so verdreht ist, dass sie günstige Wachstumsbedingungen signalisiert. Wenn sich die DNA unter Stress entspannt, beruhigen sich diese Gene von selbst. Diese eingebaute Verbindung zwischen DNA-Mechanik und Genkontrolle dürfte in vielen Bakterien wirken und ihnen helfen, ihre grundlegenden Haushaltsfunktionen schnell an wechselnde Umgebungen anzupassen.
Zitation: Forrest, D., Warman, E.A. & Grainger, D.C. The bacterial RNA polymerase-associated CarD protein couples promoter activity to DNA supercoiling. Nat Commun 17, 2295 (2026). https://doi.org/10.1038/s41467-026-69038-3
Schlüsselwörter: DNA-Supercoiling, bakterielle Transkription, CarD-Protein, Genregulation, Rhodobacter sphaeroides