Clear Sky Science · de
In vivo Dual‑RNA‑Seq enthüllt Schlüssel‑Effektoren für die Störung der epithelialen Barriere durch einen extrazellulären Erreger
Wie einige Keime unsere zellulären Zäune umgehen
Unsere Organe sind von dicht aneinandergereihten Zellen ausgekleidet, die wie Mauern wirken und Blut, Mikroben und Toxine an ihrem Platz halten. Dennoch schlüpfen bestimmte Keime zwischen diesen Zellen hindurch und verbreiten sich im Körper. Diese Studie zeigt anschaulich, wie das Bakterium, das Leptospirose verursacht — eine weltweit ernste Erkrankung — still in Organe wie Leber und Niere gelangt und dabei einen ausgeklügelten Trick nutzt: es beeinflußt das intrazelluläre Calcium, um diese Schutzbarrieren aufzubrechen.
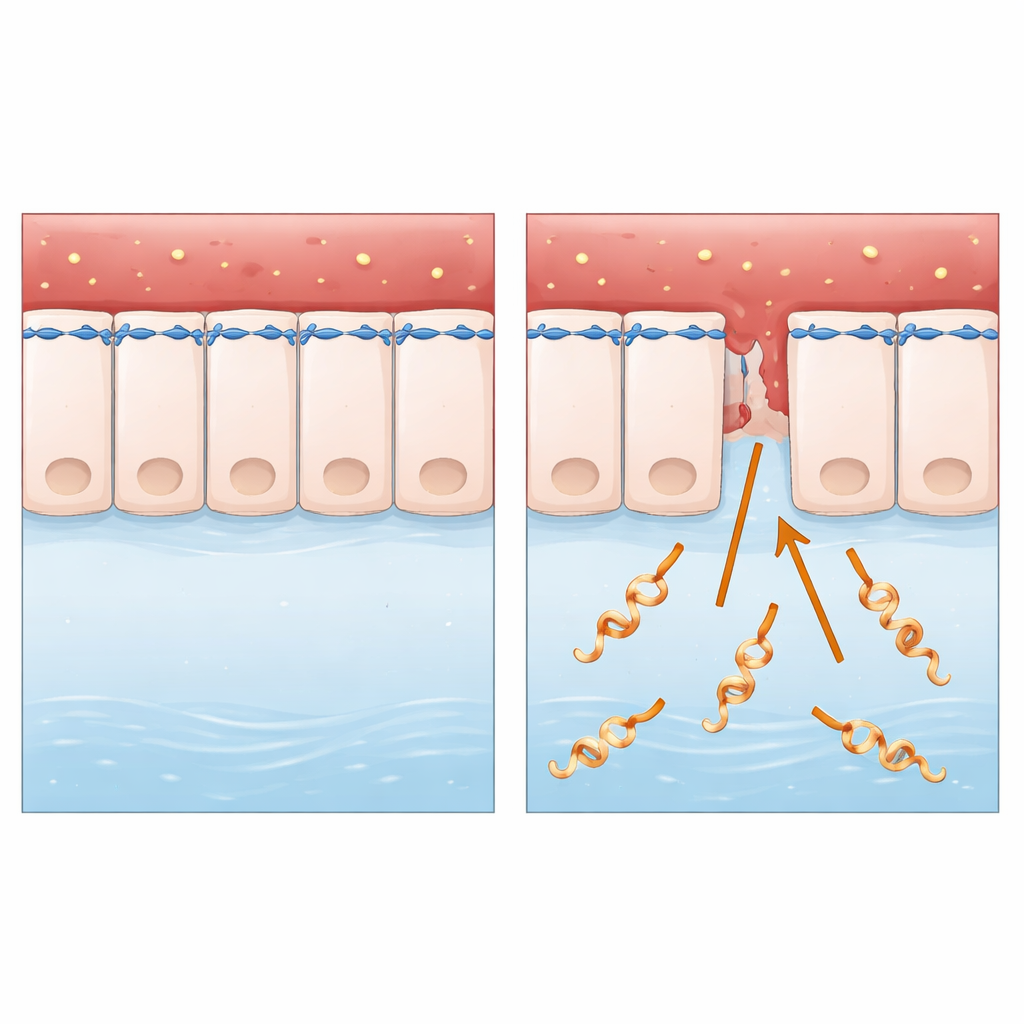
Ein heimlicher Eindringling in Tier- und Menschengewebe
Die Forschung konzentriert sich auf Leptospira interrogans, ein spiralförmiges Bakterium, das hauptsächlich von Tieren auf Menschen über verunreinigtes Wasser oder Erdreich übertragen wird. Nach dem Eindringen über kleine Hautverletzungen oder Schleimhäute gelangt es in die Blutbahn und kann schwere Erkrankungen auslösen, darunter Leber‑ und Nierenversagen sowie innere Blutungen. Anders als viele gut untersuchte Mikroben lebt Leptospira außerhalb von Zellen und fehlt es an einigen der klassischen „molekularen Waffen“, nach denen Forscher normalerweise suchen. Das machte es zu einem idealen Modell, um eine grundlegende Frage zu stellen: Wie überquert ein scheinbar einfacher, extrazellulärer Erreger intakte Zellschichten so effizient?
Zusehen, wie Wirts‑ und Keim‑Gene zugleich kommunizieren
Um den Infektionsprozess in einem lebenden Tier zu erfassen, nutzte das Team duales RNA‑Sequencing in Hamstern, einem Modell für akute Leptospirose. Diese Methode liest gleichzeitig ab, welche Gene beim Wirt und beim Erreger an- oder abgeschaltet werden. Die Wissenschaftler infizierten Hamster und entnahmen ein und drei Tage später Leber‑ und Nierengewebe. Anfangs, trotz hoher Bakterienzahlen, veränderte sich die Genaktivität der Wirtszellen kaum, was darauf hindeutet, dass Leptospira zunächst unter dem Radar des Immunsystems bleibt. Bis zum dritten Tag zeigten jedoch beide Organe eine starke Reaktion, besonders die Leber: Gene, die an Entzündung, Zell‑Zell‑Verbindungen und dem inneren Gerüst der Zellen beteiligt sind, waren deutlich verändert — ein Hinweis auf aktives Umbauen der Gewebebarrieren.
Den zellulären Reißverschluss von außen aufbrechen
Zellschichten sind durch Tight Junctions und Adherens Junctions abgedichtet, die benachbarte Zellen verbinden und an einen Ring aus Aktin und Myosin verankern — dasselbe Proteinpaar, das auch Muskeln zusammenziehen lässt. Die Mikroskopie humaner Epithelzellen, die mit Leptospira infiziert waren, zeigte Formveränderungen, auftretende Lücken zwischen Zellen und eine Abschwächung oder Fehlplatzierung wichtiger Junction‑Proteine. Wichtig ist: Die Zellen starben nicht, das heißt, die Barriere wurde auseinandergebaut, nicht zerstört. Die Forscher beobachteten außerdem Anzeichen von Stress in den Protein‑Faltungssystemen der Zellen, doch deren Blockade stellte die Junctions nicht wieder her, weshalb sie nach einem anderen Übeltäter suchten.
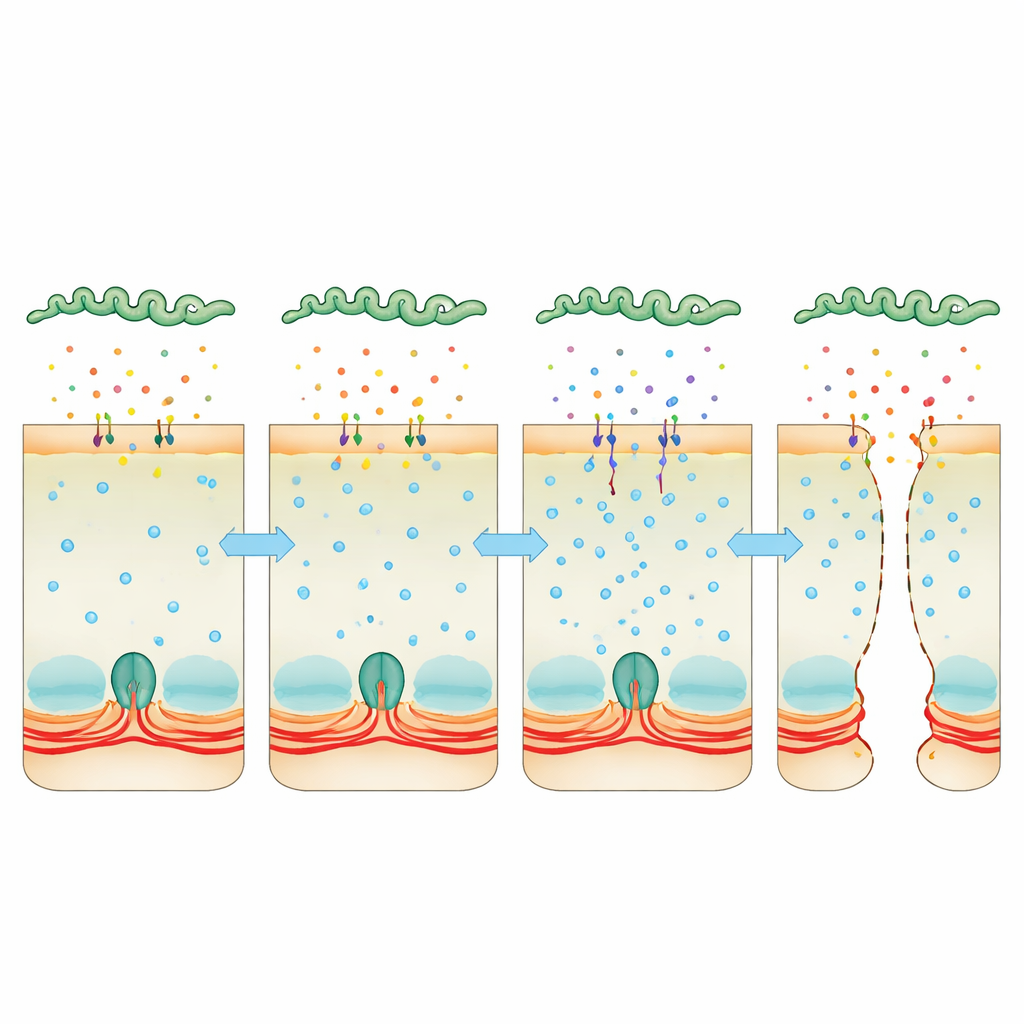
Calcium als verstecktes Brecheisen missbraucht
Der Fokus richtete sich auf Calcium, ein universelles intrazelluläres Signal, das den Aktin‑Myosin‑Ring anspannen oder entspannen kann. Infizierte Zellen häuften mehr Calcium an, was mit höherer Aktivität der Myosin‑Leichtketten‑Kinase (MLCK) verbunden war — einem Enzym, das den kontraktilen Ring anziehen lässt und so an den Junctions zieht. Als das Team ein Mittel verwendete, das Calcium bindet, oder Medikamente, die Calmodulin beziehungsweise diese Kinase hemmen, blieben die Zellschichten stabiler und die Bakterien taten sich schwerer, hindurchzupressen. Gleichzeitig zeigte tiefes Bakterien‑RNA‑Sequencing, dass Leptospira im Wirt stark die Produktion von zwei „Virulence‑Modifying“ Proteinen anhebt, die Toxinen ähneln. Diese Proteine werden sezerniert, haften an Wirtszellen und finden sich auch innerhalb dieser Zellen. Fehlen den Bakterien eines oder beide dieser Proteine, verlieren sie weitgehend die Fähigkeit, Zellschichten zu durchdringen oder tödliche Erkrankung zu verursachen, und ihre sezernierte Kulturflüssigkeit erhöht Calcium‑Spiegel oder zerstört Junctions nicht mehr so effektiv.
Folgen für Krankheit und künftige Abwehrstrategien
In der Summe zeichnen die Ergebnisse ein klares Bild. Nachdem Leptospira nahezu unbemerkt in den Körper gelangt ist, beginnt es, toxINähnliche Virulence‑Modifying‑Proteine zu sezernieren. Diese Proteine binden an Epithelzellen und stören das Calcium‑Gleichgewicht in deren Innerem, wodurch ein kontraktiler Signalweg aktiviert wird, der den zellulären „Reißverschluss“ zwischen benachbarten Zellen auseinanderzieht. Wenn Tight‑ und Adherens‑Junctions sich lockern, entstehen mikroskopische Lücken, durch die die Bakterien zwischen den Zellen hindurchwandern, Organe besiedeln und schwere Erkrankungen auslösen können. Indem die Studie diesen Calcium‑getriebenen Mechanismus und die verantwortlichen bakteriellen Proteine identifiziert, eröffnet sie Wege für neue Strategien — etwa das Blockieren dieser Proteine oder ihres Signalwegs — um unsere zellulären Zäune zu stärken und die Ausbreitung der Leptospirose und möglicherweise anderer Infektionen, die ähnliche Taktiken ausnutzen, einzudämmen.
Zitation: Giraud-Gatineau, A., Haustant, G., Monot, M. et al. In vivo dual RNA-Seq uncovers key effectors of epithelial barrier disruption by an extracellular pathogen. Nat Commun 17, 2274 (2026). https://doi.org/10.1038/s41467-026-69033-8
Schlüsselwörter: Leptospirose, epitheliale Barriere, Calcium‑Signalgebung, bakterielle Toxine, Wirts‑Pathogen‑Interaktionen