Clear Sky Science · de
Supercharging-verstärkte nDIA-MS ermöglicht globales Profiling von medikamentinduzierten Verschiebungen der Proteomlöslichkeit
Warum das Verhalten von Proteinen über bloße Mengen hinaus wichtig ist
Medikamente können nicht nur verändern, wie viel von einem Protein eine Zelle herstellt, sondern auch, wohin dieses Protein gelangt und ob es frei im Cytosol schwimmt oder an zelluläre Strukturen anlagert. Diese Verschiebungen im „Wo“ und „Wie“ des Proteinvorhandenseins in Zellen stehen in engem Zusammenhang mit Erkrankungen wie Krebs und Neurodegeneration, sind aber schwer in großem Maßstab zu messen. Diese Studie stellt eine schnelle, leistungsfähige Methode vor, um Tausende menschlicher Proteine gleichzeitig zu erfassen und zu sehen, wie ihre Löslichkeit – also ob sie in einem freien oder stärker gebundenen Zustand vorliegen – reagiert, wenn Zellen zwei weit verbreiteten experimentellen Wirkstoffen ausgesetzt werden.
Schneller und schärfer auf Proteine blicken
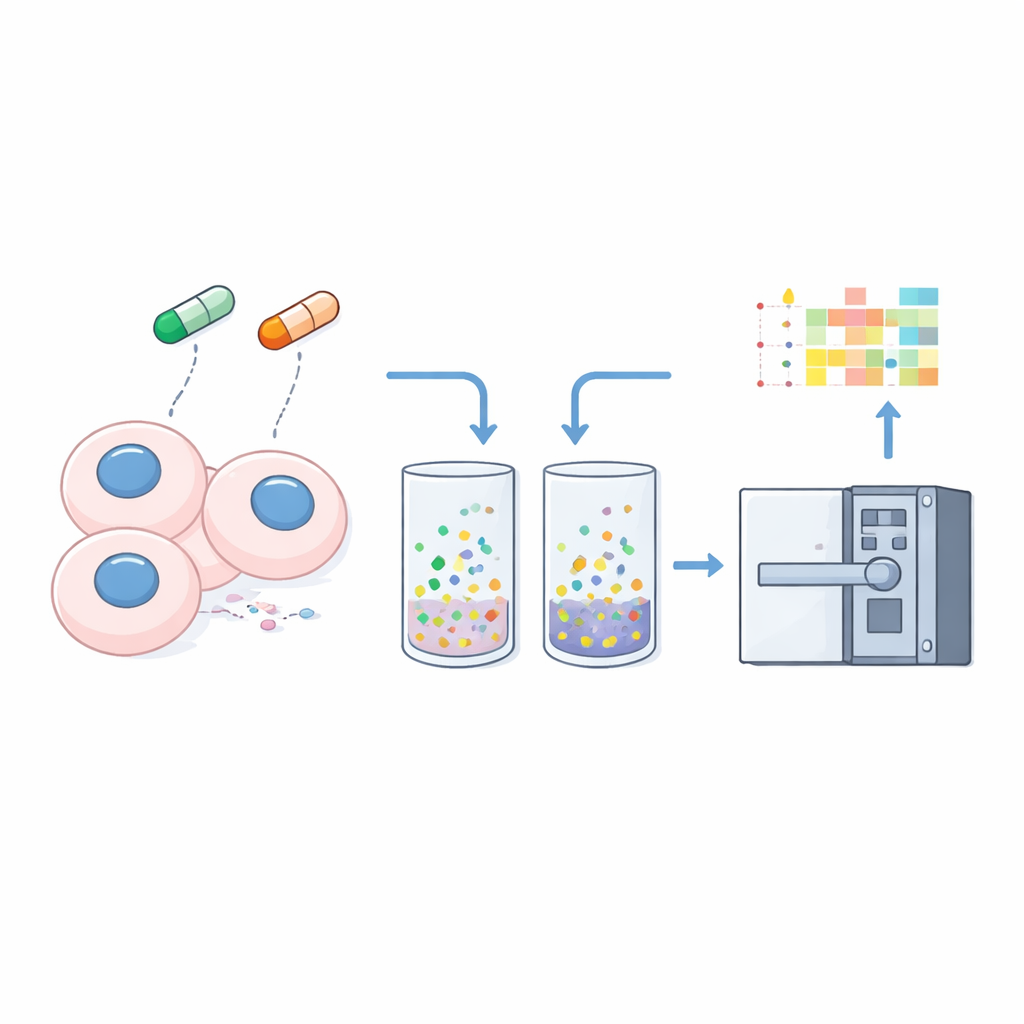
Die Autoren bauen auf einer Kerntechnologie der modernen Biologie auf: der Massenspektrometrie, einer Technik, die Proteinfragmente wiegt und zählt. Standardverfahren sind bereits exzellent darin, uns zu sagen, wie viel von jedem Protein vorhanden ist, tun sich jedoch schwer damit, Veränderungen im Proteinstatus zu zeigen, etwa das Andocken an DNA oder das Einlagern in dichte Assemblies. Hier verfeinern die Forscher eine Variante der Massenspektrometrie, die als Narrow‑Window Data‑Independent Acquisition (nDIA‑MS) bezeichnet wird. Durch Zugabe kleiner chemischer Helfer, sogenannter Supercharging‑Reagenzien, in das Lösungsmittel, das Peptide durch das Instrument transportiert, erhöhen sie die elektrischen Ladungen dieser Fragmente und verstärken das Signal deutlich.
Nach dem Testen zweier gängiger Supercharging‑Zusätze, Dimethylsulfoxid (DMSO) und m‑Nitrobenzylalkohol (mNBA), finden sie, dass 3 % DMSO die größte Gesamtsignalsteigerung und die höchste Anzahl detektierter Proteine liefert, während mNBA besser darin ist, die Zahl und Ladung einzelner Peptidfragmente zu erhöhen. Mit dem optimierten Setup kann das Team in einem 15‑minütigen Lauf etwa 9.600 menschliche Proteine aus nur einem Mikrogramm eines Standard‑Zelldigests identifizieren – eine bemerkenswerte Kombination aus Geschwindigkeit und Tiefe für Routineexperimente. Diese Leistungsfähigkeit ebnet den Weg dafür, nDIA‑MS nicht nur zum Zählen von Proteinen zu nutzen, sondern auch, um zu untersuchen, wie sich ihr physikalischer Zustand unter Stress verändert.
Löslichkeit als Messgröße für zelluläre Veränderungen
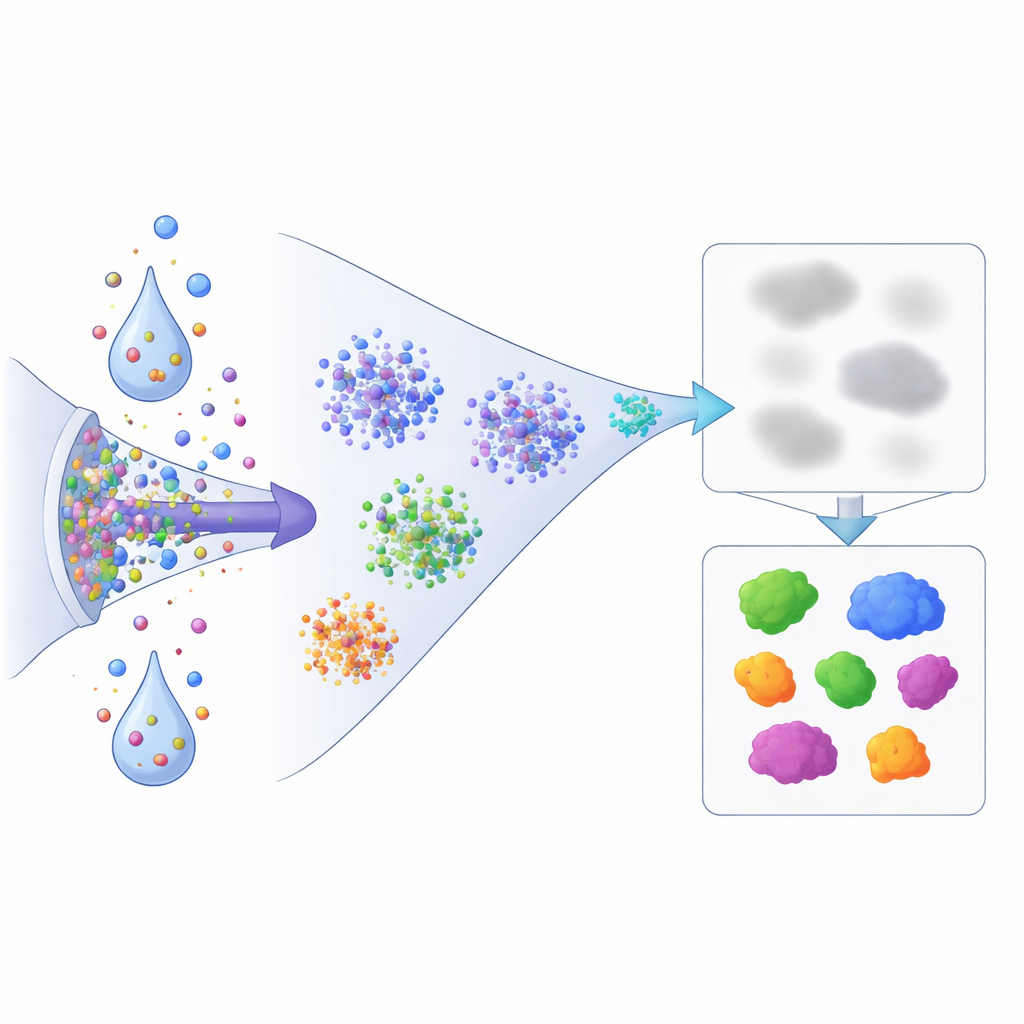
Um Löslichkeit in ein messbares Signal zu verwandeln, behandeln die Forscher Zellen schonend mit einem milden Detergens, das frei lösliche Proteine extrahiert und das Material zurücklässt, das fest an DNA, Membranen oder andere Strukturen gebunden ist. Sie analysieren sowohl das Gesamtzelllysat als auch dieses „unlösliche“ Pellet aus drei Krebszelllinien mit der optimierten nDIA‑MS‑Methode. Durch den Vergleich der Häufigkeit jedes Proteins im Pellet relativ zur Gesamtzellprobe berechnen sie ein einfaches „Unlöslichkeitsverhältnis“ – höhere Werte deuten auf stärkere Assoziation mit zellulären Strukturen hin, niedrigere Werte auf einen löslicheren, freieren Zustand.
Das Team setzt die Zellen anschließend nur für eine Stunde zwei Wirkstoffen aus: MG132, einem Proteasom‑Blocker, der verhindert, dass Zellen unerwünschte Proteine abbauen, und ML‑792, einem Inhibitor der SUMO‑Aktivierung, der ein wichtiges Protein‑Markierungssystem stört. Diese kurze Exposition ist bewusst gewählt; sie soll rasche, frühe Verschiebungen im Proteinverhalten erfassen, bevor sich Veränderungen in der Genexpression vollständig entfalten. Selbst in diesem kurzen Zeitfenster können sie Löslichkeits‑ und Mengenänderungen für 8.694 Proteine quantifizieren und bestätigen, dass ihre Fraktionierung klassische lösliche Proteine, wie Tubulin, klar von chromatingebundenen Proteinen, wie Histonen, trennt.
Wirkstoffe, die die Proteinlandschaft der Zelle umgestalten
MG132 und ML‑792 bewirken weitreichende, aber unterschiedliche Umgestaltungen der Proteomlöslichkeit. MG132 macht in den drei Zelllinien über tausend Proteine unlöslicher und mehr als sechshundert löslicher. Viele betroffene Proteine befinden sich an Schnittstellen der Qualitätskontrolle von Proteinen, der DNA‑Schadensantwort, der Genregulation und der Autophagie – des zellulären Reinigungsmechanismus. Beispielsweise werden Komponenten des Proteasom‑Aktivator‑Komplexes und Adapter, die fehlerhafte Proteine markieren, weniger löslich, was darauf hindeutet, dass bei Blockade des Abbaus zentrale Qualitätskontrollfaktoren selbst an Strukturen wie Chromatin oder Zellmembranen gebunden werden. Autophagie‑Proteine und Akteure der Schadenantwort, einschließlich des Stressregulators HSF1, verschieben sich ebenfalls in unlöslichere, kondensatähnliche Zustände, konsistent mit der Bildung nukleärer Stresskörper.
ML‑792 trifft dagegen stark Proteine, die an der Transkription und am SUMO‑System selbst beteiligt sind. Hunderte Proteine werden entweder unlöslicher oder löslicher, wenn die SUMO‑Aktivierung blockiert ist, und Kern‑SUMO‑Proteine verlagern sich wie erwartet in den löslichen Anteil. Die Studie hebt auffällige Verhaltensweisen hervor: Untereinheiten der RNA‑Polymerase III werden unlöslicher, was auf veränderten nukleären Import oder Chromatinbindung hindeutet; Schlüsselrepressoren, die mit nukleären Kompartimenten assoziiert sind, wie SP100 und DAXX, werden löslicher, was darauf schließen lässt, dass SUMO‑Markierungen helfen, sie in diesen Kompartimenten zu sequestrieren. Wenn beide Wirkstoffe einzeln oder nacheinander angewendet werden, zeigen einige Proteine, darunter NAB2, SMAD2 und RB1, koordinierte oder sogar entgegengesetzte Löslichkeitsverschiebungen, was ein feingliedriges Zusammenspiel zwischen dem Ubiquitin‑ und dem SUMO‑Markierungssystem bei der Kontrolle der Proteinlokalisation offenbart.
Was das für die zukünftige Medikamentenentwicklung bedeutet
Für Nicht‑Spezialisten ist die zentrale Botschaft: Proteine ändern sich bei Stress oder Wirkstoffbehandlung nicht nur in ihrer Menge; sie bewegen sich, kondensieren und verändern, wie stark sie an zelluläre Strukturen gebunden sind. Diese Arbeit liefert eine proteomweite, sehr schnelle Methode, um diese Verschiebungen zu beobachten. Durch die Kombination eines abgestimmten Massenspektrometrie‑Workflows mit einem einfachen Vergleich löslich versus unlöslich zeigen die Autoren, dass gängige experimentelle Wirkstoffe das interne Proteinbild der Zelle rasch umorganisieren – auf Weisen, die mit standardmäßigen Mengenmessungen übersehen würden. Der Ansatz eröffnet die Möglichkeit, nachzuvollziehen, wie Wirkstoffkandidaten Proteinzustände in der gesamten Zelle umgestalten, und hilft Forschern, unerwartete Ziele, Stresswege und Versagenspunkte zu entdecken, die für das Verständnis von Wirksamkeit und Nebenwirkungen entscheidend sein könnten.
Zitation: Xiong, Y., Zhang, H., Tan, L. et al. Supercharging-enhanced nDIA-MS enables global profiling of drug-induced proteome solubility shifts. Nat Commun 17, 2350 (2026). https://doi.org/10.1038/s41467-026-69025-8
Schlüsselwörter: Proteomlöslichkeit, Massenspektrometrie, Proteasom-Inhibitor MG132, SUMOylierungs-Inhibitor ML-792, Protein‑Zustandsübergänge