Clear Sky Science · de
Gezielt gestaltete Innenarchitektur von Kern‑Schale-Lipidnanopartikeln fördert effiziente mRNA‑Freisetzung aus Endosomen
Warum dieser neue Liefertrick wichtig ist
Viele der spannendsten neuen Medikamente, von COVID‑19‑Vakzinen bis zu experimentellen Krebsbehandlungen, basieren auf Boten‑RNA, kurz mRNA. Ein hartnäckiges Problem bleibt jedoch: Sobald diese fragilen Stränge in unsere Zellen gelangen, bleiben die meisten in kleinen inneren Bläschen, den Endosomen, gefangen und werden zerstört. Diese Studie stellt ein kluges Neudesign der winzigen Fettbläschen vor, die mRNA transportieren—sogenannte Lipidnanopartikel. Indem die Forschenden ihre innere Struktur um einen festen Goldkern herum neu anordnen, verbessern sie dramatisch, wie viel mRNA in den Arbeitsbereich der Zelle entkommt, wo sie tatsächlich nützliche Proteine herstellen kann.
Winzige Kuriere mit besserem Bauplan
Gängige mRNA‑Vakzine und Therapien beruhen meist auf weichen, klumpigen Partikeln aus einer Mischung von Lipiden, die die mRNA umhüllen. Theoretisch sollten sich spezielle „ionisierbare“ Lipide in diesen Partikeln im sauren Inneren der Endosomen positiv aufladen und die Endosomenmembran aufreißen, wodurch die mRNA freikommt. In der Praxis hebt die negative Ladung der mRNA einen Großteil dieses Effekts auf, sodass nur rund 2 Prozent der gelieferten mRNA tatsächlich die Proteinproduktionsmaschinerie der Zelle erreichen. Die Autorinnen und Autoren stellten eine einfache, aber wirkungsvolle Frage: Anstatt nur die Chemie der Lipide zu verändern—was wäre, wenn man die innere Architektur des Partikels so neu entwirft, dass man kontrollieren kann, wo mRNA und Lipide zueinander positioniert sind?
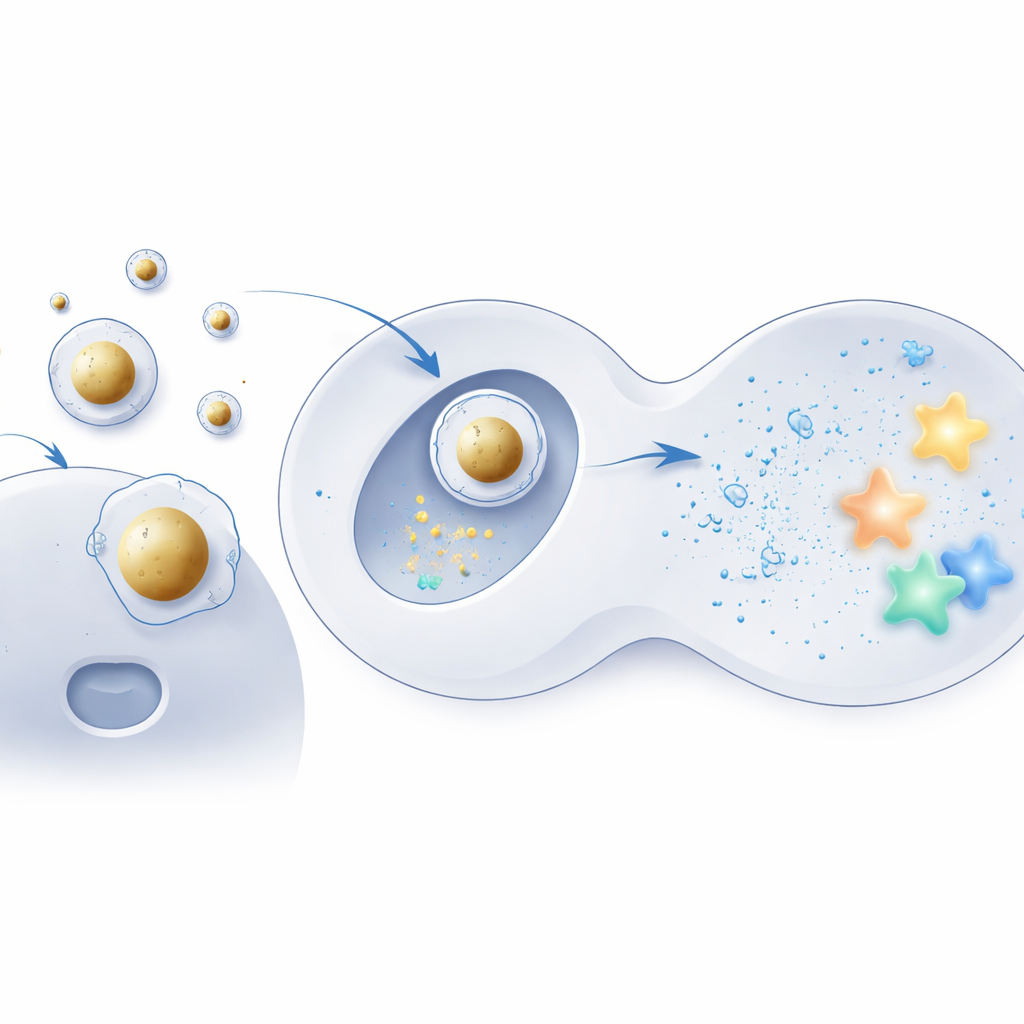
Aufbau einer goldzentrierten Lieferhülle
Um diese Idee zu testen, nutzte das Team winzige Goldkugeln als starre Kerne und beschichtete sie mit denselben ionisierbaren Lipiden, die in konventionellen Formulierungen verwendet werden. Die negativ geladene mRNA wurde zunächst auf diesen Kernen kondensiert, und erst danach wurde die Assemblierung in einer vertrauten Mischung aus Hilfslipiden und stabilisierenden Molekülen umhüllt—es entstand eine geordnete Kern‑Schale‑Struktur. Elektronenmikroskopie und Computersimulationen zeigten, dass diese „Au‑LNPs“ sehr homogen, thermodynamisch stabil und in wässrigen, körperähnlichen Bedingungen formstabil waren. Wichtig ist, dass ihre Gesamtlipidzusammensetzung der standardmäßiger Partikel entsprach—die innere Struktur, nicht die Zutaten, war also die entscheidende Änderung.
Wie ein umgebautes Inneres das Entweichen fördert
Im leicht sauren Endosomenmilieu wird der goldbasierte Kern stark positiv geladen, zieht die negativ geladene mRNA nach innen und drängt die positiv geladenen ionisierbaren Lipide nach außen zur umliegenden Membran. Diese ladungsgetriebene Segregation konzentriert die membran‑störenden Lipide genau dort, wo sie gebraucht werden. In Modellmembran‑Tests und in roten Blutkörperchen waren die neuen Partikel wirksamer dabei, Membranen bei niedrigem pH zu durchstoßen, während sie bei neutralem pH inaktiv blieben—ein erwünschtes Sicherheitsmerkmal. In lebenden Zellen zeigte die Bildgebung fluoreszenzmarkierter mRNA etwa einen zweifachen Anstieg des endosomalen Entweichens und eine erstaunliche rund 100‑fache Zunahme der mRNA‑Verbreitung im Zytoplasma im Vergleich zu konventionellen Partikeln.
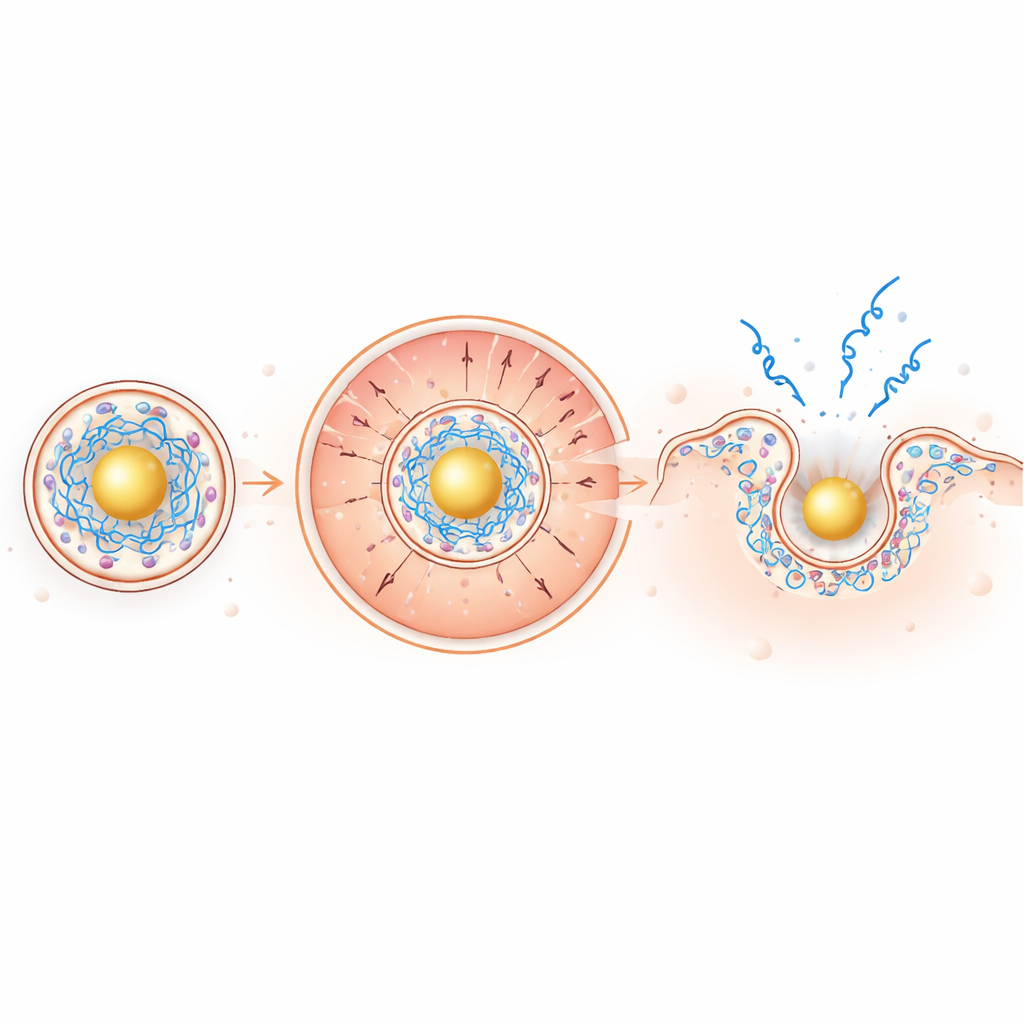
Aus der Schale in die Maus: stärkere Signale und besserer Schutz
Diese physikalischen Vorteile führten zu realen biologischen Gewinnen. In mehreren Zelltypen erzeugten die Goldkern‑Partikel deutlich höhere Mengen an Reporterprotein als Standardformulierungen, besonders bei niedrigen Dosen. Bei Mäusen steigerten sie die mRNA‑gesteuerte Proteinausbeute nach Injektionen in Muskel oder Venen um das Fünf‑ bis Siebenfache, ohne das Verteilungsmuster im Körper wesentlich zu ändern. Beim Einsatz zur Lieferung einer SARS‑CoV‑2‑Spike‑mRNA‑Vakzine verdoppelten die neugestalteten Partikel ungefähr die Antikörperspiegel nach der ersten Impfdosis und erhöhten sie weiter nach einer Auffrischung, dabei produzierten sie zudem stärkere virusneutralisierende Antikörper. In einem anspruchsvollen Modell des dreifach negativen Mammakarzinoms schrumpften durch die neuen Partikel vermittelte mRNA‑Krebsvakzine Tumoren effektiver, senkten Tumoraktivitätssignale und verlängerten bemerkenswert das Überleben.
Sicherheit und ein Weg zu künftigen Arzneimitteln
Trotz des Einsatzes von Gold in ihrem Kern erschienen die Partikel bei Mäusen gut verträglich. Körpergewichte, Entzündungsmarker und Gewebeuntersuchungen zeigten keine schwerwiegende Toxizität, und die Goldkonzentrationen in Organen sanken innerhalb von zwei Tagen wieder gegen den Ausgangswert. Die Autorinnen und Autoren betonen, dass Gold hauptsächlich als Proof‑of‑Concept‑Gerüst dient: Dasselbe interne Designprinzip ließe sich auf andere sichere oder biologisch abbaubare Materialien anwenden. Die zentrale Botschaft für Nicht‑Spezialistinnen und Nicht‑Spezialisten lautet, dass die Art und Weise, wie wir mRNA in ihrem winzigen Träger verpacken, genauso wichtig sein kann wie das, womit wir sie verpacken. Indem man Lipidnanopartikeln ein disziplinierteres Innenlayout verleiht, bietet diese Arbeit einen neuen Weg, einen langjährigen Flaschenhals der mRNA‑Lieferung zu überwinden—und damit wirksamere Vakzine und Therapien gegen Infektionskrankheiten, Krebs und darüber hinaus zu ermöglichen.
Zitation: Li, T., Zhang, J., Guo, J. et al. Engineered internal architecture of core-shell lipid nanoparticles promotes efficient mRNA endosomal release. Nat Commun 17, 2187 (2026). https://doi.org/10.1038/s41467-026-69017-8
Schlüsselwörter: mRNA‑Lieferung, Lipidnanopartikel, Endosomales Entweichen, Nanomedizin, RNA‑Vakzine