Clear Sky Science · de
FGF13 fungiert als Regulator der ERK/aeroben Glykolyse-Achse im entzündlichen Zustand bei septischem Lungenversagen
Warum diese Studie für Patienten mit schweren Infektionen wichtig ist
Sepsis ist eine lebensbedrohliche Komplikation einer Infektion, die innerhalb weniger Stunden zum Versagen der Lunge führen kann, Patienten an Beatmungsgeräte bindet und mit einem hohen Sterberisiko einhergeht. Diese Studie untersucht ein wenig bekanntes Protein in unseren Zellen, genannt FGF13, und zeigt, wie es die außer Kontrolle geratene Entzündung und den übermäßigen Energieverbrauch vorantreibt, die die Lunge bei Sepsis schwer schädigen. Indem die Arbeit diese verborgene Steuerungsstrecke nachzeichnet, weist sie auf neue Wirkstoffziele hin, mit denen sich der Sturm in der Lunge beruhigen lässt, ohne das gesamte Immunsystem lahmzulegen.
Ein versteckter Akteur bei Lungenverletzungen während der Sepsis
Die Forschenden begannen damit, Lungengewebe von septischen Mäusen und menschlichen Patienten mit Gewebe von nicht-septischen Kontrollen zu vergleichen. Sie untersuchten eine Familie von Molekülen, die als Fibroblasten-Wachstumsfaktoren bekannt sind und zur Erhaltung der Lungenfunktion beitragen. Unter ihnen stach FGF13 hervor: Seine Konzentration war in den Lungen septischer Patienten und Tiere deutlich erniedrigt. Bei der Lokalisation von FGF13 fanden sie es hauptsächlich in zwei wichtigen Zelltypen: Endothelzellen, die die Innenauskleidung von Blutgefäßen bilden, und Makrophagen, Immunzellen, die Entzündungen erkennen und verstärken. In septischen Lungen waren FGF13-positive Endothelzellen und Makrophagen stark reduziert, was darauf hindeutet, dass Veränderungen dieses Moleküls mit schweren Lungenverletzungen verknüpft sein könnten.
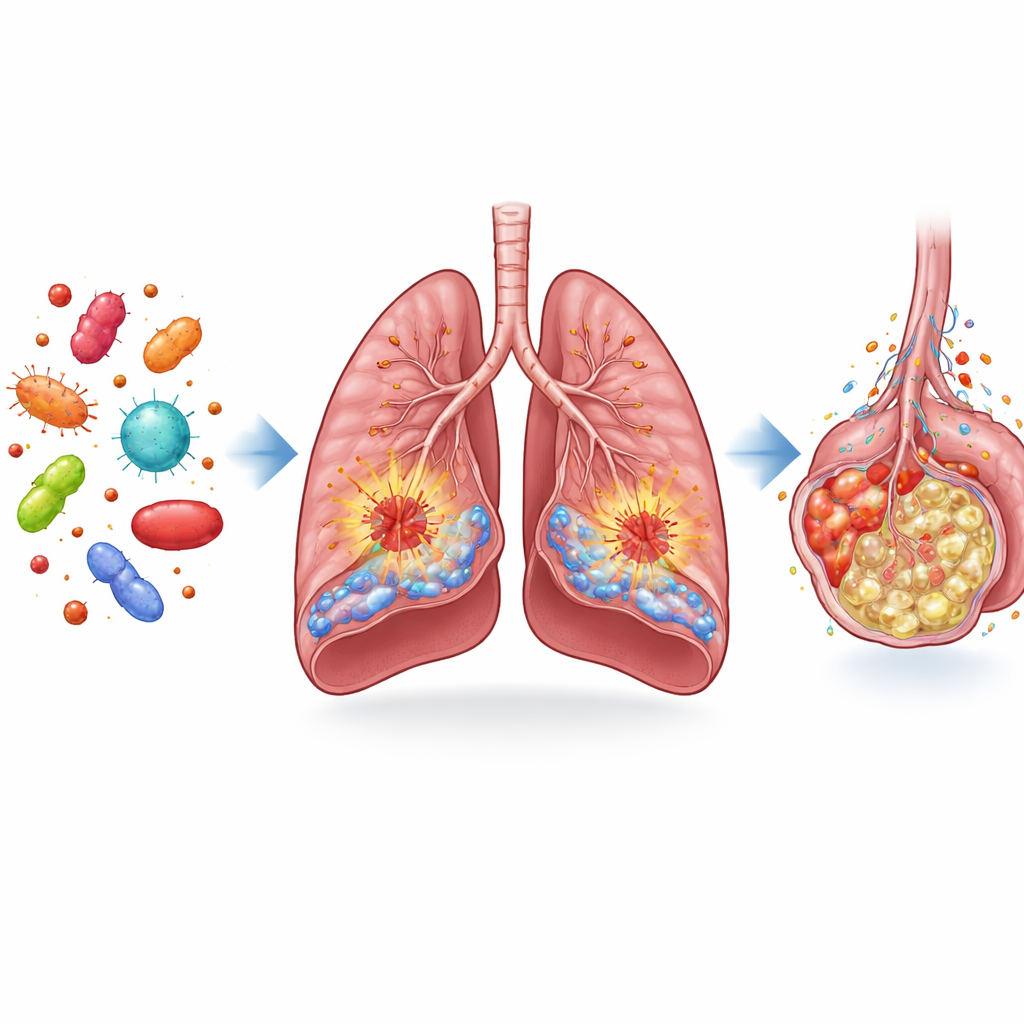
Wie FGF13 Lungenverteidiger in Treiber der Schädigung verwandelt
Um zu testen, was FGF13 tatsächlich bewirkt, setzten die Forschenden genetische Werkzeuge bei Mäusen ein, um es entweder in bestimmten Zellen zu entfernen oder diese Zellen zur vermehrten Produktion zu zwingen. Wurde FGF13 nur in Endothelzellen gelöscht, zeigten septische Mäuse weniger durchlässige, weniger geschwollene Lungen, weniger einwandernde Immunzellen und eine bessere Überlebensrate. Das Gegenteil trat ein, wenn Endothelzellen so verändert wurden, dass sie zu viel FGF13 produzierten: Lungenödem, Blutungen und Ansammlungen entzündlicher Zellen verschlechterten sich. Eine ähnliche Beobachtung ergab sich bei Makrophagen. Mäuse ohne FGF13 in diesen Immunzellen zeigten schwächere Entzündungsreaktionen und weniger Lungenverletzung, während Makrophagen mit übermäßiger FGF13 mehr entzündliche Moleküle freisetzten und den Schaden verschärften. In Zellkulturen führte eine Verringerung von FGF13 dazu, dass Gefäßzellen und Makrophagen weniger anhaftend, weniger entzündet und weniger toxisch für ihre Nachbarn waren.
Entzündete Zellen schalten auf zuckerhungrigen Stoffwechselmodus
Entzündete Zellen schalten, ähnlich wie Krebszellen, häufig ihre Energienutzung um: Statt langsam mit Sauerstoff zu verbrennen, bauen sie Zucker schnell ab in einem Prozess, der als aerobe Glykolyse bezeichnet wird und Milchsäure erzeugt. Die Autorinnen und Autoren fanden heraus, dass FGF13 diese Umschaltung stark fördert. In septischen Mäusen ohne FGF13 in Endothelzellen oder Makrophagen waren die Blutlaktatwerte niedriger. In Zellkulturen nahmen Zellen mit reduziertem FGF13 weniger Glukose auf und produzierten nach entzündlicher Stimulation weniger Laktat, während Zellen mit zusätzlichem FGF13 eine gesteigerte Glykolyse zeigten. Als die Forschenden die Glykolyse mit einem Medikament blockierten, wurde der entzündungsfördernde Effekt von überschüssigem FGF13 weitgehend abgeschwächt, wodurch die schädliche Rolle des Moleküls direkt mit diesem zuckerverbrennenden Programm verknüpft wurde.
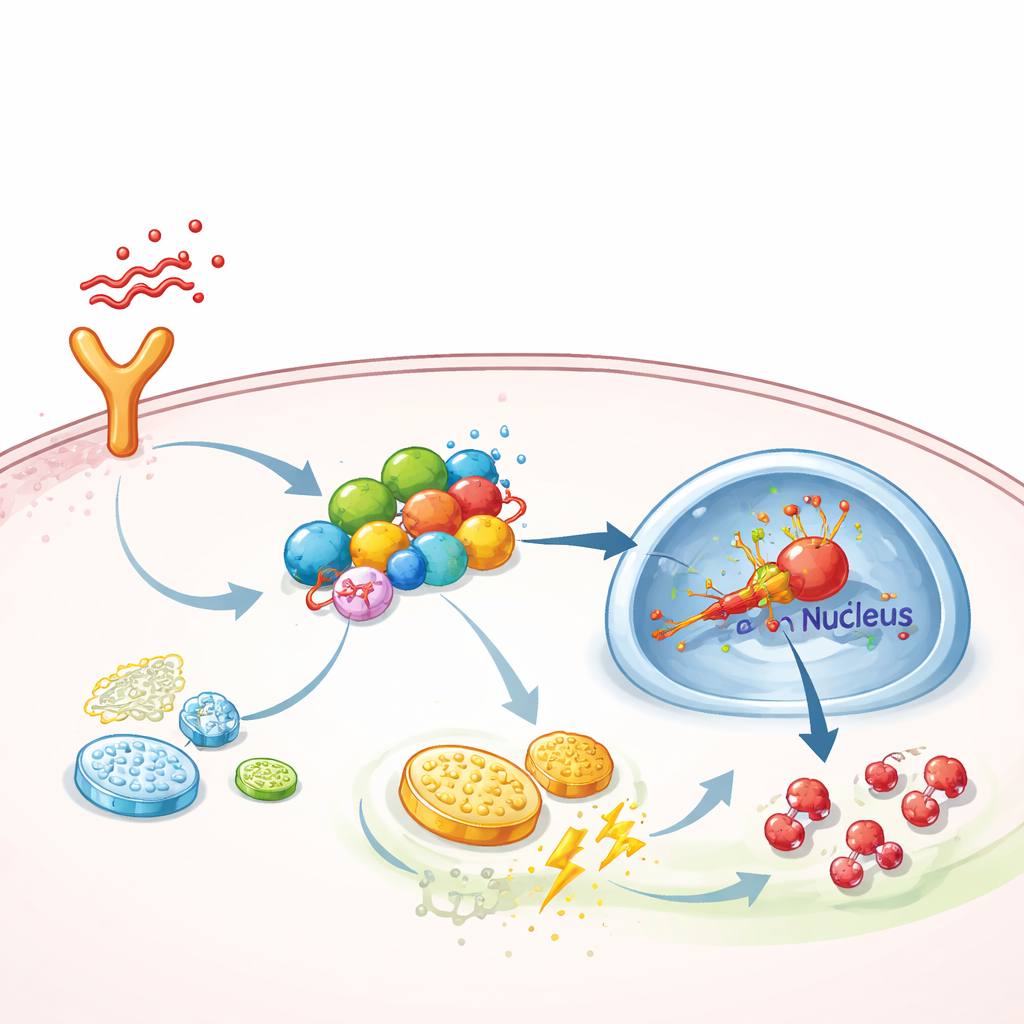
Ein molekulares Gerüst, das entzündliche Signalgebung verstärkt
Tiefergehend untersuchten die Forschenden, wie FGF13 Zellen in diesen hochgetakteten Stoffwechsel drängt. Sie entdeckten, dass FGF13 physisch an mehrere Signalproteine bindet, die eine Kette von Oberflächenrezeptoren bis in den Zellkern bilden — konkret den TAK1–MEK–ERK-Weg, der bekannt dafür ist, einen Hauptregulator der Reaktionen auf Sauerstoffmangel namens HIF-1α zu aktivieren. FGF13 wirkt wie ein Gerüst, das diese Komponenten zusammenhält, sodass Signale effizienter weitergeleitet werden. Bei reduziertem FGF13 gingen die Aktivierung von ERK und HIF-1α sowie die Glykolyse zurück; bei erhöhtem FGF13 wurde der Weg hyperaktiv. Die Überexpression von HIF-1α in Mäusen beseitigte den schützenden Effekt des FGF13-Entzugs, während ein selektiver ERK-Inhibitor, SCH772984, den durch FGF13-Überproduktion verursachten Schaden neutralisierte und den Lungenzustand bei septischen Tieren verbesserte.
Was das für künftige Sepsis-Therapien bedeutet
Für eine nichtwissenschaftliche Leserschaft ist die Hauptaussage: Septisches Lungenversagen ist nicht bloß zufällige Gewebezerstörung; es wird von einer spezifischen molekularen Schaltung in Gefäßzellen und Makrophagen angetrieben. FGF13 steht im Zentrum dieser Schaltung und hilft, ein Signalzentrum zusammenzubauen, das Zellen in einen zuckerfressenden, hochentzündlichen Zustand zwingt. Obwohl die FGF13-Spiegel während der Sepsis sinken — wahrscheinlich als Teil einer breiteren Stressantwort — zeigt diese Studie, dass das verbleibende Protein weiterhin ein starker Treiber von Schäden ist. Durch das Blockieren entweder der Signalpartner von FGF13 oder der von ihm geförderten glykolytischen Umschaltung könnte es möglich sein, Lungenödem, Durchlässigkeit und Entzündung zu verringern, ohne die Fähigkeit des Körpers zur Bekämpfung von Infektionen zu lähmen. Diese Arbeit hebt daher FGF13 und die ERK–HIF‑1α–Glykolyse-Achse als vielversprechende Ansätze für die Entwicklung präziserer, sichererer Behandlungen bei sepsisbedingtem Lungenversagen hervor.
Zitation: Zhu, J., Wang, J., Jiang, C. et al. FGF 13 functions as a regulator of the ERK/aerobic glycolysis axis in the inflammatory state during septic lung injury. Nat Commun 17, 2383 (2026). https://doi.org/10.1038/s41467-026-69014-x
Schlüsselwörter: septisches Lungenversagen, FGF13, endotheliale Entzündung, aerobe Glykolyse, ERK-Signalgebung