Clear Sky Science · de
Kombinierte zielgerichtete und epigenetische Therapie verstärkt die Antitumor-Immunität durch Stabilisierung der GATA6‑abhängigen MHCI‑Expression beim duktalen Adenokarzinom der Bauchspeicheldrüse
Warum diese Forschung für Pankreaskrebs wichtig ist
Das duktale Adenokarzinom der Bauchspeicheldrüse zählt zu den tödlichsten Krebsarten, nicht zuletzt weil es sich dem Immunsystem entzieht und gegen die meisten Therapien resistent ist. Diese Studie enthüllt einen spezifischen Tumorzellzustand, der von einem Gen namens GATA6 gesteuert wird und Pankreaskarzinomzellen für Immunangriffe besser sichtbar macht. Die Autor*innen zeigen außerdem, wie die Kombination zweier Wirkstoffklassen diesen verwundbaren Zustand bewahrt und in experimentellen Modellen die Fähigkeit zytotoxischer T‑Zellen erhöht, Tumoren anzugreifen.
Ein Tumorzellzustand, der das Immunsystem einlädt
Nicht alle Pankreaskarzinomzellen verhalten sich gleich. Einige behalten eine geordnete, epitheliale Identität, während andere in einen beweglicheren, aggressiveren mesenchymalen Zustand übergehen. Der Transkriptionsfaktor GATA6 trägt zur Aufrechterhaltung der epithelialen Identität bei und ist mit besseren Patientenverläufen assoziiert. In großen Patientenkohorten enthielten Tumoren mit hohem GATA6‑Spiegel mehr Immunzellen, darunter CD8‑„Killer“‑T‑Zellen, als Tumoren mit wenig oder keinem GATA6. Mit Hilfe fortschrittlicher räumlicher Bildgebung an humanen Tumorproben fanden die Forschenden, dass GATA6‑positive Krebszellen häufiger neben CD8‑T‑Zellen lagen und höhere Mengen des Moleküls MHCI zeigten, das wie eine Flagge wirkt und T‑Zellen anzeigt, was sich in der Zelle befindet. Diese Beobachtungen legen nahe, dass GATA6 eine Tumorzellpopulation kennzeichnet, die natürlicherweise besser für das Immunsystem sichtbar ist. 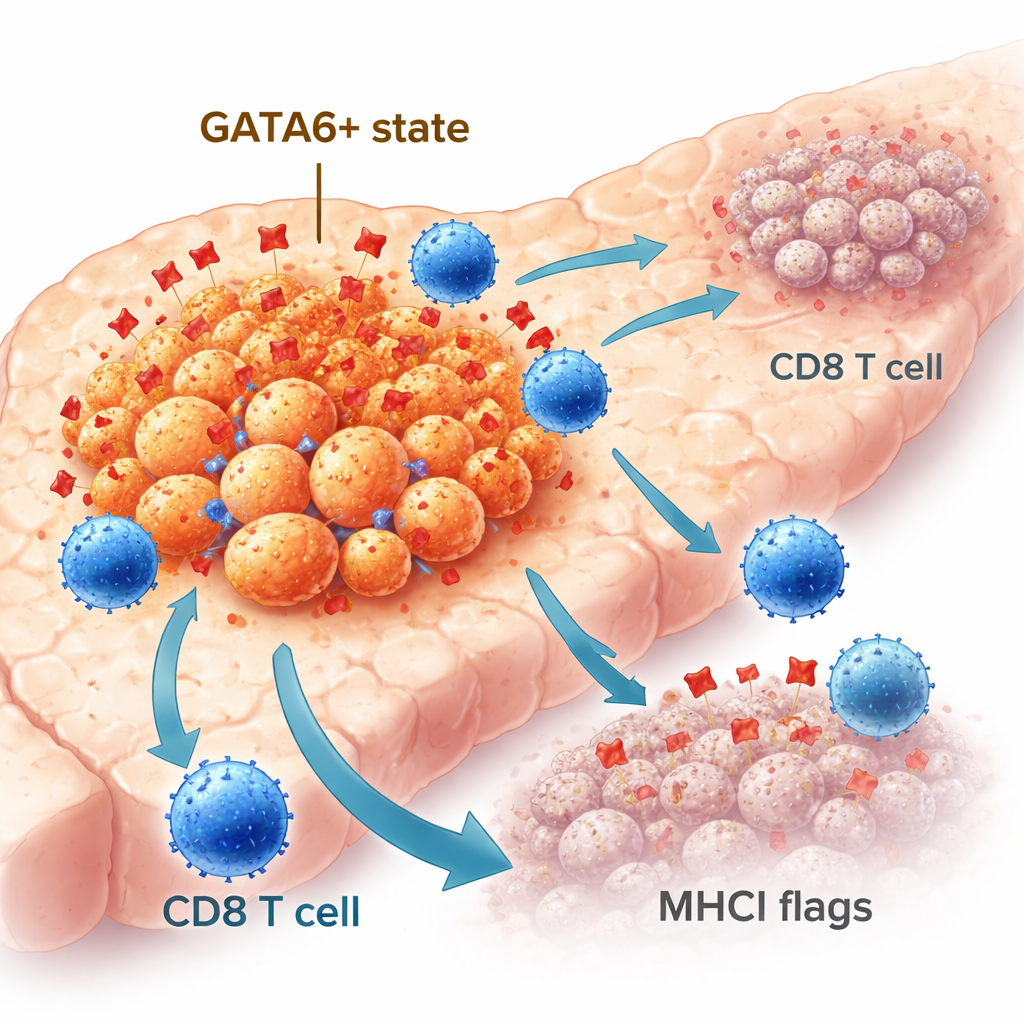
Zielgerichtete Therapie, die Tumorsichtbarkeit erhöht – aber mit einem Preis
Das Team untersuchte anschließend, ob zielgerichtete Medikamente diese Sichtbarkeit weiter steigern können. Sie konzentrierten sich auf MEK‑Inhibitoren, eine Wirkstoffklasse, die einen Wachstums‑Signalweg blockiert, der bei Pankreaskrebs häufig aktiv ist. In Maus‑Pankreaskrebszelllinien sowie in Tumoren in Mäusen und in patientenabgeleiteten Xenotransplantaten erhöhte die MEK‑Hemmung die MHCI‑Präsenz auf der Oberfläche von GATA6‑hohen Tumorzellen und machte sie dadurch potenziell bessere Ziele für T‑Zellen. Bei in Mäusen behandelten GATA6‑reichen Tumoren verlangsamte sich das Tumorwachstum, MHCI stieg an und mehr CD8‑T‑Zellen mit zytotoxischen Molekülen infiltrierten die Tumoren. Die direkte Blockade von GATA6, entweder durch Gen‑Knockout oder durch rasche Abbau des Proteins, hob diesen durch MEK‑Inhibitoren induzierten Anstieg von MHCI und die damit verbundene Tumorkontrolle auf, was zeigt, dass GATA6 für diesen vorteilhaften Effekt unerlässlich ist.
Wie Tumoren sich anpassen: Übergang in einen schwerer zu zerstörenden Zustand
Die Geschichte enthält jedoch eine Wendung. Eine längerfristige Behandlung mit MEK‑Inhibitoren trieb viele Tumorzellen dazu, vom GATA6‑positiven epithelialen Zustand in einen mesenchymalen, GATA6‑armen Zustand überzugehen, der mit Therapieresistenz verbunden ist. Sowohl in Mausmodellen als auch in patientenabgeleiteten Xenotransplantaten zeigten MEK‑Inhibitor‑behandelte Tumoren schließlich weniger GATA6‑positive Zellen, verstärkte Marker des epithelial‑zu‑mesenchymalen Übergangs und insgesamt geringeren anhaltenden Nutzen. Obwohl einzelne GATA6‑positive Zellen weiterhin MHCI als Reaktion auf das Medikament hochregulierten, begrenzte die schrumpfende Größe dieser Population die Gesamtverbesserung der Tumorantigen‑Präsentation und hilft zu erklären, warum MEK‑Inhibitoren allein in klinischen Studien beim Pankreaskrebs enttäuscht haben.
Epigenetische Wirkstoffe, die Tumoren im verwundbaren Zustand halten
Um dieser adaptiven Flucht entgegenzuwirken, wandten sich die Forschenden Histon‑Deacetylase‑Inhibitoren (HDAC‑Inhibitoren) zu, einer Klasse epigenetischer Wirkstoffe, die Zellidentität und Immun‑Sichtbarkeit beeinflussen können. In Zellkulturen und Mausmodellen stellte die Kombination aus MEK‑Inhibitoren und Klasse‑I‑HDAC‑Inhibitoren wie Domatinostat die durch MEK‑Hemmung unterdrückte GATA6‑Expression wieder her, kehrte Zeichen des epithelial‑zu‑mesenchymalen Übergangs um und steigerte die MHCI‑Spiegel auf Tumorzellen weiter. Wichtig war, dass diese Kombinationsbehandlung zu stärkerer Infiltration und Aktivierung von CD8‑T‑Zellen sowie zu vermehrtem Tumorzellsterben in orthotopen Maustumoren und in einem gentechnisch veränderten Mausmodell führte, das den menschlichen Pankreaskrebs gut nachbildet. Die Depletion von CD8‑T‑Zellen beseitigte einen Großteil des Nutzens, was bestätigt, dass die Kombination vor allem dadurch wirkt, dass sie die Killer‑T‑Zellen stärkt.
Auf dem Weg zu klügeren Kombinationstherapien für eine schwere Krebsform
Ausgehend von diesen Befunden schlägt die Studie eine Strategie vor, bei der gezielte MEK‑Hemmung und epigenetische HDAC‑Hemmung gemeinsam eingesetzt werden, um einen GATA6‑gesteuerten Tumorzellzustand zu stabilisieren, der reich an MHCI ist und damit für das Immunsystem besonders leicht erkennbar. Indem sowohl die Zahl GATA6‑positiver Zellen erhöht als auch ihre MHCI‑„Flaggen“ verstärkt werden, fördert die Kombination eine tiefere CD8‑T‑Zell‑Infiltration, stärkere zytotoxische Aktivität und längeres Überleben in aggressiven Mausmodellen des Pankreaskrebses. Obwohl HDAC‑Inhibitoren erhebliche Nebenwirkungen haben können und die Arbeit präklinisch ist, weist diese Forschung auf zukünftige Behandlungsansätze hin, die weg‑/signalweggerichtete Wirkstoffe mit sorgfältig ausgewählten epigenetischen Modulatoren kombinieren könnten, um Pankreastumoren anfälliger für die körpereigenen Immunabwehr zu machen. 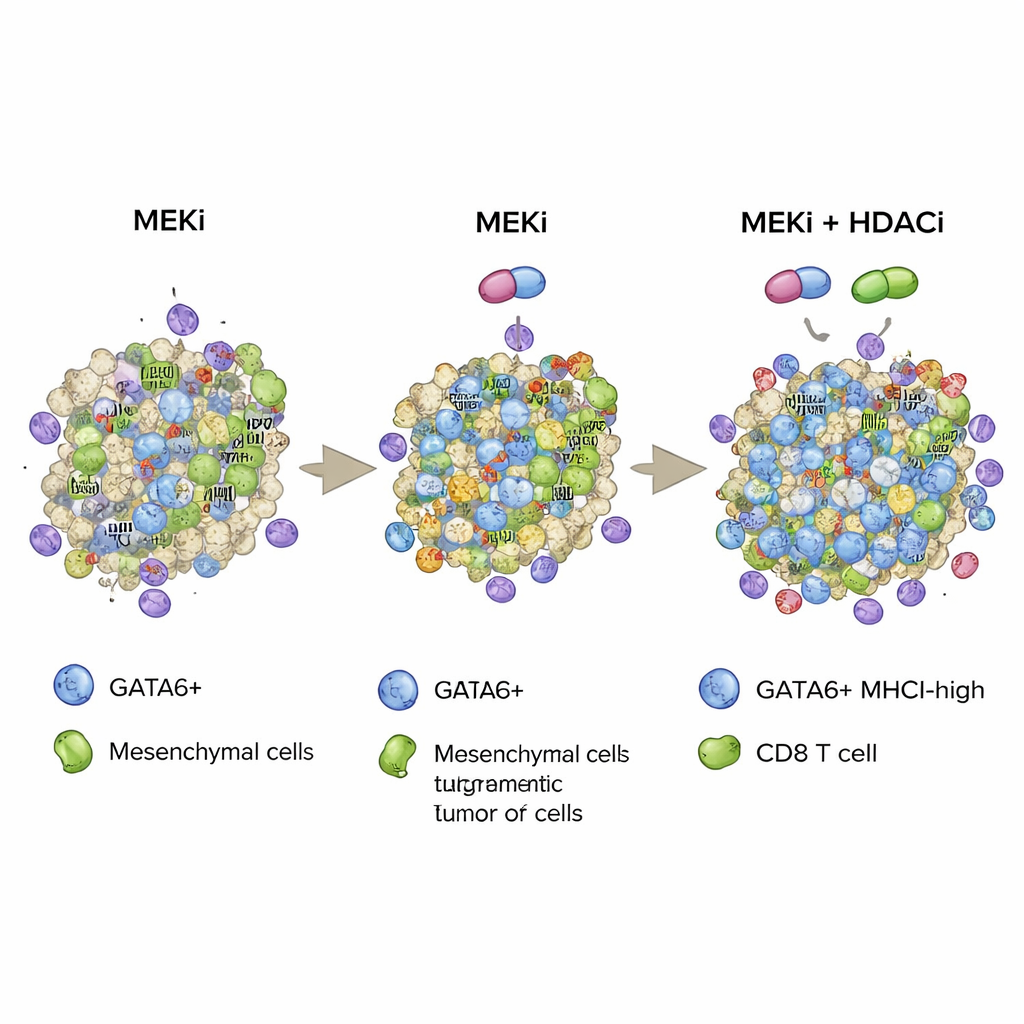
Zitation: Peng, J., Yang, J., Antonopoulou, G. et al. Combined targeted and epigenetic-based therapy enhances antitumor immunity by stabilizing GATA6-dependent MHCI expression in pancreatic ductal adenocarcinoma. Nat Commun 17, 1476 (2026). https://doi.org/10.1038/s41467-026-69013-y
Schlüsselwörter: Pankreaskrebs, Tumorimmunität, GATA6, MEK‑Inhibitor, HDAC‑Inhibitor