Clear Sky Science · de
Multikomponentige synergistische Immobilisierung durch in-situ- und dynamische Austauschstrategien zur Konstruktion hierarchischer Biopharmazeutika
Warum es wichtig ist, klügere Arzneimittel zu entwickeln
Viele der derzeit wirkungsvollsten Medikamente sind große, empfindliche Biomoleküle wie Proteine und Enzyme. Sie können Krebs bekämpfen, schädliche Bakterien töten und die Heilung beschleunigen, sind aber leicht beschädigt und schwer gezielt im Körper abzuliefern. Diese Arbeit beschreibt eine neue Methode, mehrere dieser empfindlichen Bausteine zusammen in einem schützenden, schwammartigen Material unterzubringen, damit sie nacheinander wirkungsvoller und mit weniger Nebenwirkungen arbeiten können.
Aus einem Kristall wird eine molekulare Wohnanlage
Die Forschenden beginnen mit einem speziellen porösen Material aus Metallionen und kleinen organischen Bausteinen. Es verhält sich ein wenig wie ein winziges, flexibles Wohnhaus voller Zimmer und Flure. Sie zeigen, dass dieses Gerüst, ein so genanntes zeolitisches Pyrimidingerüst, um Proteine herum wachsen kann, sodass die Proteine geschützt im Inneren des Kristalls landen. Dieses „in-situ“-Einschließen zerquetscht oder deaktiviert die Proteine nicht, und sorgfältige Abbildungen bestätigen, dass sie gleichmäßig im Inneren verteilt sind – ähnlich wie Mieter auf allen Etagen eines Hauses.
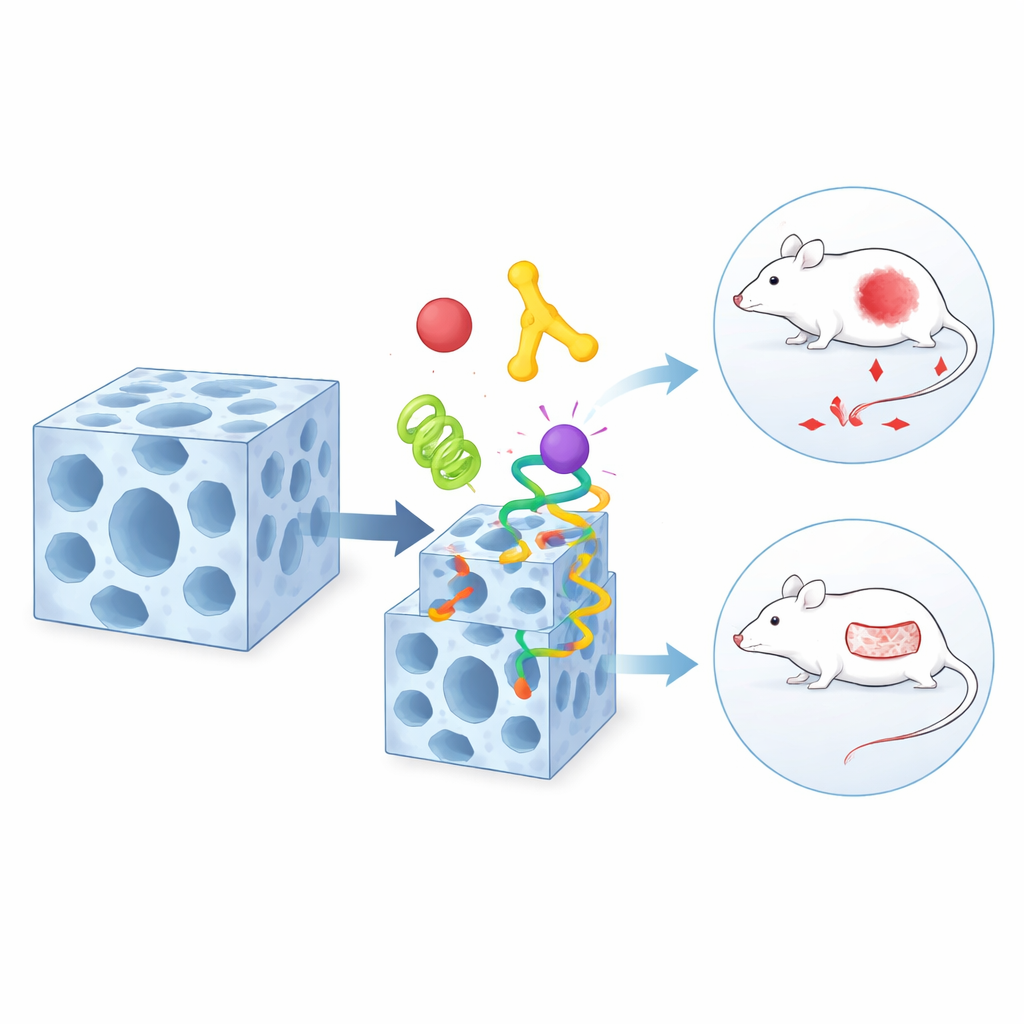
Ein formwandelnder Wirt zur Oberflächendekoration
Dasselbe Material hat einen überraschenden zweiten Trick: Es kann seine innere Struktur reversibel verändern, wenn es bestimmten Lösungsmitteln oder Wasser ausgesetzt wird. Während dieser schonenden Formänderung lockern sich einige chemische Verbindungen im Gerüst und bilden sich anschließend wieder. Das Team entdeckte, dass bestimmte chemische Gruppen auf Proteinoberflächen – wie sie in bestimmten Aminosäuren vorkommen – diesen Moment der Schwäche ausnutzen können. Sie konkurrieren vorübergehend mit den ursprünglichen Bausteinen des Gerüsts und schlüpfen in neu entstandene „Defekte“ in der Nähe der Oberfläche. Infolgedessen verankert sich eine Schicht von Proteinen vorwiegend an der Außenseite des Kristalls, während die inneren Proteine an ihrem Platz bleiben. Dieser dynamische Austauschprozess erlaubt es den Wissenschaftlern zu bestimmen, welche Komponenten tief innen wohnen und welche die äußere Hülle schmücken.
Entwurf von Enzym-Fertigungsstraßen
Mit Kontrolle über Innen- und Außenraum bauen die Autor*innen winzige enzymatische „Fertigungsstraßen“. In einem Beispiel ist ein Enzym, das Zucker in ein aggressives Zwischenprodukt umwandelt, im Gerüst eingeschlossen, während ein zweites Enzym, das dieses Zwischenprodukt sicher abbaut, nahe der Oberfläche fixiert ist. Diese Innen‑Außen-Anordnung lässt die Reaktion schneller und effizienter ablaufen als traditionellere Kern‑Schale-Designs oder zufällige Enzymmischungen. Da die äußeren Enzyme für Moleküle leichter zugänglich sind und das schädliche Zwischenprodukt schnell entfernt wird, bleibt das System über viele Zyklen aktiv und toleranter gegenüber Hitze, rauen Bedingungen und wiederholter Nutzung.
Intelligente Anti-Krebs- und Anti-Bakterien-Pakete
Die wahre Stärke dieses Ansatzes zeigt sich in der medizinischen Anwendung. Das Team kombiniert ein tumorzielendes Protein, ein zuckerverzehrendes Enzym und ein übliches Chemotherapeutikum in einem einzigen, geschichteten Partikel. Die auf der Oberfläche sitzende Zielkomponente lenkt das Partikel zu Krebszellen, das Enzym entzieht ihnen durch Verbrauch des lokalen Zuckers die Energie, und das kleine Molekül‑Medikament setzt einen zusätzlichen tödlichen Schlag. Bei Mäusen mit humanen Tumorimplantaten schrumpft dieses Dreifachpaket Tumore deutlich effektiver als jede der Komponenten allein oder einfacher angeordnete Mischungen. In einem separaten Design passen die Autor*innen das Gerüst für infizierte Hautwunden an, indem sie ein antibakterielles Peptid und ein gewebeumbauendes Enzym in unterschiedlichen Bereichen desselben Trägers platzieren. In Rattenmodellen reduzieren diese Partikel die Infektion deutlich und beschleunigen das Verschließen schwieriger Wunden im Vergleich zu konventionellen Behandlungen.

Wie diese Arbeit die Medizin voranbringt
Für Nicht‑Spezialistinnen und -Spezialisten lautet die Kernbotschaft, dass diese Studie einen einzelnen porösen Kristall in ein programmierbares Zuhause für viele Arten therapeutischer Moleküle verwandelt. Indem die Forschenden entscheiden, wer im Inneren lebt, wer sich auf der Oberfläche befindet und in welchem Verhältnis, können sie schrittweise Behandlungen orchestrieren – zuerst Zielsteuerung, dann Angriff, dann Reparatur – innerhalb eines winzigen Objekts. Diese Strategie schützt nicht nur fragile biologische Medikamente, sondern ermöglicht es ihnen auch, sich gegenseitig zu unterstützen, was zu stärkeren, präziseren Anti‑Krebs‑ und Anti‑Bakterien‑Therapien führt. Dieselben Gestaltungsprinzipien könnten an viele künftige „intelligente Arzneimittel“ angepasst werden, die mehrere Komponenten brauchen, um zur richtigen Zeit am richtigen Ort zusammenzuarbeiten.
Zitation: Yang, M., Meng, X., Shi, R. et al. Multicomponent synergistic immobilization via in-situ and dynamic exchange strategies for constructing hierarchical biopharmaceuticals. Nat Commun 17, 2208 (2026). https://doi.org/10.1038/s41467-026-69009-8
Schlüsselwörter: metall-organische Gerüste, Enzymimmobilisierung, Krebs-Nanomedizin, Wundheilung, Lieferung von Biopharmazeutika