Clear Sky Science · de
Die extrazelluläre Matrix vermittelt die Clusterbildung zirkulierender Tumorzellen bei Metastasen von triple-negativem Brustkrebs
Wie sich verräterische Brustkrebszellen im Blut zusammenschließen
Wenn Brustkrebs streut, liegt das oft daran, dass einzelne Krebszellen in den Blutkreislauf entweichen und in entfernten Organen Tumoren bilden. Diese Studie stellt eine auf den ersten Blick einfache, aber folgenreiche Frage: Wie schaffen es die aggressivsten Brustkrebszellen, die ihre üblichen „Klett“-Verbindungen verloren haben, dennoch als eng verbundene Cluster zu reisen — und warum macht das sie so tödlich?
Ein klebriger Zuckermantel als Ersatz für den klassischen Zellkleber
Die Autorinnen und Autoren konzentrieren sich auf den triple-negativen Brustkrebs (TNBC), eine besonders aggressive Form, die häufig zirkulierende Tumorzellen (CTCs) ins Blut abgibt. In vielen Krebsarten sind CTC-Cluster weitaus metastasenbildender als einzelne Zellen. Typischerweise werden solche Cluster durch epitheliale Adherens-Junctions zusammengehalten — spezielle Proteinkomplexe, die wie molekulare Nieten zwischen benachbarten Zellen wirken. TNBC-Zellen verlieren jedoch häufig diese Junction-Proteine, was ein Paradox erzeugt: Ohne den üblichen Kleber, was hält ihre Cluster zusammen? Durch Auswertung großer Krebsgenbanken fanden die Forschenden, dass TNBC-Tumoren verstärkt Gene exprimieren, die mit dem äußeren Gerüst der Zelle, der extrazellulären Matrix, zusammenhängen. Ein auffälliges Gen, HAS2, kodiert für ein Enzym, das Hyaluronan (HA) herstellt — ein langes, zuckerartiges Polymer, das Zellen umhüllt. Hohe HAS2- und HA-Level standen stark im Zusammenhang mit aggressiven, metastatischen Tumoreigenschaften.
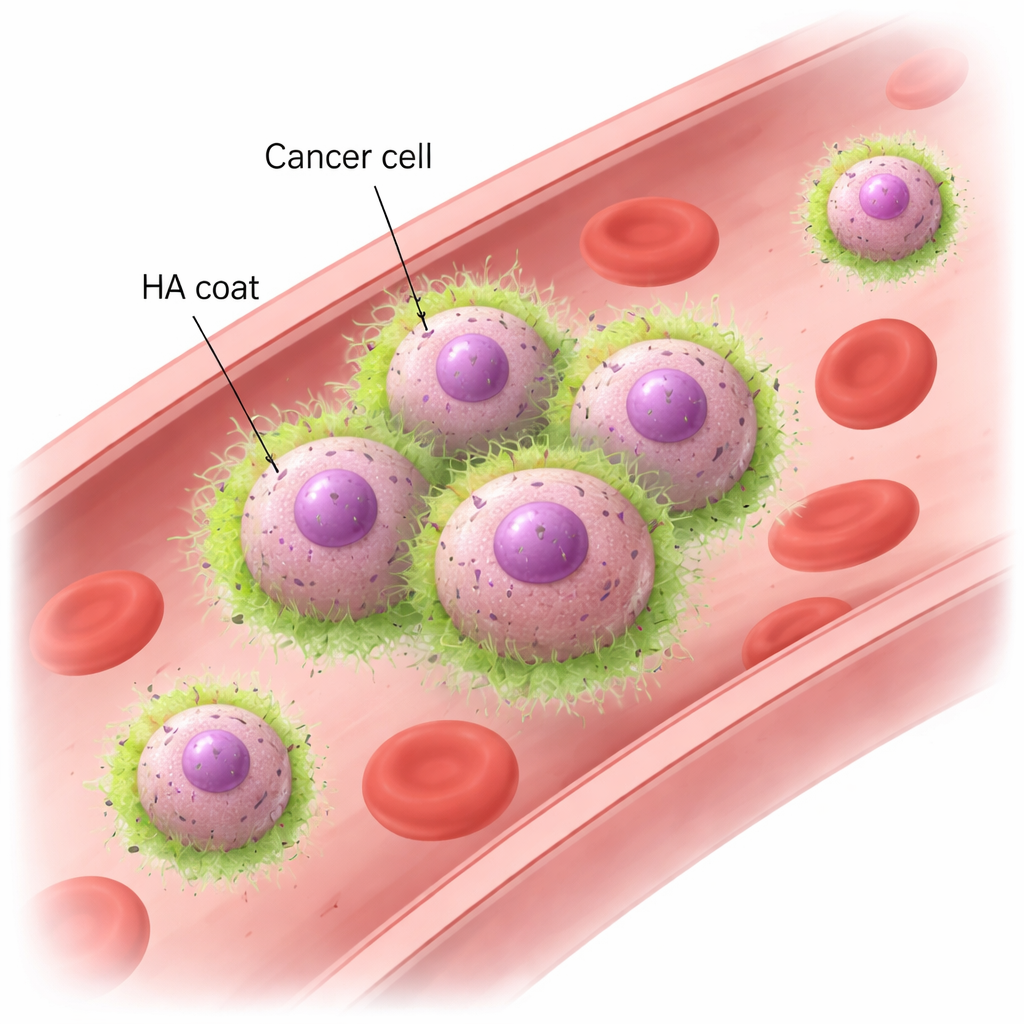
Hyaluronan und CD44: Ein neuer Weg, wie Zellen Händchen halten
In Mausmodellen und humanen Brustkrebszelllinien zeigte das Team, dass metastatische TNBC-Zellen schnell Cluster bilden, wenn sie strömendem Fluid ausgesetzt werden, das den Blutfluss nachahmt. Diese Cluster bleiben auch unter Kräften stabil, wie sie in echten Blutgefäßen auftreten, während weniger aggressive Brustkrebszellen auseinanderfallen und als Einzelne treiben. Die Mikroskopie zeigte, dass die metastatischen Zellen von einem HA-„Mantel“ umgeben sind, der genau an den Stellen konzentriert ist, an denen sich Zellen berühren. Die Entfernung von HA durch Enzyme oder die Herunterregulierung von HAS2 führte dazu, dass die Zellen unter Strömung ihre Clusterbildungsfähigkeit verloren, obwohl sie sich im ruhenden Zustand noch gemeinsam absetzen konnten. Der entscheidende Partner auf der Zellseite ist CD44, ein verbreiteter Oberflächenrezeptor, der HA bindet. Zellen ohne CD44 konnten HA nicht auf ihrer Oberfläche halten und bildeten keine Cluster mehr. Umgekehrt erlangten ursprünglich nicht-clusternde Zellen, die so verändert wurden, dass sie sowohl HAS2 als auch CD44 produzieren, eine ausgeprägte Fähigkeit zur Clusterbildung. Diese Experimente zeigten, dass die Wechselwirkung von HA mit CD44 sowohl notwendig als auch ausreichend ist, damit Krebszellen in schnell fließendem Blut zusammenkleben.
Winzige Vorsprünge und mechanische Schlösser bauen stabile Cluster
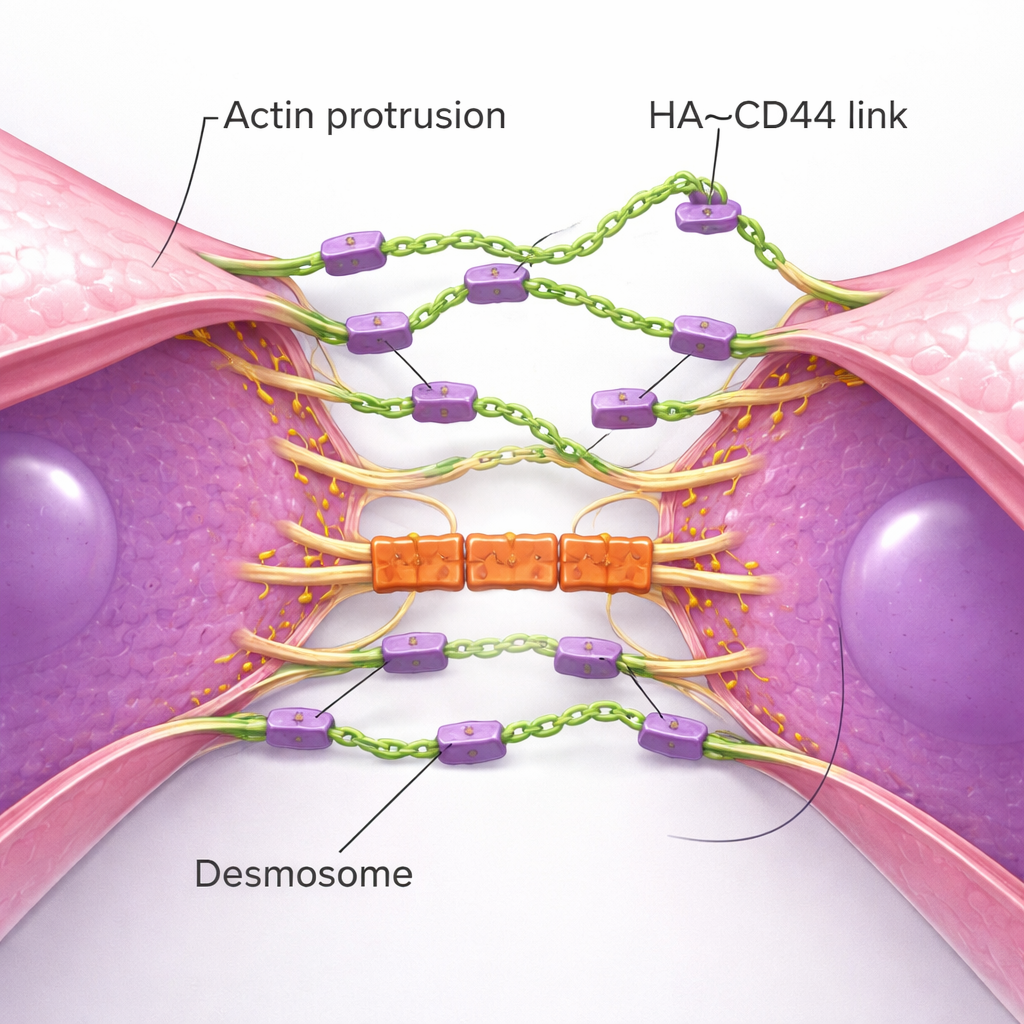
Hochauflösende Bildgebung enthüllte die physikalische Choreografie der Clusterbildung. Einzelne TNBC-Zellen strecken zahlreiche dünne, actinbasierte Membranvorsprünge aus — wie Fühler —, die mit CD44 besetzt und an ihren Spitzen mit HA versehen sind. Treffen zwei Zellen nahe aufeinander, begegnen sich zuerst diese Fühler und bilden initiale HA–CD44-Brücken. Im Laufe der Zeit gleiten die Vorsprünge aneinander vorbei und ziehen die ganzen Zellkörper näher zusammen, bis große Membranflächen nahezu nebeneinanderliegen. Dieser Prozess ähnelt dem Aufbau von Adherens-Junctions in normalen epithelialen Zellen, wird hier jedoch von einem flexiblen Zuckermantel statt starrer Proteinketten angetrieben. Während die Kontaktzone reift, kommt eine zweite Strukturgruppe hinzu: Desmosomen, robuste Verbindungen, die Zellmembranen mit dem inneren Gerüst verknüpfen. Desmosomale Proteine reichern sich erst nach Etablierung des HA-basierten Kontakts an und wirken als mechanische „Schlösser“, die den Clustern helfen, den Zerreißkräften des Blutflusses zu widerstehen. Werden Desmosomenkomponenten reduziert, bilden sich zwar Cluster, diese gehen aber bei höherer Scherbelastung auseinander.
Warum Clustering für Überleben und Metastasenbildung wichtig ist
Das HA-basierte Clustering-System erwies sich als mehr als nur ein Zusammenbleibenmechanismus; es steigerte direkt das Überleben. Unter längerer simulierter Blutströmung zeigten HA-reiche Cluster deutlich niedrigere Werte schädlicher reaktiver Sauerstoffspezies und wesentlich weniger Zelltod als HA-depletierte Einzelzellen. In Mausmodellen produzierten TNBC-Zellen ohne HAS2 deutlich weniger CTCs, bildeten nur winzige Cluster und erzeugten dramatisch weniger Lungenmetastasen — obwohl ihre Primärtumoren genauso gut wuchsen. Wurden vorgebildete Cluster aus Kontroll- und HAS2-defizienten Zellen in Mäuse injiziert, kolonisierten die HA-armen Zellen die Lunge wesentlich seltener erfolgreich. Zudem konnten HA-beschichtete CTCs andere Zellen „rekrutieren“ — sowohl Krebszellen ohne HA als auch normale Immunzellen wie Neutrophile — in gemischte Cluster, sofern diese Partner CD44 exprimierten. Blutproben von Patientinnen mit metastasiertem TNBC zeigten dasselbe Muster: CTCs trugen oft einen HA-Mantel, mit HA-Anreicherung an Kontaktstellen zwischen Tumorzellen und zwischen Tumor- und Nicht-Tumorzellen.
Was das für Patientinnen und künftige Therapien bedeutet
Für Nicht-Fachleute lautet die Hauptbotschaft: Einige der tödlichsten Brustkrebszellen reisen nicht allein, sondern als kleine, kooperative Teams, die durch einen zuckerartigen Außenschicht und ihren Rezeptor zusammengehalten werden, statt durch die klassischen Zell–Zell-„Nieten“ normaler Gewebe. Dieser HA–CD44-basierte Mechanismus hilft Tumorzellen, den harten Bedingungen des Blutflusses zu trotzen, sich miteinander und mit unterstützenden Blutzellen zu verbünden und effizienter neue Tumoren in entfernten Organen zu begründen. Die Hemmung der HA-Produktion (z. B. durch Blockade von HAS2) oder das Unterbrechen der Interaktion zwischen HA und CD44 könnte theoretisch diese Cluster schwächen und TNBC die Metastasierung erschweren — ein neuer Ansatzpunkt für künftige anti-metastatische Therapien.
Zitation: Bobkov, G.O., Patel, K.J., Lege, B.M. et al. Extracellular matrix mediates circulating tumor cell clustering in triple-negative breast cancer metastasis. Nat Commun 17, 1352 (2026). https://doi.org/10.1038/s41467-026-69007-w
Schlüsselwörter: triple-negativer Brustkrebs, zirkulierende Tumorzellen, Hyaluronan, CD44, Metastase