Clear Sky Science · de
Escherichia coli fördert die Metastasierung kolorektaler Karzinome durch Erhalt von Enhancer‑Promoter‑Schleifen über Freisetzung von Neutrophilen‑extrazellulären Netzen
Darmkeime und die geheime Autobahn des Krebses
Beim kolorektalen Krebs ist es häufig nicht der ursprüngliche Tumor im Darm, der tötet, sondern die Ausbreitung von Krebszellen in die Leber. Diese Studie deckt einen unerwarteten Komplizen auf dieser Reise auf: ein häufiger Darmkeim, Escherichia coli. Indem die Forschenden die Ereigniskette vom Bakterium im Darm bis zu aggressiven Tumoren in der Leber verfolgten, zeigen sie, wie Mikroben, Immunzellen und die DNA‑Architektur innerhalb von Krebszellen zusammenwirken können, um Metastasen zu begünstigen — und deuten neue Möglichkeiten an, diese Kette zu durchbrechen.
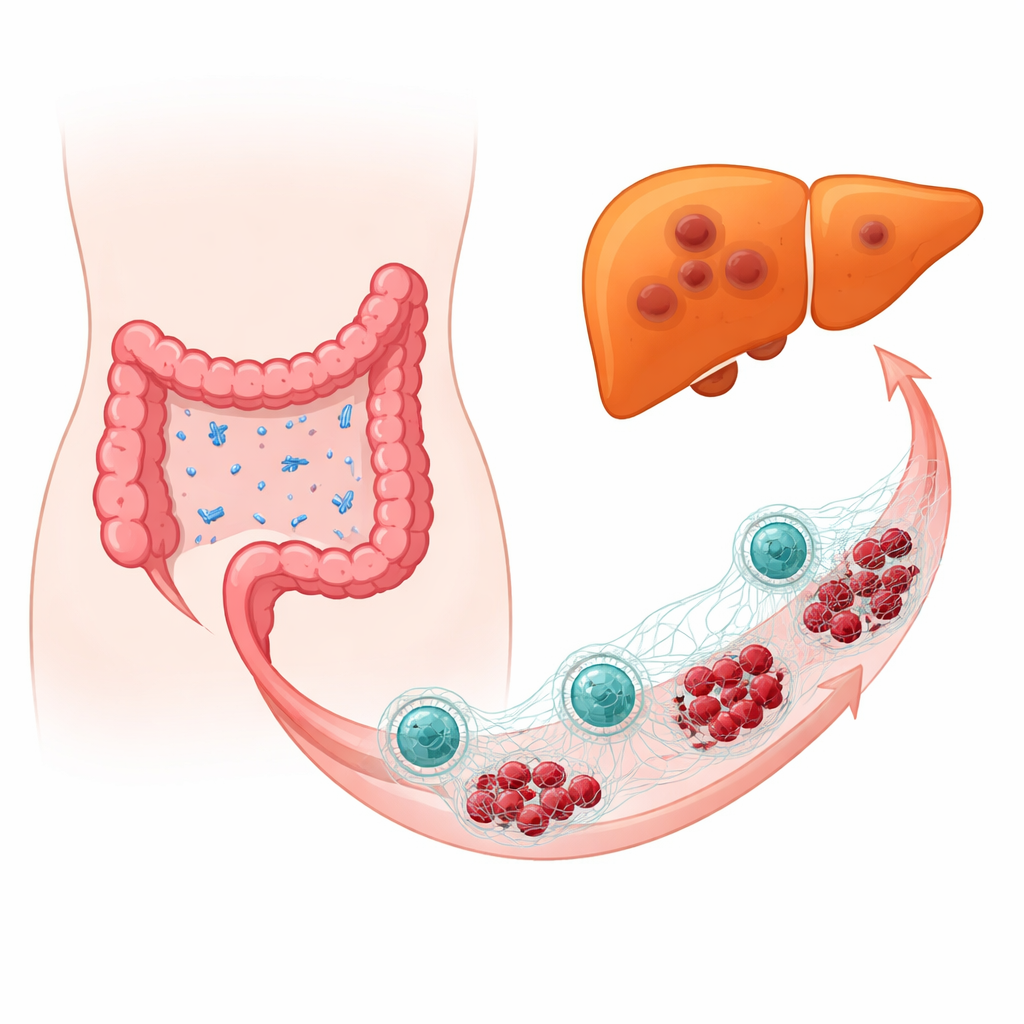
Wenn freundliche Bakterien feindlich werden
Das Team untersuchte Tumorproben von Menschen mit kolorektalem Krebs und verglich Proben von Patientinnen und Patienten, deren Krebs bereits in die Leber gestreut hatte, mit solchen ohne Lebermetastasen. Mittels hochauflösender DNA‑basierter Mikrobiomprofilierung fanden sie, dass E. coli in Tumoren, die bereits die Leber besiedelt hatten, deutlich häufiger vorkam. In Mausmodellen und in Mäusen mit humanisiertem Immunsystem führte das gezielte Anbringen von E. coli in der Nähe kolorektaler Tumore zu größeren und häufigeren Lebermetastasen und trieb Tumorzellen in einen beweglicheren, invasiveren Zustand. Selbst nachdem mit Antibiotika die meisten normalen Darmflora entfernt und nur E. coli wieder eingeführt worden war, förderten die Bakterien weiterhin Tumorwachstum und -ausbreitung — ein Hinweis darauf, dass E. coli selbst und nicht eine allgemeine Störung des Mikrobioms verantwortlich ist.
Immunnetze, die dem Krebs zur Flucht verhelfen
Neutrophile — die vordersten Immunzellen, die normalerweise Mikroben einfangen und töten — erwiesen sich als entscheidende Vermittler. Als Reaktion auf E. coli setzten Neutrophile netzartige Strukturen frei, sogenannte extrazelluläre Fallen, bestehend aus DNA und toxischen Proteinen. Diese Netze sollen Bakterien fangen, schützten in diesem Kontext aber ungewollt die Krebszellen und stärkten sie. Wenn die Forschenden die Netze enzymatisch auflösten oder Schlüsselenzyme blockierten, die zu ihrer Bildung nötig sind, verkleinerten sich die Lebermetastasen und die Tumoren wurden weniger aggressiv. Auch die Reduktion der Neutrophilen hatte einen ähnlichen Schutzeffekt — ein Paradoxon: Die Immunantwort, die eigentlich vor Infektionen schützt, wurde hier gekapert, um die Krebsausbreitung zu fördern.
Von elektrischen Signalen zu Gen‑Schaltern
Wie können klebrige DNA‑Netze außerhalb einer Tumorzelle beeinflussen, was tief im Zellkern passiert? Die Antwort liegt im Calcium, einem einfachen Ion, das als elektrisches Signal in Zellen fungiert. Die Studie zeigte, dass Neutrophilen‑Netze die Menge eines Kanalproteins, TRPC1, auf kolorektalen Krebszellen erhöhten. TRPC1 ließ zusätzliches Calcium in die Zelle strömen, was wiederum einen calcium‑sensitiven Regulator namens NFATC3 aktivierte und eine sich selbst verstärkende Schleife erzeugte, die TRPC1‑Spiegel hochhielt. Dieser Calciumanstieg förderte das Zusammenlagern der kleinen Proteine S100A8 und S100A9, die dann an das bedeutende Wachstumssteuerungsprotein STAT3 bindeten. Das Trio wanderte in den Zellkern, wo es etwas besonders Auffälliges tat: Es trug dazu bei, die DNA so zu biegen und zu schleifen, dass entfernte Regulationsregionen und Genstartstellen miteinander in Kontakt kamen und dadurch die physische Stabilisierung von „Enhancer–Promoter‑Schleifen“ förderten, die bestimmte Gene hochregulieren.
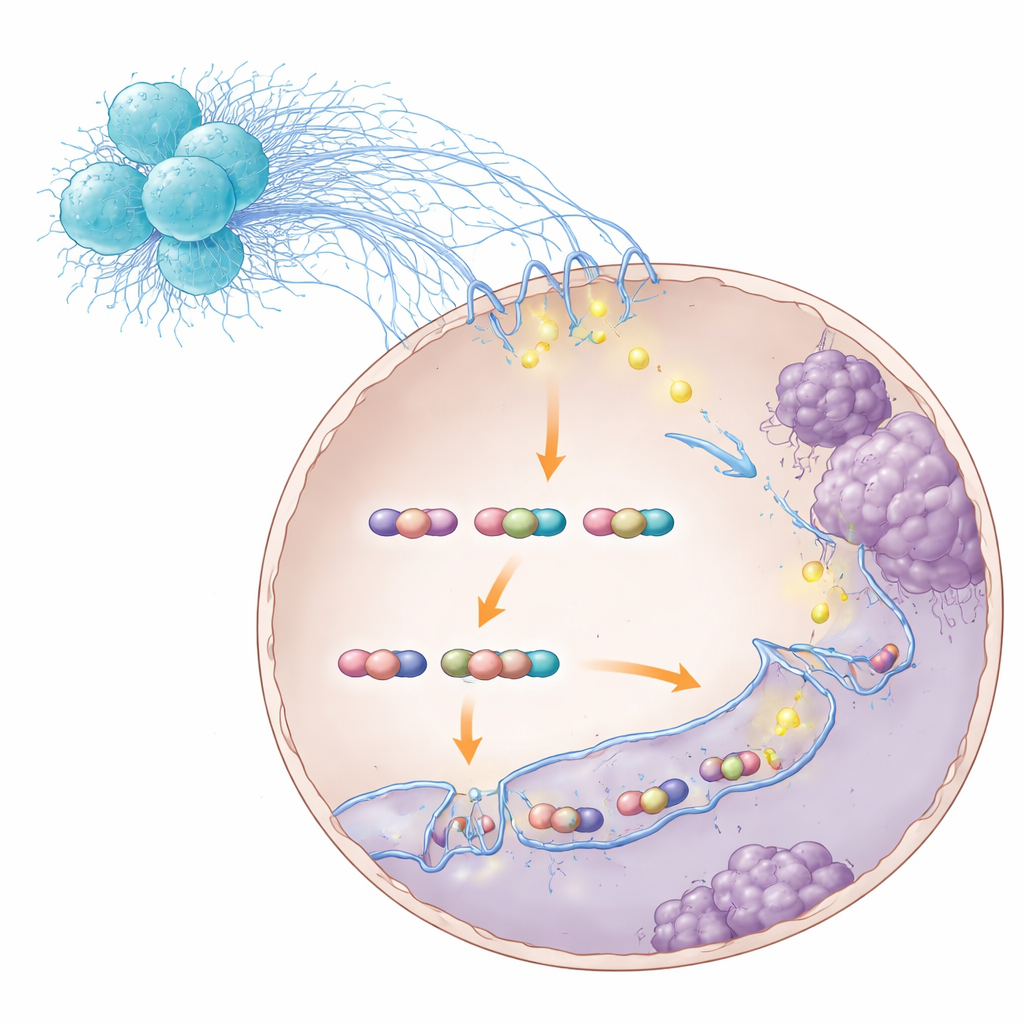
Umschaltung von Krebszellen zugunsten der Metastasierung
Durch Kartierung der dreidimensionalen Kontakte im Genom fanden die Forschenden, dass der STAT3–S100A8/9‑Komplex Schleifen förderte, die Gene aktivierten, die an Zellbewegung und Invasion beteiligt sind. Ein besonders auffälliges Gen war TNS1, das Zellen dazu bringt, ihre Verankerungen zu lockern und leichter zu migrieren. Wurde der STAT3–S100A8/9‑Komplex gestört, schwächten oder verschwanden viele dieser Schleifen, die TNS1‑Spiegel sanken, und die Krebszellen verloren einen Teil ihrer Fähigkeit zu invasivem Verhalten und zur Leberbesiedlung. Wichtig ist, dass diese Störung nicht verhinderte, dass STAT3 überhaupt noch DNA berührte — vielmehr destabilisierte sie spezifisch die Schleifenarchitektur, die metastatische Programme verstärkt. In Tiermodellen reduzierte das Blockieren verschiedener Schritte dieser Kette — von dem bakteriellen Sensorsignal RIPK2 in Neutrophilen über S100A8/9 bis hin zu STAT3 selbst — die Lebermetastasierung und verbesserte das Überleben.
Die Kette zwischen Keimen und Tumoren durchtrennen
Für Nicht‑Spezialisten lautet die Kernbotschaft: Ein häufiger Darmkeim kann die Ausbreitung kolorektalen Krebses begünstigen, indem er zunächst Immunzellen dazu veranlasst, DNA‑Netze auszubringen, und diese Netze dann einen calciumgetriebenen Signalweg auslösen, der die Schaltvorgänge von Krebsgenen umbaut. Statt breit wirkender Antibiotika, die nützliche Mikroben schädigen und die Krebsimmuntherapie abschwächen können, weist die Arbeit auf präzisere Arzneiziele hin: bakterielle Sensoren wie RIPK2, die TRPC1–Calcium–S100A8/9‑Kaskade und die STAT3‑gesteuerten DNA‑Schleifen, die metastaserelevante Gene hochschalten. Das Unterbrechen dieser Kette an einem oder mehreren Punkten könnte eine neue Strategie bieten, um zu verhindern, dass kolorektaler Krebs aus einem lokalen Darmproblem eine tödliche Lebererkrankung wird.
Zitation: Pan, B., Yao, Y., Zhang, Z. et al. Escherichia coli promotes colorectal cancer metastasis by maintaining enhancer-promoter loops through releasing neutrophil extracellular traps. Nat Commun 17, 2290 (2026). https://doi.org/10.1038/s41467-026-69005-y
Schlüsselwörter: Metastasierung kolorektaler Karzinome, Darmmikrobiom, Neutrophilen‑extrazelluläre Netze, STAT3‑Signalweg, epigenetische Genregulation