Clear Sky Science · de
Kovalente Inhibitor-Entwicklung führt zu Aktivität gegen sowohl GDP- als auch GTP-gebundene Formen von KRAS G12C
Warum das für künftige Krebstherapien wichtig ist
Krebsarten, die durch Mutationen im Gen KRAS angetrieben werden, galten lange als besonders schwer behandelbar. Jüngst sind neue Medikamente, die eine häufige mutante Form, KRAS G12C, ausschalten, für Patientinnen und Patienten verfügbar geworden und haben dieses Bild begonnen zu ändern. Diese Studie untersucht eine noch ehrgeizigere Frage: Kann man Wirkstoffe so entwerfen, dass sie KRAS G12C in beiden seinen hauptsächlichen Funktionszuständen in der Zelle blockieren, und würde das die Krebsbehandlung schneller, wirkungsvoller oder dauerhafter machen?
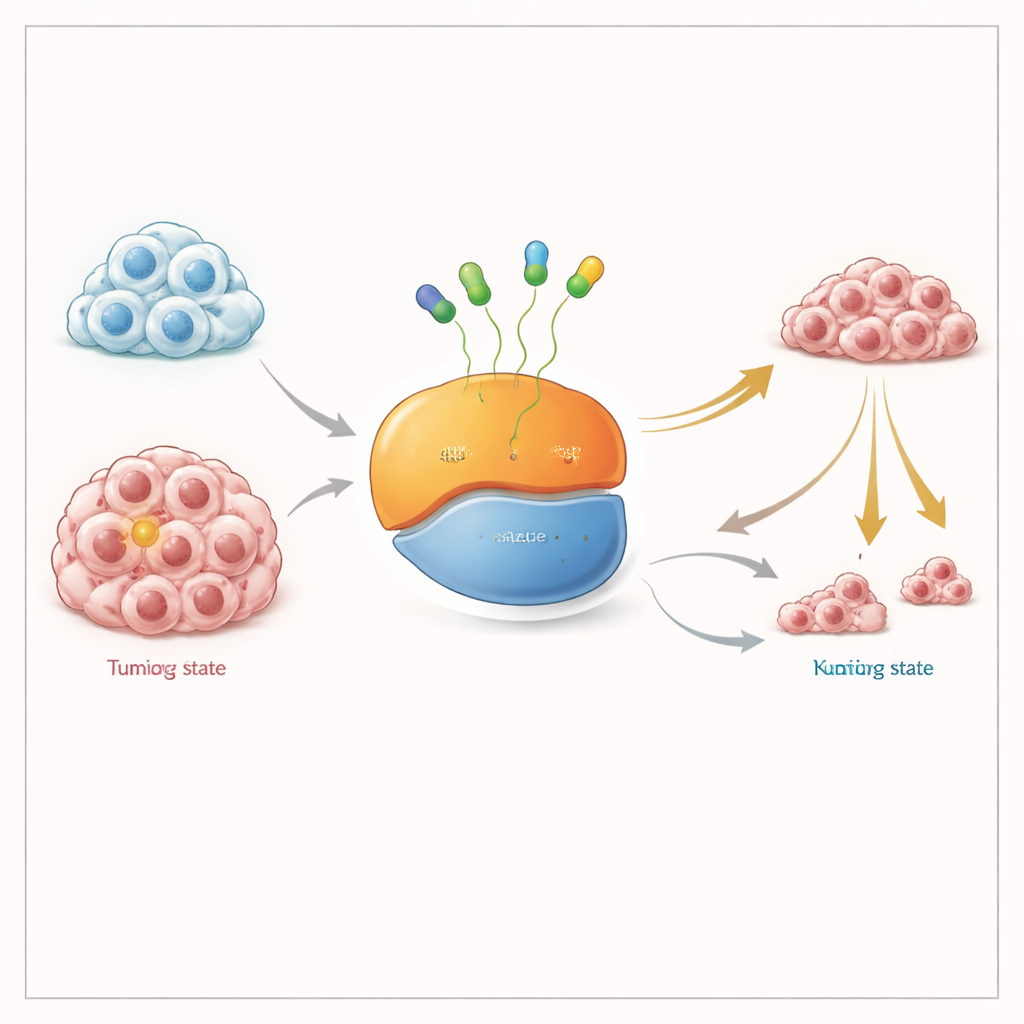
Den molekularen Lichtschalter an zwei Stellen ausknipsen
KRAS wirkt wie ein winziger Ein-/Ausschalter für Wachstumssignale der Zelle. Er wechselt zwischen einem „aus“-Zustand, in dem er ein Energieträgermolekül (GDP) hält, und einem „ein“-Zustand, in dem er ein anderes (GTP) trägt. Die KRAS G12C‑Mutation hält diesen Schalter teilweise eingeschaltet und treibt so Tumorwachstum an. Zugelassene Medikamente binden an die „aus“-Form und fixieren sie; mit der Zeit werden dadurch nach und nach viele mutante Proteine außer Gefecht gesetzt. Viele Forschende haben argumentiert, dass ein Wirkstoff, der KRAS in beiden Zuständen greifen kann, besser wirken sollte, insbesondere in Tumoren, die durch Verlagerung des Gleichgewichts in Richtung des aktiven Zustands resistent werden.
Entwicklung eines neuen molekularen Hakens
Die Autorinnen und Autoren machten sich daran, solche Doppelzweck‑Wirkstoffe zu entwickeln. Sie konzentrierten sich auf eine kleine Vertiefung in der Nähe einer flexiblen Region von KRAS, genannt Switch II, an der bereits bestehende Wirkstoffe binden. Anstatt die Affinität ihrer Moleküle für diese Tasche zu verändern, überarbeiteten sie den „Warhead“-Teil, der eine permanente chemische Bindung an die mutierte Cystein‑Aminosäure an Position 12 eingeht. Durch Computermodellierung und Synthese Dutzender Varianten entdeckten sie einen besonderen dreiteiligen Warhead, der die Cysteinseite aus einem leicht anderen Winkel annähert. Diese subtile Verschiebung schafft genug Platz für das sperrigere GTP‑Molekül, sodass die neuen Verbindungen an KRAS binden können, egal ob GDP oder GTP gebunden ist. Biochemische Tests bestätigten, dass führende Verbindungen die Interaktion von KRAS mit einem wichtigen Signalkopplungspartner, RAF, in beiden Zuständen stören konnten.
Beobachtung, wie sich das Protein umformt
Um zu verstehen, warum diese Moleküle wirkten, ermittelten die Forschenden hochaufgelöste Kristallstrukturen des Wirkstoffs gebunden an KRAS. Diese Schnappschüsse zeigten, dass der neue Warhead an einer ungewöhnlichen Stelle des chemischen Gerüsts reagiert, dabei ein Fluoratom abspaltet und eine kovalente Bindung an einem anderen Kohlenstoff eingeht als typische Krebsmedikamente, die Cysteine anvisieren. Diese veränderte Chemie hilft dem Wirkstoff, auch bei Anwesenheit von GTP in die Switch-II‑Tasche zu passen. Die Strukturen zeigten außerdem, dass die Bindung des Inhibitors ein winziges Wassermolekül verschiebt und eine andere Schleife, Switch I, subtil umordnet, die normalerweise Kontakt zu nachgeschalteten Signalproteinen hat. Diese allosterische Umgestaltung zieht zwei Aminosäuren näher zusammen, so dass eine enge Salzbrücke entsteht und die Oberfläche so verzerrt wird, dass RAF nicht mehr andocken und Wachstumssignale weiterleiten kann.
Schnelles Abschalten, aber keine stärkere Langzeitwirkung
Mit diesen strukturellen Erkenntnissen verfeinerten die Forschenden zwei Wirkstoffkandidaten, die effizient und selektiv an KRAS G12C binden, während sie andere cysteinhaltige Proteine größtenteils verschonen. In Krebszelllinien blockierten diese Doppelzustands‑Inhibitoren rasch eine zentrale Signalübertragungsachse, bekannt als MAPK‑Weg, messbar durch den Verlust eines chemischen Markers am ERK‑Protein und eine starke Unterdrückung des Zellwachstums. Sie inaktivierten KRAS in Zellen schneller als ein Referenzwirkstoff, der nur die inaktive Form anvisiert. In Maus‑Tumormodellen zeigte ein Wirkstoffkandidat gute orale Bioverfügbarkeit, bildete schnell kovalente Bindungen zum Ziel und verkleinerte Tumoren oder verlangsamte deren Wachstum. Dennoch ergab der Vergleich von Doppelzustands‑ und inaktiv‑zustands‑Wirkstoffen über längere Zeiträume, dass beide Klassen schließlich ähnliche Grade an KRAS‑Abschaltung, Signalweghemmung und Tumorkontrolle erreichten.
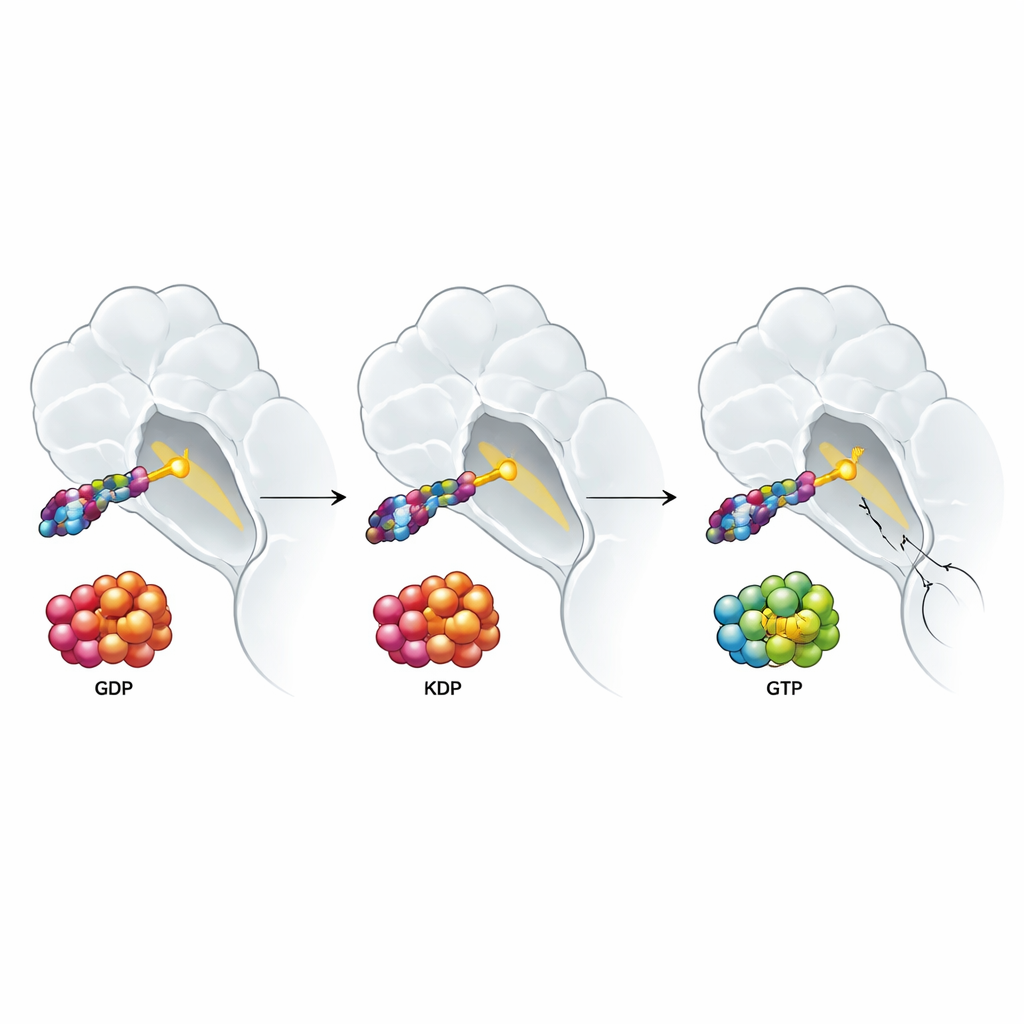
Warum Wachstumssignale aus der Tumorumgebung trotzdem dominieren
Die Studie untersuchte außerdem, wie Signale aus der Tumorumgebung die Wirksamkeit dieser Medikamente beeinflussen. Wachstumsfaktoren wie EGF und HGF, die in der Umgebung vieler Tumoren reichlich vorhanden sind, drängen RAS‑Proteine in den aktiven, GTP‑geladenen Zustand und sind dafür bekannt, die Ansprechbarkeit auf gezielte Therapien zu dämpfen. Man könnte erwarten, dass ein Wirkstoff, der die aktive Form von KRAS G12C bindet, dieses Problem umgeht. Stattdessen stellten die Autoren fest, dass sowohl Doppelzustands‑ als auch Inaktiv‑zustands‑Inhibitoren an Wirksamkeit verlieren, wenn solche Wachstumsfaktoren präsent sind. Detaillierte Experimente deuteten auf einen überraschenden Schuldigen hin: die Aktivierung der normalen, nicht mutierten RAS‑Formen (H‑RAS und N‑RAS), die KRAS G12C umgehen und das Fließen von Wachstumssignalen aufrechterhalten können. Als die Forschenden H‑RAS und N‑RAS in einer Lungenkrebszelllinie löschten, verschwand der wachstumsfaktor‑getriebene Resistenzmechanismus größtenteils für alle Typen von KRAS G12C‑gerichteten Wirkstoffen, während ein Wirkstoff, der einen nachgeschalteten Schritt im Weg blockiert, von vornherein weniger betroffen war.
Was das für Patientinnen, Patienten und Wirkstoffentwicklung bedeutet
Insgesamt zeigt die Arbeit, dass es chemisch und strukturell möglich ist, kovalente KRAS G12C‑Wirkstoffe zu entwickeln, die das Protein in beiden seinen Ein‑ und Aus‑Zuständen greifen, und dass diese Doppelzustands‑Inhibitoren die Signalübertragung schneller herunterfahren können als bestehende Medikamente. Die schnelle Bindung führte jedoch in präklinischen Modellen nicht zu klar besseren Tumorkontrolle oder zu einer Lösung des durch Wachstumsfaktoren verursachten Resistenzproblems. Für Patientinnen und Patienten deutet dies darauf hin, dass die bloße Ergänzung der Aktivität gegen die aktive KRAS‑Form möglicherweise nicht ausreicht; Kombinationsstrategien, die auch andere RAS‑Familienmitglieder oder nachgeschaltete Signalwege adressieren, könnten nötig sein. Der neue Warhead und die hier vorgestellte strukturelle Blaupause erweitern dennoch das Werkzeugkasten zum Targeting von KRAS und werden künftige Generationen präziser Krebstherapien informieren.
Zitation: Condakes, M.L., Zhang, Z., Danahy, D.B. et al. Covalent inhibitor design confers activity against both GDP- and GTP-bound forms of KRAS G12C. Nat Commun 17, 2233 (2026). https://doi.org/10.1038/s41467-026-69003-0
Schlüsselwörter: KRAS G12C, kovalenter Inhibitor, Doppelzustands-Inhibition, MAPK-Signalübertragung, Arzneimittelresistenz