Clear Sky Science · de
Chemische Anfärbung für Grundlagenstudien und Optimierung von Bindemitteln in Li‑Ionen‑Batterie‑Negativelektroden
Das verborgene Klebemittel in Batterien sichtbar machen
Lithium‑Ionen‑Batterien betreiben unsere Telefone, Autos und bald ganze Stadtviertel, doch eine entscheidende Zutat in ihrem Inneren ist nahezu unsichtbar: das Bindemittel, ein dünnes Polymer‑„Klebe“mittel, das Partikel zusammenhält. Diese Arbeit zeigt eine neue Methode, das verborgene Bindemittel chemisch zu „anfärben“, sodass es im Elektronenmikroskop sichtbar wird. Indem man endlich erkennt, wo das Bindemittel tatsächlich sitzt, zeigen die Autoren Wege zu langlebigeren, schneller ladenden Batterien und zur Verbesserung von Fabrikationsprozessen, die bisher weitgehend auf Versuch und Irrtum beruhten.
Warum die Verteilung des Bindemittels wichtig ist
In einer typischen Negativelektrode macht das aktive Material wie Graphit über 95 % des Volumens aus; weniger als 5 % entfallen auf Bindemittel und leitendes Kohlenstoff, die mechanische Festigkeit und elektrische Verbindungen liefern. Trotz dieses geringen Anteils beeinflusst die räumliche Verteilung des Bindemittels stark, wie gut Partikel aneinander und am metallischen Stromabnehmer haften, wie leicht sich Elektronen und Ionen bewegen und wie stabil die Oberflächenschichten beim Zyklisieren sind. Bisher war es extrem schwierig, zu kartieren, wohin wasserbasierte Bindemittel in kommerziellen Graphit‑ und Graphit‑Silizium‑Electroden wandern, sodass Ingenieure meist die Chemie des Bindemittels änderten, statt seine Verteilung zu steuern.
Das unsichtbare Bindemittel zum Leuchten bringen
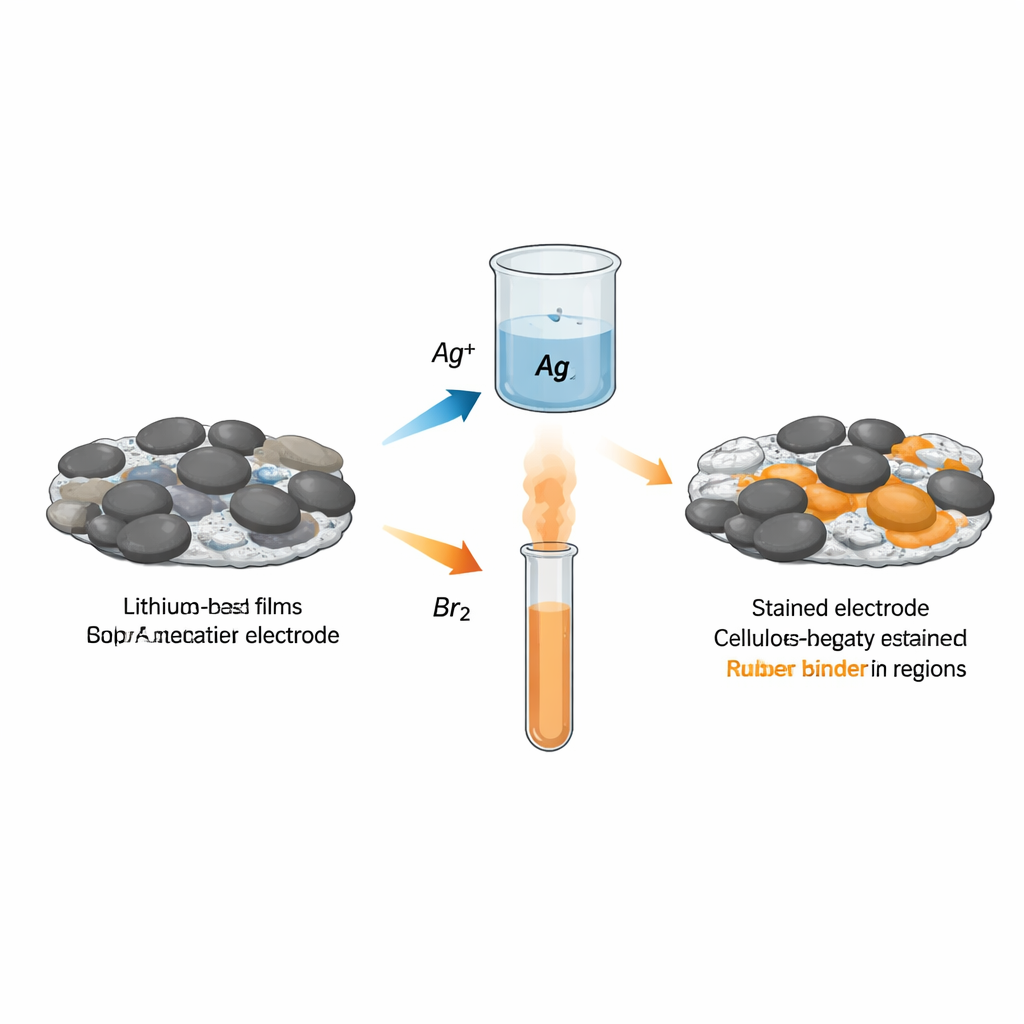
Die Autoren stellen zwei einfache chemische Anfärbungen vor, zugeschnitten auf die am weitesten verbreiteten wasserverarbeitbaren Bindemittel: Carboxymethylcellulose (CMC) und Styrol‑Butadien‑Kautschuk (SBR). Das Eintauchen einer Elektrode in eine Silbernitratlösung lässt Silberionen selektiv an saure Gruppen in CMC binden, während die Exposition gegenüber Bromdampf Bromatome an Doppelbindungen in SBR anlagert. Diese zusätzlichen Silber‑ oder Bromatome sind schwer genug, um in rückstreuenden Elektronenbildern hervorzustechen und lassen sich präzise mittels Röntgenspektroskopie messen. Tests an reinen Bindemittelfilmen und gemischten Elektroden bestätigen, dass Silber CMC und Brom SBR mit guter Spezifität und Empfindlichkeit bei realistischen Bindemittelanteilen nachverfolgt.
Verborgene Filme und fragile Strukturen offenbaren
Mit den eingefärbten Elektroden untersuchte das Team die Bindemittelorganisation mit fortschrittlicher Elektronenbildgebung auf mehreren Skalen. Auf dem Mikrometermaßstab identifizierten sie verschiedene Typen bindemittelreicher Cluster: einige dominierten von leitfähigem Kohlenstoff und CMC, die Elektronen perkolieren lassen, andere waren stärker in Gummi‑SBR, das Elastizität beiträgt. Auf der Nanometerebene zeigte die Silberfärbung einen ultradünnen, etwa 10–15 Nanometer dicken CMC‑Film, der frische, unkomprimierte Graphitpartikel konform überzieht. Diese kontinuierliche Beschichtung war lange theoretisiert, aber selten direkt zu sehen. Auffällig zerschlug das industrielle Kalendrieren (der Warmwalzschritt zur Verdichtung von Elektroden) diesen fragilen Film in verstreute Flecken und ließ große Bereiche des Graphits in Labor‑ und kommerziellen Proben unbedeckt. Diese Fleckenhaftigkeit verändert wahrscheinlich, wo Ionen eindringen können, wo schützende Oberflächenschichten entstehen und wo schädliche Lithium‑Abscheidung beginnen kann.
Bilder in bessere Fertigung übersetzen
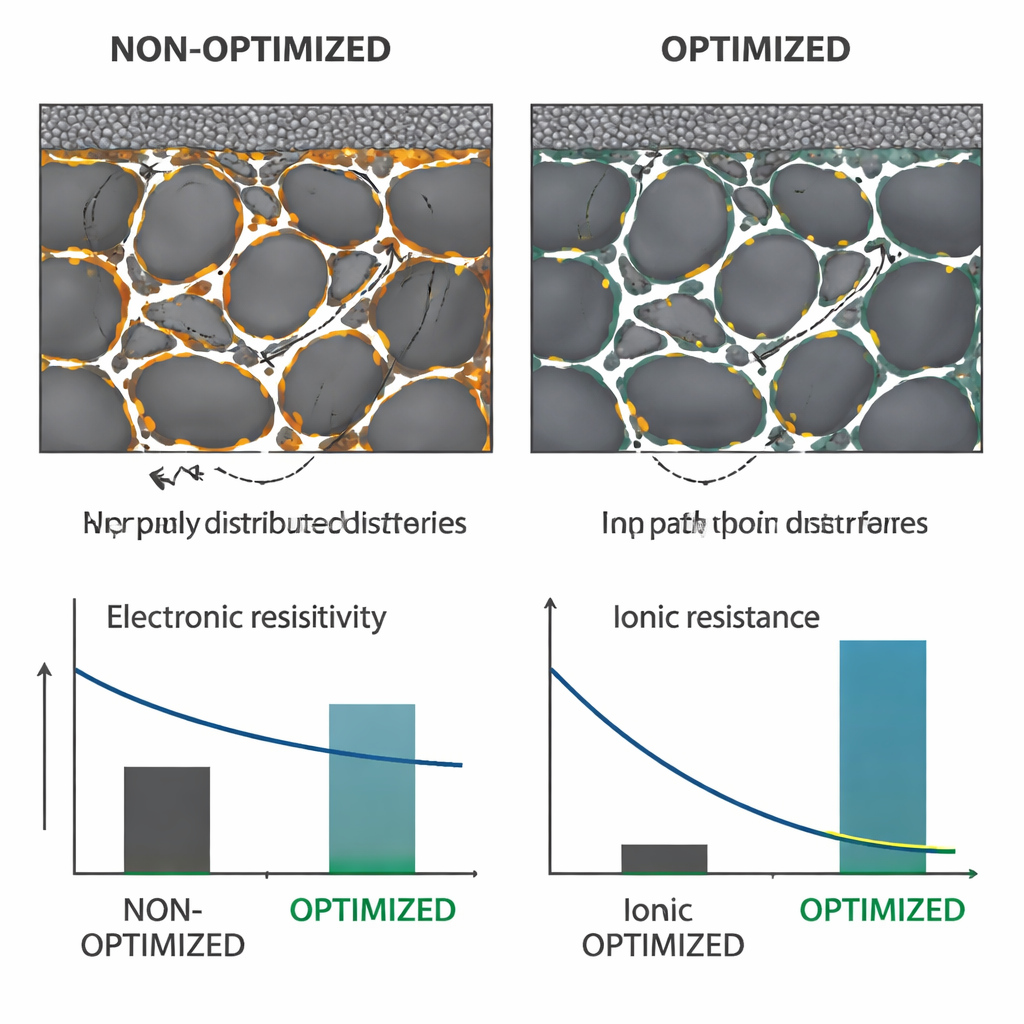
Da sich die eingefärbten Bindemittel nun messen lassen, konnten die Autoren Mikrostruktur mit Leistung und Prozessentscheidungen verknüpfen. Durch Anpassungen beim Mischen des Schlamms – insbesondere durch den Anfangseinsatz einer konzentrierteren CMC‑Lösung – reduzierten sie stark die Bildung großer Kohlenstoff‑Bindemittel‑Cluster, ohne die Gesamtrezeptur zu ändern. Das führte zu einem messbaren Rückgang des elektronischen Widerstands der Graphitbeschichtung um 14 %. In einer zweiten Studie nutzten sie die Färbung, um die Bindemittelwanderung während schneller Hochtemperatur‑Trocknung zu verfolgen, einem Engpass in industriellen Beschichtungsstraßen. Ein einfacher „Phaseninversions“-Schritt – kurzes Eintauchen der nassen Beschichtung in Aceton vor dem Trocknen – trieb mehr Bindemittel in Richtung Stromabnehmer statt zur Oberfläche. Die resultierenden Elektroden bogen sich ohne Risse, hafteten besser und zeigten etwa 40 % geringeren ionischen Widerstand durch ihre Poren, bei unveränderter Dicke, Porosität und Zusammensetzung.
Grenzen, Chancen und Bedeutung für Batterien
Die Färbemethode ist nicht universell: hochreaktive Materialien wie Nano‑Silizium oder Lithium‑Eisen‑Phosphat können mit der Chemie interferieren, und Silber oder Brom müssen an Prüfproben angewendet werden, nicht an fertigen Zellen. Trotzdem funktioniert der Ansatz gut für die dominierenden wasserbasierten Bindemittel in Graphit und vielen siliziumhaltigen Anoden und erfordert nur bescheidene Laborausstattung. Für Nicht‑Spezialisten ist die Kernbotschaft: Wie das „Klebe“mittel innerhalb einer Elektrode angeordnet ist – bis in Zehner von Nanometern – kann Leistung, Lebensdauer und Sicherheit deutlich beeinflussen. Indem Herstellern ein klares Bild der Bindemittelposition geliefert wird, eröffnet diese Arbeit praktische Wege zu schnellerem Trocknen, besserer mechanischer Robustheit und gleichmäßigeren Stromverteilungen und hilft letztlich, zuverlässigere und effizientere Lithium‑Ionen‑Batterien zu entwickeln.
Zitation: Zankowski, S.P., Wheeler, S., Barthelay, T. et al. Chemical staining for fundamental studies and optimization of binders in Li-ion battery negative electrodes. Nat Commun 17, 1438 (2026). https://doi.org/10.1038/s41467-026-69002-1
Schlüsselwörter: Lithium‑Ionen‑Batterien, Elektrodenbindemittel, Graphitanoden, Elektronenmikroskopie, Batterieherstellung